Clear Sky Science · ja
散発性およびリンチ症候群関連のマイクロサテライト不安定性大腸がんにおける腫瘍免疫の文脈と免疫逃避
がん患者にとってなぜ重要か
免疫療法は多くの大腸がん患者の見通しを変えましたが、すべての患者に効果があるわけではありません。本研究は重要な疑問を投げかけます。免疫系にとって明らかに認識されやすいはずの腫瘍が、なぜ免疫の網をすり抜けられるのか。遺伝性のリンチ症候群に関連するものと散発性のもの、二種類の遺伝的に不安定な大腸がんを比較することで、研究者たちは免疫細胞が腫瘍を取り巻き攻撃する場合と、逆に腫瘍を保護してしまう場合の重要な違いを明らかにしました。
同じ型の腫瘍に至る二つの経路
マイクロサテライト不安定性(MSI)を持つ大腸がんは多数のDNAエラーを抱え、これが異常タンパク質を生み出して免疫系にとっての目印となります。これらの腫瘍は、DNA修復の遺伝的欠損(リンチ症候群)によって生じる場合と、腫瘍内でのみ起こる変化(散発性MSI腫瘍)によって生じる場合があります。どちらの腫瘍も顕微鏡下では類似して見えますが、免疫を取り巻く環境や治療への反応は同じではありません。研究チームはフィンランドの患者から43例のMSI大腸がん(リンチ関連と散発性の両方)を集め、組織染色、全ゲノム解析、RNAシーケンスを用いて、どの免疫細胞が存在し、腫瘍がどのように破壊を回避しているかを詳細に描き出しました。
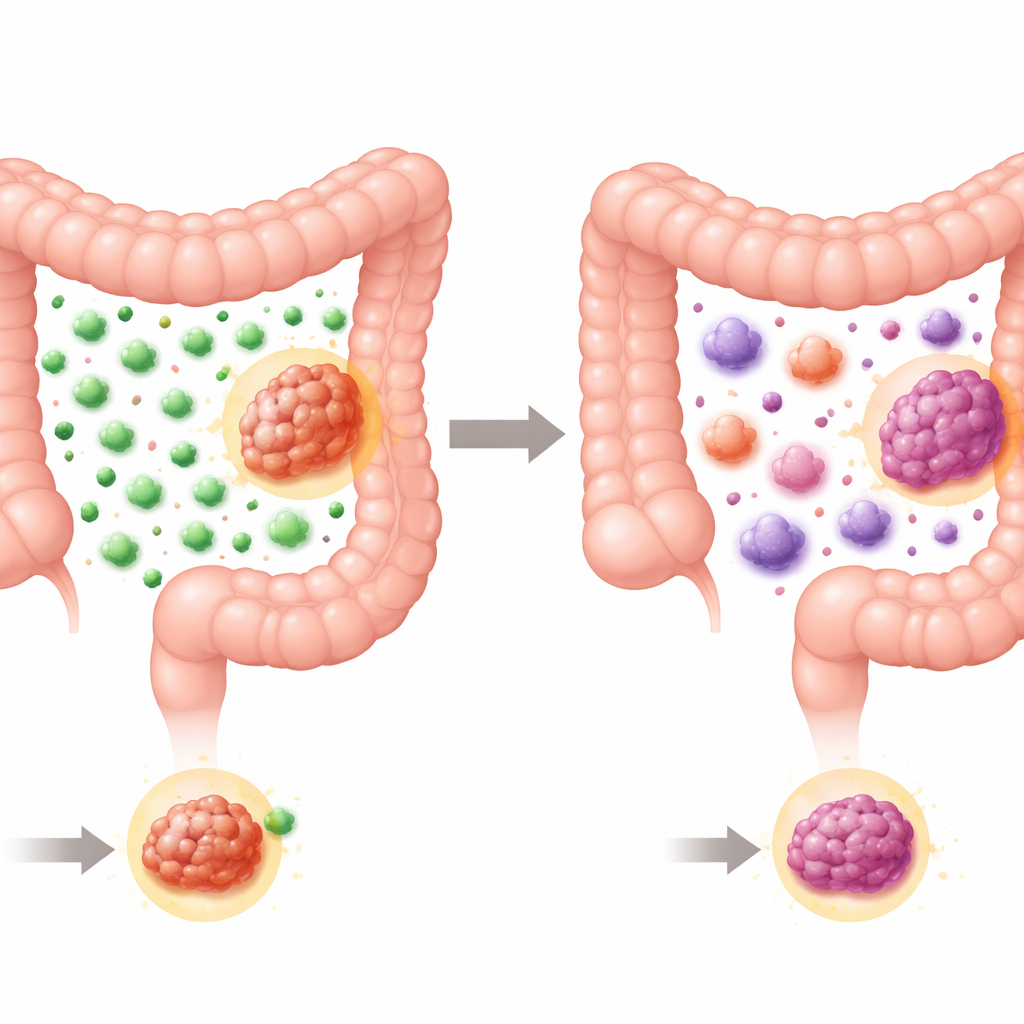
どれだけの免疫細胞が集まるか
まず研究者たちはT細胞、すなわち免疫系の標的指向の“ヒットマン”に着目しました。彼らは腫瘍中央と浸潤縁辺における総T細胞とキラーT細胞の密度を組み合わせた確立された免疫スコアを測定しました。予想どおり、MSI腫瘍は一般的な大腸がんより高いスコアを示し、T細胞を引き寄せやすいことを反映していました。しかしMSI群内を詳しく見ると明確なパターンが現れました。リンチ症候群由来の腫瘍はすべて高い免疫スコアを示したのに対し、散発性MSI腫瘍はおおよそ半々に高スコア群と低スコア群に分かれていました。つまり、遺伝性のMSI腫瘍はほぼ常に強いT細胞の浸潤を誘導する一方で、散発性MSI腫瘍はよりばらつきがあり、免疫系に対して比較的“冷たい”ものも存在するということです。
助ける細胞と妨げる細胞
次に研究は骨髄系細胞に向かいました。これはマクロファージや好中球のような自然免疫細胞で、T細胞のがん攻撃を助けることもあれば、逆に腫瘍を保護してしまうこともあります。複数のタンパク質を同時に標識するマルチプレックス染色を用いて、著者らはマクロファージを大まかに二つの性質に分類しました。炎症と腫瘍殺傷を支持するM1様細胞と、鎮静的で創傷治癒的、しばしば腫瘍促進的なM2様細胞です。リンチ由来・散発性のいずれのMSI腫瘍にも多数の骨髄系細胞が含まれていましたが、散発性腫瘍は特にM2様マクロファージが多い点で目立ち、浸潤縁辺の支持結合組織ではその差が顕著でした。その領域では、散発性腫瘍でM2様がM1様を上回ることさえありました。散発性群の中でも高いT細胞スコアを示した腫瘍はM1様マクロファージがより多く、M2様レベルは一貫して高かったことから、これら二つのマクロファージのバランスがT細胞による有効な攻撃を左右する手がかりになることが示唆されます。
遺伝的な抜け穴と腫瘍の多様性
一部のMSI腫瘍が免疫系を回避する理由を理解するため、研究者たちは腫瘍タンパク質が免疫細胞に提示される仕組みや、免疫応答にかかる“ブレーキ”に影響する遺伝的変化を調べました。リンチ由来と散発性のMSIの両方で抗原提示機構の主要構成要素に変異が頻繁に見られましたが、両群を分けるのはわずかな差にとどまりました。より顕著だったのは免疫チェックポイントシグナルの差でした。散発性腫瘍はPD-L2やCD40Lの発現が高く、これらの分子は免疫細胞の挙動を形作ることができ、既存のチェックポイント阻害剤と組み合わせて薬剤標的として注目されています。研究チームは各腫瘍が持つ潜在的ネオアンチゲンの数と、腫瘍が遺伝的に均一か混在しているか(クローン性対異質性)も測定しました。驚くべきことに、予測されるネオアンチゲン負荷が多いことが必ずしもより多くのT細胞を引き寄せることにはつながりませんでした。むしろ遺伝的により多様な腫瘍、特に散発性MSI腫瘍はネオアンチゲンを多く抱える傾向にありつつも、好中球の減少など免疫系がそれらの標的を十分に活用していないことを示唆するパターンが見られました。
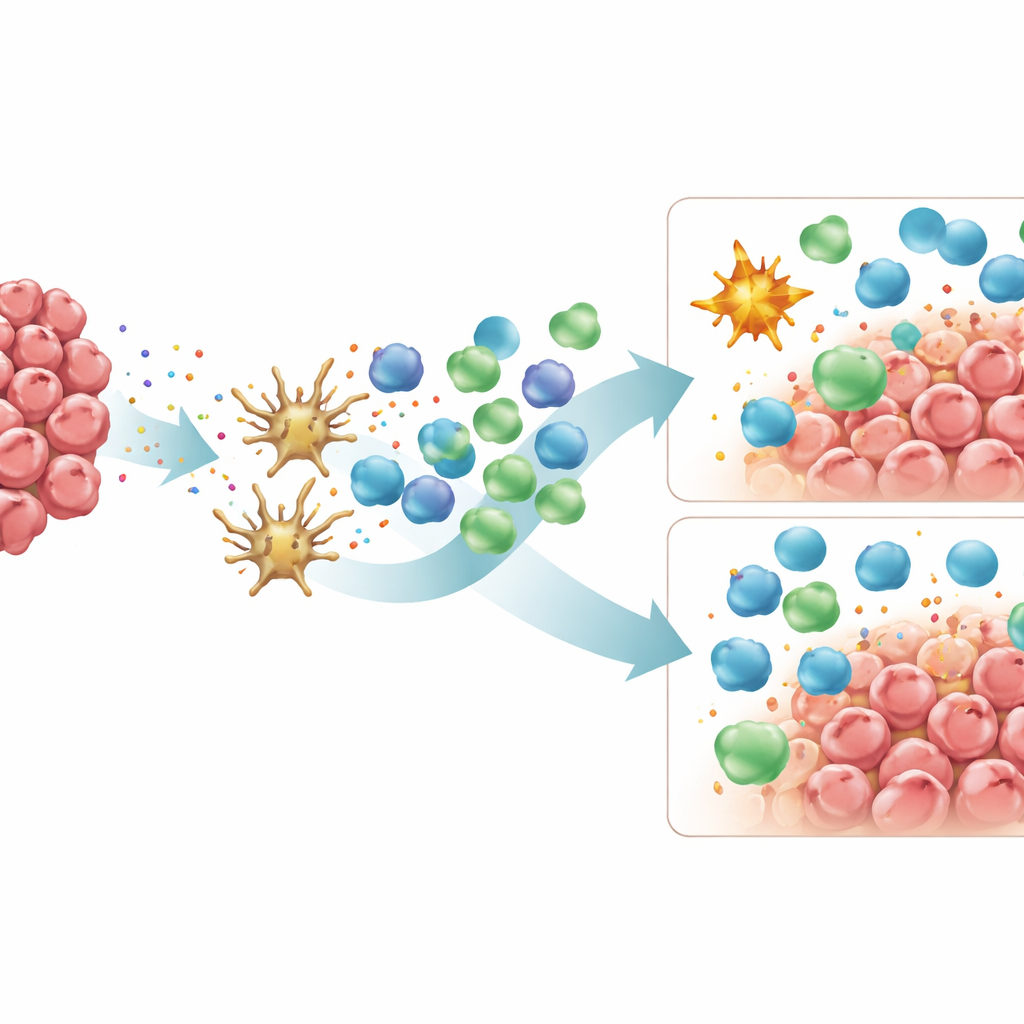
将来の治療に向けての示唆
総じて本研究は、リンチ関連MSI大腸がんを一貫してT細胞が豊富な“ホット”腫瘍として描き、散発性MSI腫瘍は強く浸潤するものと、免疫抑制的なマクロファージや特定のチェックポイント分子の高発現により抑えられたものとに分かれる混合群であることを示しています。同時に散発性腫瘍は高い遺伝的多様性と大量のネオアンチゲンをサブクローンに分散して抱えることが多く、以前の研究が示唆するようにそのパターンはT細胞応答の有効性を鈍らせる可能性があります。患者にとって、これらの知見は、高い変異率を共有していてもすべてのMSI大腸がんが免疫療法に同じように反応するわけではない理由を説明する手助けになります。また、M2様マクロファージを再プログラムするか除去する薬や、PD-L2やCD40Lのような追加チェックポイントを標的とする治療といった新たな戦略が、特に散発性MSI腫瘍に対して有望であることを示唆しています。各腫瘍の固有の免疫風景に治療をより適合させることで、大腸がんに対する免疫療法の効果を向上させ、個別化できる可能性があります。
引用: Martin, S., Elomaa, H., Väyrynen, J.P. et al. Tumour immune contexture and immune evasion in sporadic and Lynch syndrome-associated microsatellite unstable colorectal cancers. Br J Cancer 134, 1019–1030 (2026). https://doi.org/10.1038/s41416-025-03302-z
キーワード: マイクロサテライト不安定性大腸がん, リンチ症候群, 腫瘍免疫微小環境, 腫瘍関連マクロファージ, がん免疫療法