Clear Sky Science · ja
PRMT6はCCL2発現を増加させることで、異所性骨化におけるマクロファージ誘導性炎症の開始と増幅に必要である
治癒が行き過ぎるとき
重度の外傷や手術の後、体は治そうと過剰に反応し、もともと骨が存在すべきでない場所に新たな骨を作ってしまうことがあります。この痛みを伴う状態は軟部組織内の望まれない骨形成と呼ばれ、関節を固め、切断術を複雑にし、日常動作を困難にします。現在の治療法は限られており、再発を防げないことがしばしばです。本研究は、外傷をこの異常な骨形成につなげる免疫系の早期の重要なスイッチを明らかにし、治療が効果を発揮できる短く重要な窓口を示しています。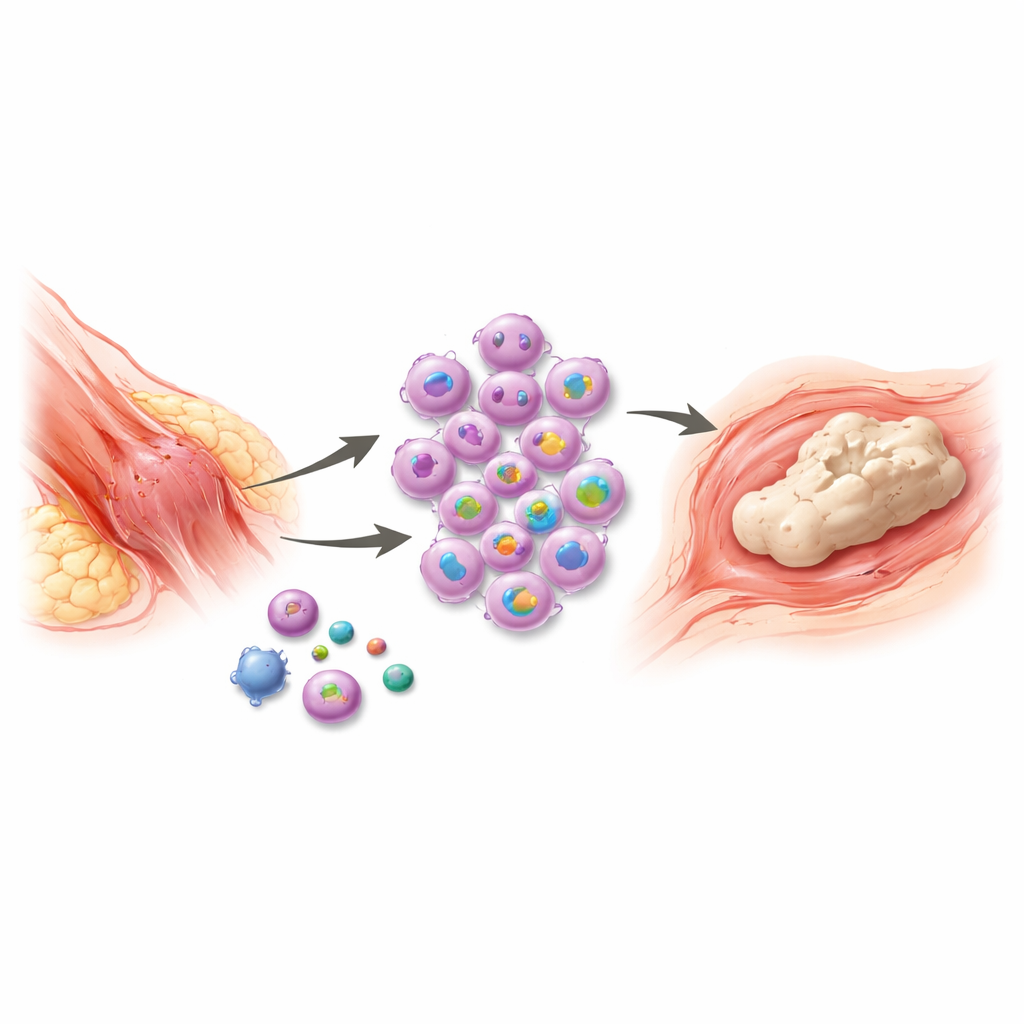
間違った場所にできる骨の問題
火傷、骨折、整形外科手術といった大きな外傷の後、一部の患者では筋肉や腱、他の軟部組織の中に骨の島が生じます。この新しい骨は正常な骨発生に似た過程で形成され、炎症から始まり成熟した石灰化組織で終わります。免疫細胞であるマクロファージがこの反応の中心的役割を担うことは知られているものの、彼らが炎症を点火し持続させる過程の詳細な制御は不明でした。その知識がなければ、抗炎症薬、放射線、遅れた外科的除去といった治療は原因ではなく結果に対処するにとどまり、再発が一般的です。
炎症の鍵を握る仲介者
研究者らは、腱の損傷と熱傷を組み合わせたマウスモデルを用いて(人の重度外傷をよく模倣する)、損傷部位で時間とともに何が起きるかを追跡しました。損傷後最初の数日でマクロファージが急速に蓄積し、その後異常な骨が形成される間も持続するのを観察しました。これらの細胞を枯渇させると、余分な骨はほとんど消え、周囲組織の血管や支持細胞の乱れもはるかに少なくなりました。損傷組織の遺伝子発現を詳しく解析すると、これらのマクロファージで際立っていた分子が一つ見つかりました:PRMT6、タンパク質を修飾しどの遺伝子がオンになるかを制御する酵素です。
炎症のための分子的な音量つまみ
研究チームは、PRMT6のレベルが損傷後および実験室での危険信号や細菌成分への反応でマクロファージ内で急速に上昇することを見出しました。PRMT6を欠くマウス、またはマクロファージだけでPRMT6を選択的に減らしたマウスでは、損傷部位のマクロファージははるかに少なく、異常な骨形成も著しく減少しました。重要なのは、これらの動物の損傷した腱はむしろ良好に治癒し、組織がより整然とし瘢痕形成が少なかったことです。これはPRMT6が健康な修復に必須ではなく、むしろ有害な炎症を増幅する音量つまみとして働くことを示しています。研究者らがPRMT6を阻害する薬を投与すると、効果があったのは損傷後最初の数週間という早期のみでした。治療開始が遅れるとほとんど効果がなく、狭いが強力な治療の時間窓が明らかになりました。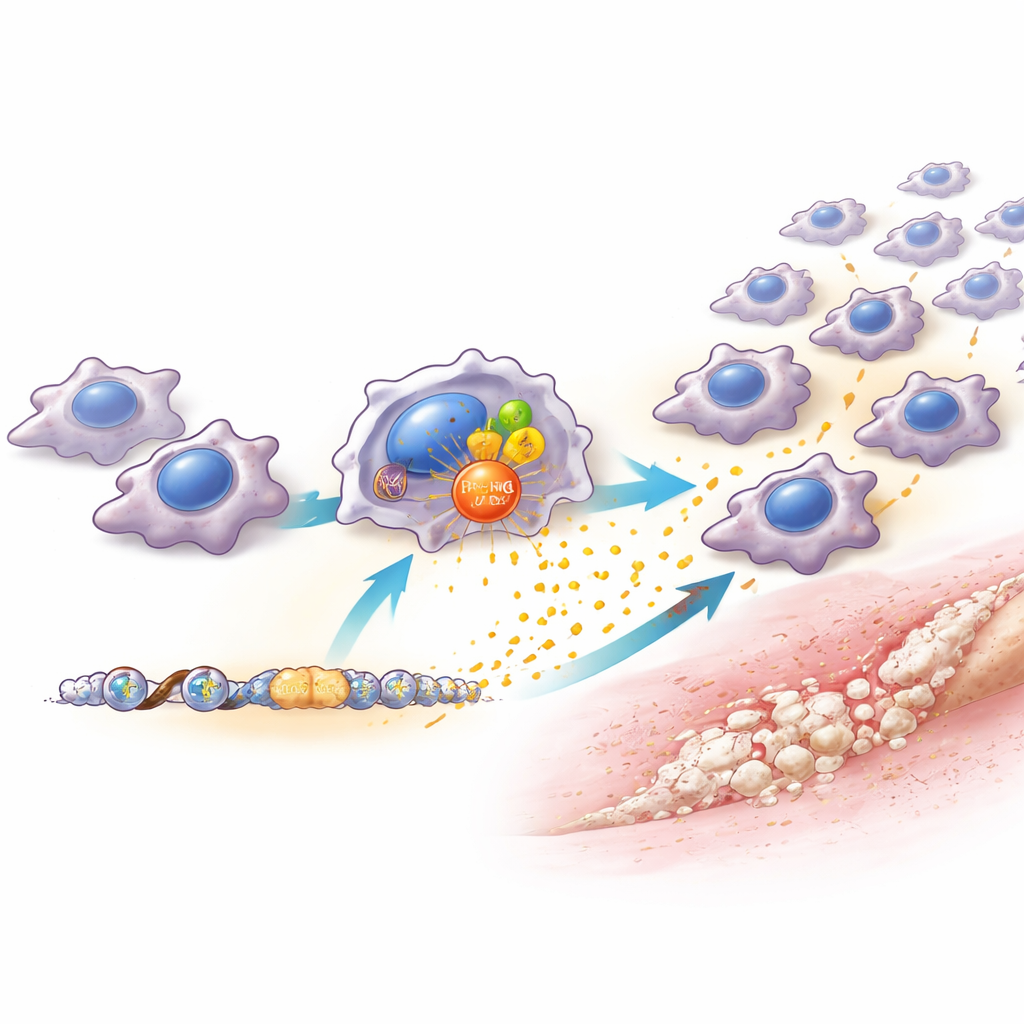
一つのシグナルが多数の免疫細胞を引き寄せる仕組み
PRMT6がどのようにしてこの効果を発揮するかを理解するために、科学者らはマクロファージを詳細に調べました。PRMT6がないと、これらの細胞は複数の化学的走化性因子、特に血中から単球やマクロファージを損傷組織へ引き寄せるCCL2の産生をはるかに少なくしました。PRMT6はCCL2遺伝子を二重の方法でオンにするのを助けます:よく知られた炎症制御因子NF-κBと協調し、近傍のDNAパッケージングタンパク質に化学的な印を付けてその遺伝子を読みやすくするのです。その結果、PRMT6が高いマクロファージはより多くのCCL2を放出し、追加のマクロファージを引き寄せて血管や骨形成前駆細胞を育む「炎症の中心」を築きます。マクロファージで特異的にCCL2を減らすと、結果はPRMT6欠損に非常に近くなり——マクロファージの減少、弱い炎症ニッチ、少ない余分な骨——CCL2を戻すとマクロファージ流入と異常骨形成の一部が回復しました。
望まれない骨を予防するための標的化された機会
総じて、本研究はマクロファージ内のPRMT6が早期のエピジェネティックな増幅因子として機能し、より多くの免疫細胞を呼び寄せる重要な化学シグナルを増大させ、その結果として本来骨ができるべきでない場所での骨形成を促進することを示します。PRMT6を初期の炎症期にだけ阻害すると、正常な腱の治癒は保たれつつ望まれない骨が大幅に減少し、組織の配列も改善されるため、この経路は有望な新しい戦略を提供します。理論的には、重度の外傷や手術後に短期間、適切なタイミングでPRMT6を標的とする治療を行うことで、体の自然な修復能力を損なうことなく異所性骨による長期的障害を防げる可能性があります。
引用: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
キーワード: 異所性骨化, マクロファージ, 炎症, エピジェネティック制御, CCL2シグナル伝達