Clear Sky Science · ja
脊髄損傷の回復を制限するTGF-β誘導性の線維性瘢痕形成
なぜ脊髄の瘢痕が重要なのか
脊髄が重度に損傷すると、多くの人が永続的な麻痺や感覚喪失を抱えることになります。これは、損傷した神経線維が再び伸びないためです。本研究は単純だが重要な問いを立てます:正確には何がその再成長を阻んでいるのか――そしてその障壁を安全に取り除けるのか?損傷した脊髄内で特定の種類の瘢痕がどのように形成されるかを明らかにすることで、著者らは神経系の自己修復を助ける新しい手がかりを提示しています。
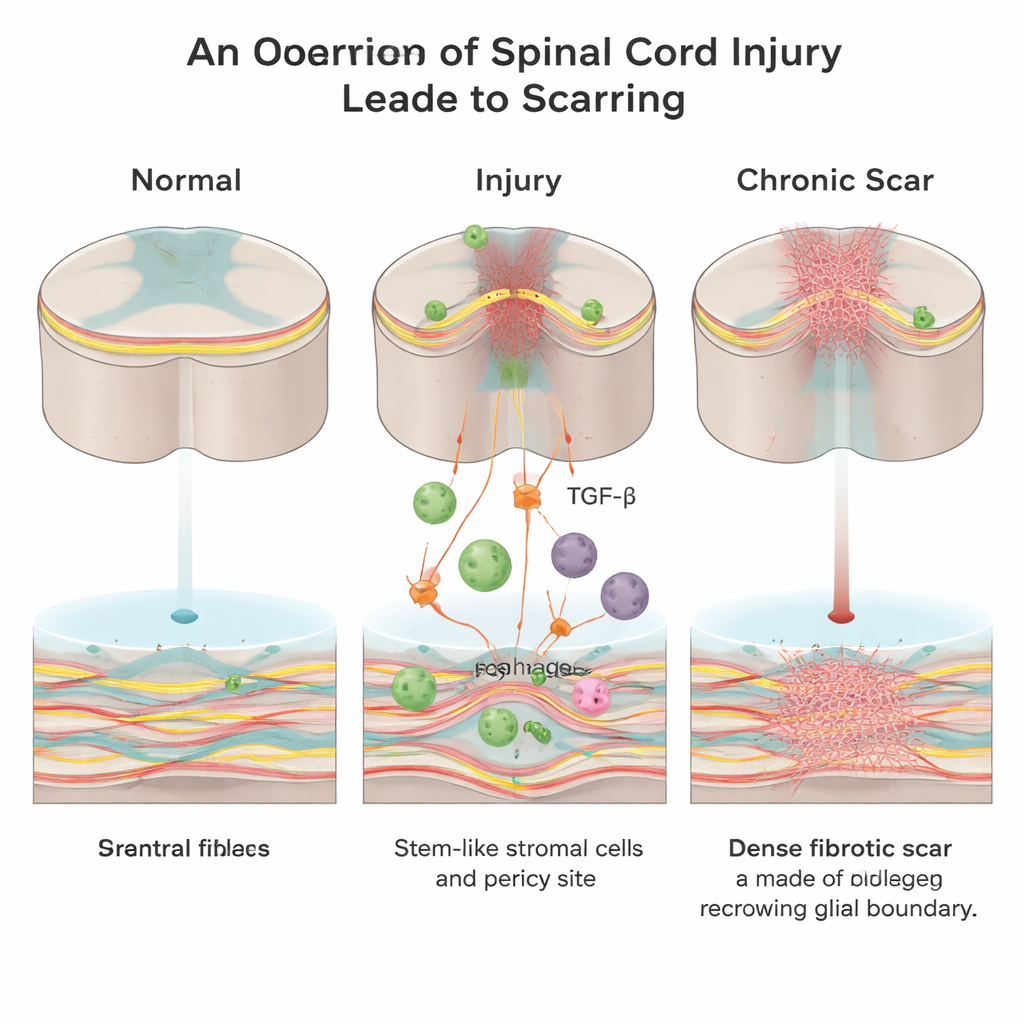
損傷部位内に隠れた壁
脊髄損傷後、体は傷を封鎖するために急いで反応します。主に二種類の瘢痕組織が形成されます:支持細胞であるアストロサイトが作る「グリア」瘢痕と、コラーゲン、フィブロネクチン、線維芽細胞を豊富に含む「線維性」瘢痕です。グリア瘢痕には保護的な役割がある場合もありますが、線維性瘢痕は密な物理的・化学的な壁を作り、伸長する神経線維が容易に越えられなくなります。これまで、線維質コアがどのように現れ、どのシグナルがその形成を駆動するかについてはほとんど知られていませんでした。
免疫細胞と強力なシグナルの役割
成体マウスを用いて研究したところ、研究者たちはトランスフォーミング成長因子ベータ(TGF‑β)というシグナル分子に注目しました。TGF‑βは全身の創傷修復を調整し、線維化疾患で過剰に活性化されることが多い分子です。脊髄損傷後、侵入した免疫細胞であるマクロファージが病変部位で活性型のTGF‑β1の主要な供給源になることが分かりました。このTGF‑β1の急増は局所の間葉系ストローマル/幹細胞や血管関連のペリサイトを呼び寄せ、これらを線維芽細胞へと変化させます。これらの線維芽細胞がコラーゲン豊富な線維性瘢痕を沈着します。
シグナルを抑えて通路を開く
この経路が有害な瘢痕を実際に引き起こしているかを確かめるため、チームはマウスでいくつかの遺伝学的手法を用いました。マクロファージを除去したり、マクロファージ系統の細胞でのみTGF‑β1遺伝子を欠損させると、損傷した脊髄の線維性組織量は大幅に減少し、より多くの神経線維やセロトニン含有経路が損傷領域を越えて伸びられるようになりました。同様に、ペリサイトに特異的にTGF‑β受容体を欠損させると、彼らのTGF‑β応答が低下し、コラーゲンの蓄積が減り、運動および感覚の行動試験で改善が見られました。重要なのは、ペリサイトや関連する幹様細胞は依然として存在していたものの、瘢痕を形成する線維芽細胞になる可能性が低くなっていたことです。
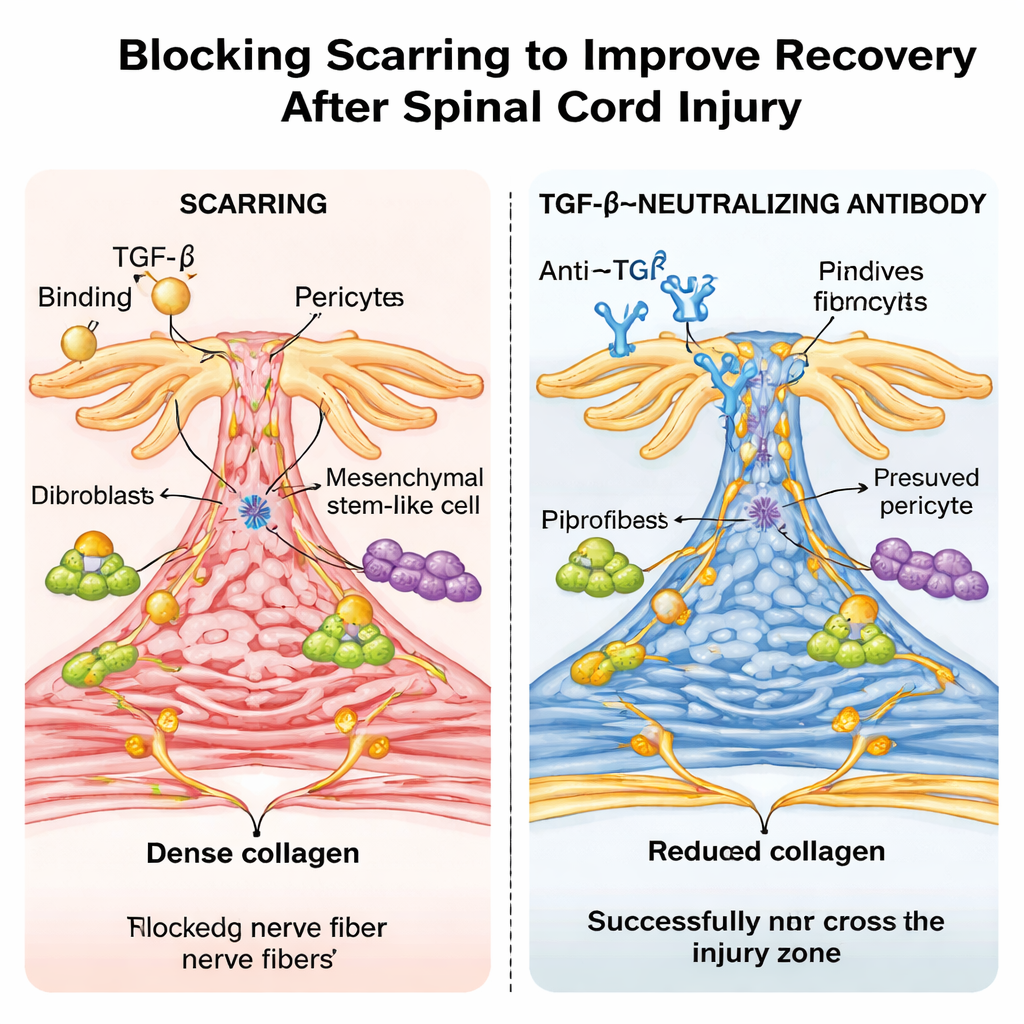
薬剤様の抗体と驚くべき年齢効果
研究者らは次に、臨床的により関連するアプローチを試みました:実験室で作られたTGF‑βを中和する抗体で通常のマウスを治療することです。損傷後の反復投与により、血中と脊髄の活性型TGF‑βレベルが低下し、線維性瘢痕が縮小し、神経線維が病変をより効果的に橋渡しできるようになり、歩行および感覚機能に顕著な改善が見られました。単一細胞RNAシーケンシングは、未治療マウスで瘢痕形成細胞型においてTGF‑β応答遺伝子が高活性であり、抗体により抑制されたことを確認しました。注目すべきは、新生子のマウスで同じタイプの脊髄圧挫を行うと、動物はほとんど線維性瘢痕を伴わずに治癒し、傷害部位で検出可能なTGF‑β活性化を示さず、ほぼ正常な運動を回復したことです――これは一部の非哺乳類で見られる瘢痕のない修復に似ています。
将来の治療にとっての意義
総じて、本研究結果は、脊髄損傷後の過剰なTGF‑β活性化が、修復に役立つ細胞を剛直な線維性の壁を作る方向にそらし、それが神経の再成長と機能回復を阻害していることを示唆します。マクロファージでのTGF‑β産生を標的にする、ペリサイトやストローマル細胞での受容体を遮断する、あるいは中和抗体を使用するなど、過剰な活性化を防ぐことで、有害な瘢痕を減らしつつ、より有益な組織応答を保存または高めることが可能になるかもしれません。これらの戦略をヒトに翻訳するには副作用を避けるための慎重な検討が必要ですが、本研究はTGF‑β駆動の線維化瘢痕を脊髄修復に対する中心的で薬物で狙える可能性のある障壁として浮き彫りにしています。
引用: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
キーワード: 脊髄損傷, 線維性瘢痕, TGF-ベータ, マクロファージ, 神経再生