Clear Sky Science · ja
光合性細菌のキュープレドキシン由来ペプチドによるミトコンドリアエネルギー産生抑制が腫瘍成長を阻害する
細菌をがん治療の味方に変える
がん細胞はエネルギーを大量に消費します。増殖、浸潤、治療抵抗性を支えるために、細胞内の小さな「発電所」であるミトコンドリアに依存しています。本研究は、がんと戦う思いがけない味方――光合性細菌に由来する短いタンパク質断片――を検討します。研究者らは、この設計されたペプチドががん細胞に入り込み、エネルギー供給をその発生源で遮断し、放射線療法の効果を大幅に高めることを示しています。しかも正常細胞への影響は主に限定的でした。
大役を担う小さなペプチド
研究チームは、細菌タンパク質アズリンが腫瘍抑制因子p53に作用して腫瘍成長を遅らせるという以前の発見を出発点としました。次に、人間の腫瘍周辺に生息する細菌、特に光を利用してエネルギーを生成する光合性微生物に注目しました。これらの細菌はキュープレドキシンと呼ばれる関連タンパク質群を持っています。構造と進化的履歴を比較することで、研究者らはオウラサイアニンB(auracyanin B)というキュープレドキシンに着目し、aurBと名づけた28アミノ酸の短い領域を切り出しました。この断片は水溶性で細胞膜を通過でき、細胞内部の主要なエネルギー生成装置と相互作用する可能性を示唆する形状を持っていました。
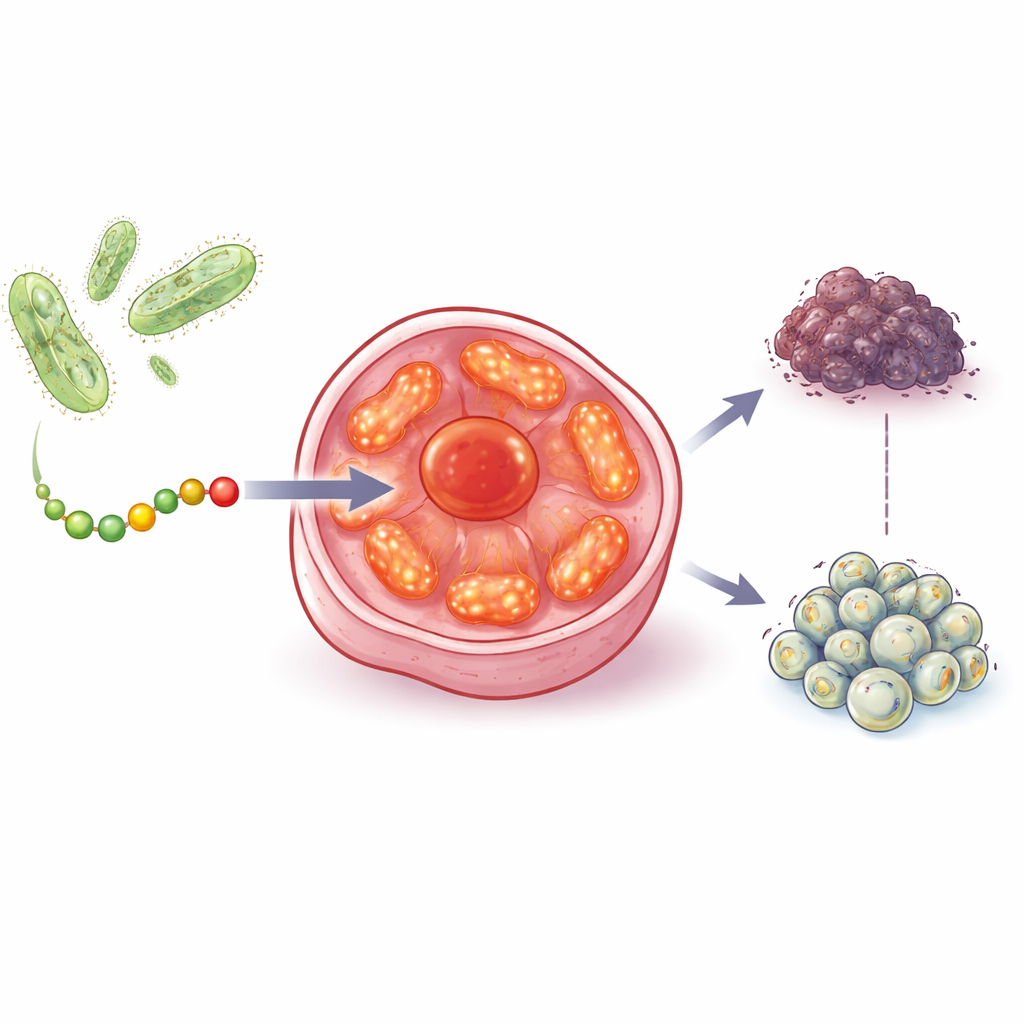
がんの発電所を見つけて攻撃する
in vitro試験で、aurBは乳がん、前立腺がん、大腸がん、卵巣がんの細胞株の生存率を低下させました。これらの細胞の中にはp53が機能していないものや、多くの既存薬が依存するホルモン受容体を欠くものも含まれていました。重要な点として、aurBはミトコンドリアが豊富な正常な前立腺、心臓、筋肉細胞に対してははるかに弱い影響しか示しませんでした。イメージング実験は、aurBががん細胞に選択的に取り込まれ、その後ミトコンドリア内に濃縮されることを示しました。オーガニックな可視化ハンドルとして小さな金棒に結合させたaurBを用いた電子顕微鏡観察は、実際にこのペプチドがこれらの細胞小器官内に蓄積することを裏付けました。
エネルギー供給を断つ
ミトコンドリア内に入ると、aurBはATP合成酵素の特定の構成要素に結合しました。ATP合成酵素はATPという細胞の主要なエネルギー通貨を作る分子タービンです。生化学的なプルダウン実験と質量分析により、この相互作用相手は酵素の中心コアの一部であるATP5Cであることが同定されました。表面プラズモン共鳴による測定は、aurBがATP5Cに対して中程度の強さで結合し、解離が遅いことを示し、安定した相互作用と整合しました。機能的アッセイはこの結合の影響を明らかにしました:aurBは前立腺がん細胞のミトコンドリアATPレベルを急激に低下させ、酸素消費率を遅らせ、呼吸と代替の解糖系の両方を阻害しました。エネルギー産生が崩壊すると、がん細胞は主要な実行酵素であるカスパーゼ3によるプログラム細胞死の特徴を示しました。
腫瘍を阻止し放射線効果を高める
研究者らは次に、攻撃的な前立腺がんのマウスモデルでaurBを試験しました。皮下に移植したヒト前立腺腫瘍を持つ動物に定期的にaurBを投与すると、腫瘍成長は約3分の2縮小し、化学療法薬パクリタキセルと同等かそれ以上の効果を示しましたが、体重減少や明らかな苦痛は観察されませんでした。治療を受けたマウスの腫瘍標本には、分裂細胞が減少し、死滅細胞が増加していました。前立腺がんの転移先として一般的かつ致命的な骨転移を模した第二のモデルでは、aurB単独でも脚の骨内での腫瘍拡大を遅らせ、肺転移の数を減少させました。しかし、適度な線量の放射線と組み合わせると効果は劇的でした:治療した脚の腫瘍はほとんど消失し、肺転移は対照群に比べて90%以上減少しました。
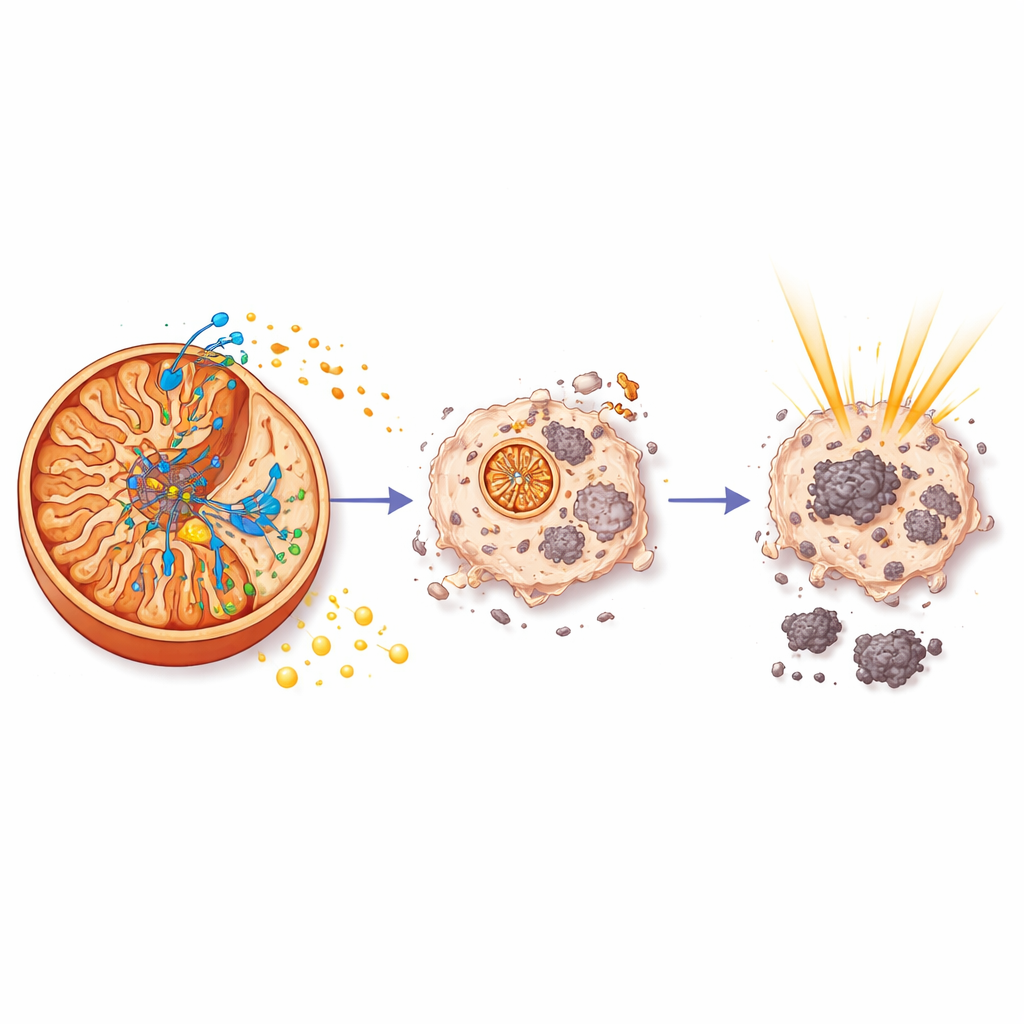
なぜエネルギーが放射線に重要なのか
aurBが放射線効果を高める理由を理解するために、チームは治療を受けたマウスの腫瘍における遺伝子発現を調べました。aurBは放射線単独では抑えられなかったHIF-1に制御される遺伝子ネットワークを低下させることが分かりました。HIF-1は低酸素環境に適応し治療抵抗性を助ける主要な制御因子です。aurBによって作られたエネルギー不足の条件下で、PI3Kやc-Mycが駆動する重要な成長・生存経路は抑制され、腫瘍が過酷な環境で生き残るための解糖系装置も低下しました。本質的に、ミトコンドリアのタービンであるATP産生を直接破壊することで、aurBはがん細胞をエネルギー危機に追い込み、放射線ダメージに対してはるかに脆弱な状態にしました。
新しい精密エネルギー遮断剤の一群
本研究は、腫瘍で変化したミトコンドリアのエネルギーシステムに向かう小さな細菌由来ペプチドを設計するという新たながん治療戦略を提示します。光合性細菌タンパク質に由来するaurBは、前立腺、乳房、卵巣、脳腫瘍などでしばしば過活動となるATP合成酵素の構成要素を選択的に標的とします。エネルギーを直接枯渇させ防御を弱めることで、特に放射線治療に対して既存治療を補完し、免疫療法が効果を出しにくい場合の選択肢を提供する可能性があります。この概念が臨床に到達するまでには多くの作業が残されていますが、古代の細菌のエネルギータンパク質を現代の高精度ながん治療ツールへと再利用できることを示す研究です。
引用: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
キーワード: ミトコンドリアATP合成酵素, 癌代謝, 治療用ペプチド, 前立腺がん, 放射線感受性化