Clear Sky Science · ja
消化管がんにおけるClaudin18.2特異的IL-7/XCL1搭載CAR-T細胞の有効性と免疫修飾効果:前臨床および臨床解析
免疫系を活用して消化器がんに立ち向かう
胃がんや膵がんは手術、化学療法、放射線療法に抵抗することが多く、死亡率の高い腫瘍の一つです。本研究は、体内の免疫細胞を強化して固形腫瘍に浸透させ、そこで生存させ、増援を呼び込めるようにする新たなアプローチを検討します。がんを攻撃するT細胞を再設計して有益な免疫シグナルを放出させることで、腫瘍を直接攻撃するだけでなく、がんの“敵対的”な局所環境の中で他の免疫構成要素を目覚めさせることを目指しています。
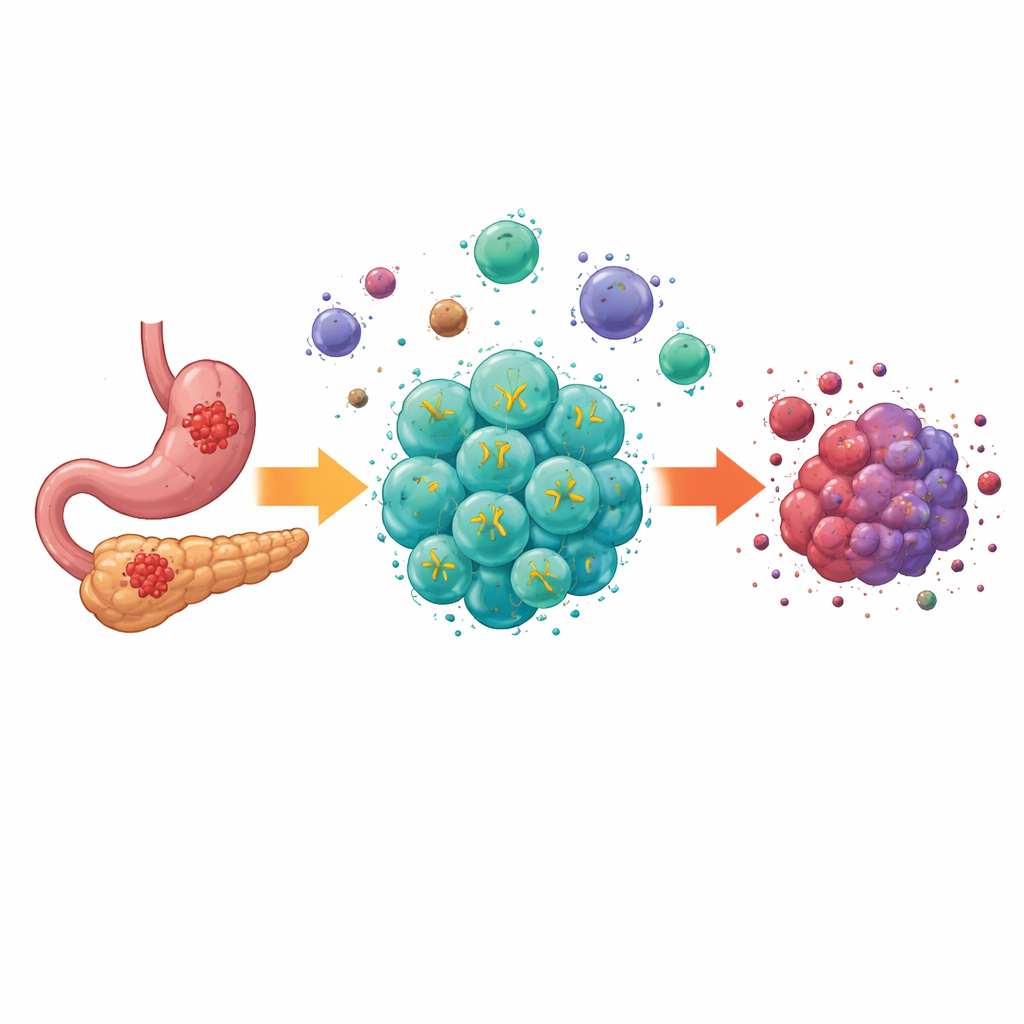
固形腫瘍が治療しにくい理由
現代の細胞療法であるCAR-T細胞は、血液がんで劇的な成果を上げ、他に選択肢のなかった患者を治癒する例もありました。しかし消化管に発生するような固形腫瘍は、さらなる障壁を抱えています。腫瘍内の細胞は場所ごとに異なり、内部は栄養や酸素が乏しく、抑制的な細胞やシグナル分子の混合が免疫攻撃を鈍らせます。これまでの世代のCAR-Tは消化管がん細胞上の標的分子を認識できても、この過酷な環境内で十分に増殖・持続・機能することが難しく、臨床効果が限定されていました。
賢い設計の改良型T細胞
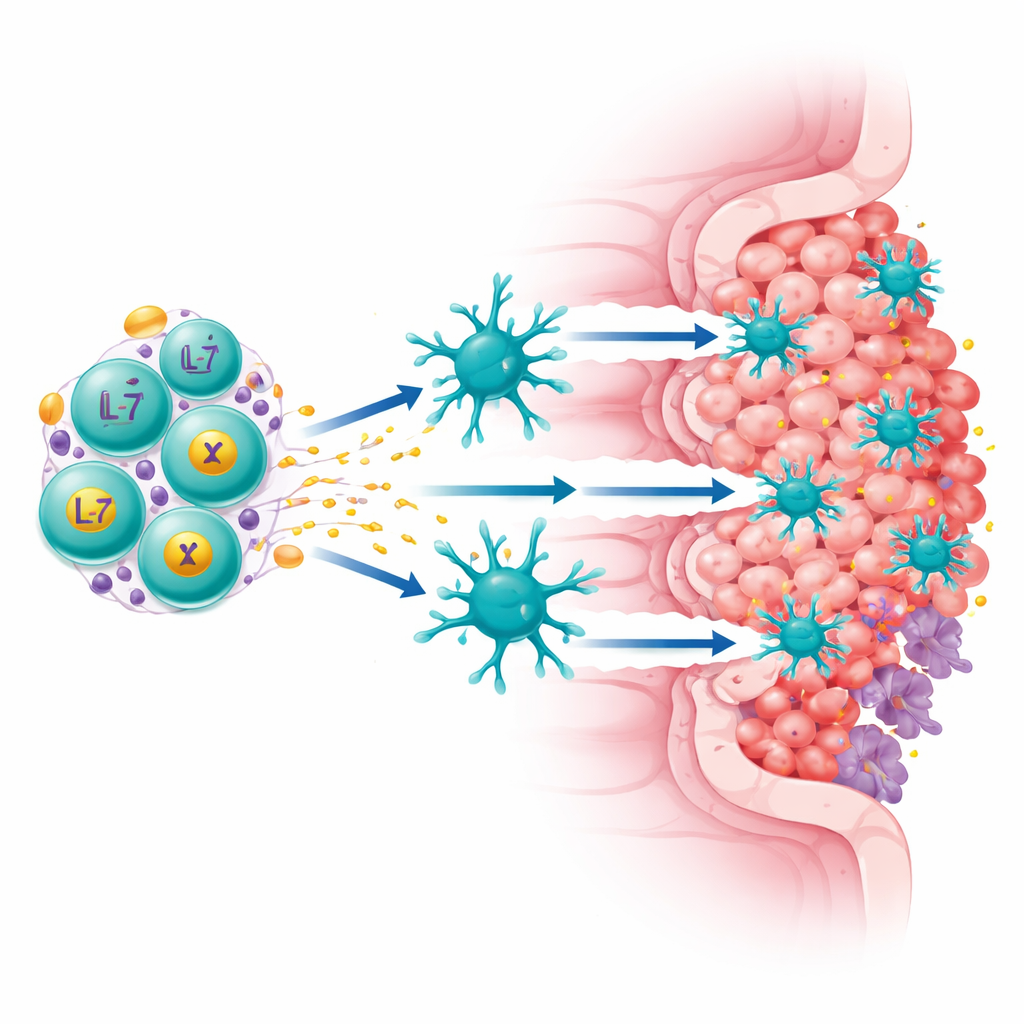
研究チームはClaudin18.2というタンパク質に着目しました。これは多くの胃がんや膵がん細胞で高発現する一方、正常組織にはほとんど存在しません。彼らは“第四世代”のCAR-T細胞を構築し、二つの役割を同時に果たすようにしました:腫瘍細胞上のClaudin18.2を認識するとともに、IL-7とXCL1という二つの免疫増強因子を継続的に分泌します。IL-7はT細胞の生存と長寿命の幹様状態の維持に寄与し、XCL1はcDC1と呼ばれる稀少だが強力な樹状細胞を誘引するシグナルとして働き、キラーT細胞の活性化を助けます。この改良型細胞(ExCAR-TまたはRD07と命名)は、見かけ上の標的を破壊するだけでなく、腫瘍の免疫環境そのものを再構築するよう設計されています。
前臨床モデルでの強力な腫瘍制御
消化器がんのマウスモデルにおいて、ExCAR-T細胞はIL-7とXCL1を欠く従来型CAR-Tを上回る成果を示しました。in vitroでは、改変細胞はより多くのがん細胞を殺し、長期持続する記憶様T細胞をより多く含んでいました。Claudin18.2陽性腫瘍を有する動物では、ExCAR-T投与により腫瘍縮小がより深く、標準的なCAR-Tに比べ生存期間が延長しました。改良型は血中でよりよく拡大し、追加の免疫細胞を呼び込むシグナルを誘導する一方で腫瘍転移に結びつく因子を低下させるなど、より広範な免疫応答を引き起こしました。注目すべきは、ExCAR-Tで治癒したマウスがClaudin18.2標的を失ったがん細胞による再挑戦を拒絶した点であり、これは治療が狭い単一標的応答ではなく、持続的で全腫瘍に及ぶ免疫記憶を誘発したことを示唆します。
患者における早期臨床試験の結果
これらのデータを受けて、研究者らは進行した胃がん、胃食道接合部がん、膵がんの既治療患者12名を対象にRD07の第一相ヒト試験を開始しました。副作用は概ね管理可能で、重篤な問題の多くは投与前化学療法による血球減少であり、サイトカイン放出症候群は軽度にとどまり、脳に関連する重篤な毒性は認められませんでした。評価可能な10例のうち7例で腫瘍縮小が確認され、2例が部分奏効を達成しました。腫瘍でのClaudin18.2発現が中等度〜高い患者は特に良好な反応を示し、そうした患者は少なくとも病勢安定を経験し、一部は期待より長く生存しました。これらの奏効者では、改変T細胞の血中での拡大がより顕著であり、血中IL-7およびXCL1の上昇も観察され、治療設計と一致しました。
腫瘍の免疫的近隣を可視化する
ヒトにおけるRD07の作用を理解するため、チームは治療前後の腫瘍サンプルを単一細胞分解能で解析しました。奏効例ではClaudin18.2陽性がん細胞の割合が低下し、治療が標的を的確に攻撃していることが確認されました。同時に、多様なT細胞クローンの増加が見られ、活性化したキラー細胞や組織常在性の記憶T細胞が増えており、体内でより広範な免疫応答が誘導されていることを示唆します。専門化した樹状細胞は活性化の兆候を示し、増殖中のT細胞との相互作用が強化されており、これはXCL1によってこれらの細胞が腫瘍へ引き寄せられたことと整合します。ある患者の腫瘍スライスのイメージングでは、治療後に腫瘍細胞や抑制的な骨髄由来細胞が減少し、T細胞やB細胞が増加し、組織が免疫細胞に富むゾーンへと再編成される様子が確認されました。これらは“ホット”で炎症が強い微小環境への変化の指標です。
将来のがん治療にとっての意義
前臨床および早期臨床の所見を総合すると、RD07は単に別の標的薬を追加する以上の効果を持つ可能性があります。腫瘍認識と内蔵の免疫支援を組み合わせることで、これらの改変T細胞はより長く生存し、重要な協働細胞を呼び寄せ、患者自身の免疫系を訓練して元の標的が失われてもがんを抑え続けるのを助けます。試験は小規模で既に多くの治療を受けた患者で行われましたが、安定した腫瘍縮小、容認できる安全性、深い免疫再編成が示された点は有望です。より大規模な研究で確認されれば、このアプローチは消化管がん治療において新たな章を開く可能性があり、腫瘍内の免疫エコシステムを強化することが、がん細胞への最初の攻撃と同じくらい重要であることを示すでしょう。
引用: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
キーワード: CAR-T細胞療法, 消化管がん, 腫瘍微小環境, Claudin18.2, 免疫療法