Clear Sky Science · ja
Visinin様タンパク質1はカルシウム恒常性を乱し、ヒトおよび齧歯類モデルで心房細動を促進する
この心拍リズムの話が重要な理由
心房細動は脳卒中や心不全のリスクを高める一般的な不整脈です。多くの人がこれを抱えて暮らしており、一方で医師は予防や治療後の再発防止に依然として苦労しています。本研究は心筋細胞に存在するこれまで見落とされてきたタンパク質、VILIP-1(Visinin-like protein 1)を明らかにしました。これは故障したカルシウムスイッチのように振る舞い、ヒトと動物の双方で心房細動を引き起こす要因となります。このスイッチを特定し、既存薬がその働きを抑えられることを示したことで、より安全で標的を絞った治療への新たな道を開きます。
乱れた心拍を詳しく見る
健康な心臓では、上室である心房内に電気的な波が秩序正しく伝わり、各拍動を導きます。その秩序は主にカルシウムに依存しており、カルシウムが心筋細胞内外を出入りすることで収縮と弛緩を調整します。心房細動ではこのカルシウムの流れが乱れ、余分な漏れや変動が生じて、孤立した電気信号が発生し、速く不規則なリズムへと発展します。カルシウムの取り扱い不良がこの障害の中心であることは長年知られていましたが、混乱を引き起こす上流のきっかけは不明瞭でした。
隠れた問題児の発見
研究者らは、乱れたカルシウム処理を心房細動に結びつける分子を探すために、複数の先端的アプローチを組み合わせました。ペーシングで心房細動を誘導したラットの数百個の個別心房細胞からカルシウム信号を記録し、同じ細胞で発現している遺伝子の全セットをシーケンスしました。さらに、心房細動患者の心房組織と正常リズムの患者の組織の遺伝子発現も比較しました。これらのデータセットを重ね合わせ、細胞が健康な状態から病的状態へ変化する経路を追跡したところ、繰り返し際立った遺伝子が見つかりました。それがVsnl1で、VILIP-1を産生するこの遺伝子は、これまで主に脳や膵臓で研究されており、心臓での役割はほとんど注目されていませんでした。
VILIP-1がカルシウムバランスを乱す仕組み
患者と動物モデル双方の心房組織で、VILIP-1の量は有意に高く、タンパク質は細胞表面に濃縮していました。この変化が単なる随伴現象か原因かを調べるため、研究チームはマウスの心房心筋細胞にVILIP-1を過剰発現させました。これらのマウスで心臓の明らかな構造的損傷は見られませんでしたが、電気的ペーシングにより心房細動を誘発しやすくなりました。詳細な電気記録では、遅延後脱分極(各拍後に生じる異常な電位変動)や拍ごとの活動電位形状の交互変化が増加し、カルシウム過負荷に関連する不安定な電気的挙動の典型的な兆候が示されました。高解像度のカルシウムイメージングは、頻繁な自発的カルシウム波と細胞内カルシウム貯蔵の枯渇を確認し、細胞内部での深刻な漏れを示しました。
細胞表面での重要な相棒
VILIP-1がどのようにこの攪乱を引き起こすかを理解するため、研究者らは心筋細胞内でVILIP-1と相互作用するタンパク質をマッピングしました。心房組織から結合パートナーを引き出す方法と、生細胞で周辺タンパク質を「ビオチンハロー」で標識する二つの補完的手法を用い、標的を絞ったところ、心膜の主要なナトリウム–カルシウム交換体であるNCX-1が浮かび上がりました。この交換体は通常ナトリウムと引き換えにカルシウムを排出する役割を担いますが、条件によっては逆方向に働いてカルシウムを細胞内に押し込むことがあります。本研究はVILIP-1がNCX-1に物理的に結合し、総産生量を増やすことなく膜に埋め込まれるNCX-1の数を増やすことを示しました。その結果、交換体電流が増大し、選択的阻害薬でNCX-1を遮断するとカルシウム波が減少し、VILIP-1過剰のマウスで心房細動を誘発しにくくなりました。
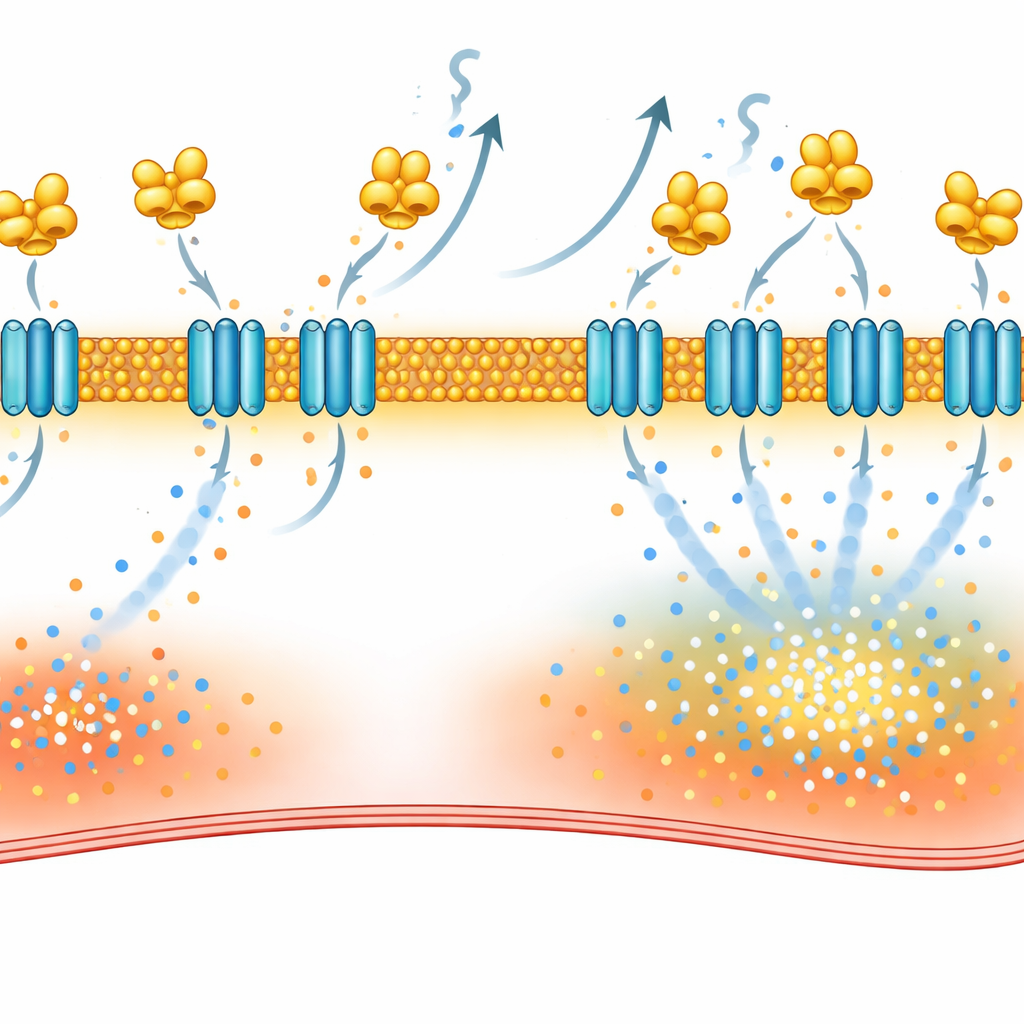
既存薬で故障したスイッチを切る
VILIP-1はミリストイルという脂肪性のタグを介して膜にアンカーされ、カルシウム結合時にそのタグが露出します。研究チームはこのタグ付け過程を妨げることで知られるデスロラタジンを使用し、細胞表面のNCX-1が減少し、交換体電流が正常化され、カルシウム波が減り、ラットモデルでの心房細動エピソードが減少することを見出しました。また、関連するカルシウムセンサーに結合することで知られる糖尿病薬レパグリニドも試験しました。生物物理学的アッセイでレパグリニドがVILIP-1に直接結合することを確認し、ペーシングされたラットおよび心房細動患者の心房組織におけるレパグリニド処理は、膜上のNCX-1を減らし、個々の細胞でのカルシウム漏れを抑え、心房細動の誘発しやすさを大幅に低下させました。
不整脈を持つ人々にとっての意味
まとめると、本研究は自己増幅ループを描き出します。上昇したカルシウムがVILIP-1を細胞表面に誘引し、VILIP-1はNCX-1を増やしてさらにカルシウム過負荷を促進し、結果として心房細動の土壌を作ります。このループをVILIP-1のレベルで遮断すれば、脂肪アンカーを阻害するかカルシウムセンサー部位に結合することで、既存薬がより安定したカルシウムバランスを回復させ、不整脈の脆弱性を低下させ得ます。薬剤特異性の精緻化やより大きな動物モデルおよび臨床試験での検証が必要ですが、VILIP-1はこの広く、しばしばしつこい心拍リズム障害の予防と治療に向けた有望な新たな手がかりとして浮上しました。
引用: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
キーワード: 心房細動, カルシウムシグナル伝達, 心不整脈, ナトリウム・カルシウム交換体, 治療標的