Clear Sky Science · ja
化学療法と光熱併用がフェロトーシスを介して抗腫瘍免疫を喚起する
体の熱と光をがん治療に変える
化学療法薬は腫瘍を縮小させ得ますが、重い副作用を伴うことが多く、再発を確実に防げるわけではありません。本研究は既存薬ドセタキセルを、熱応答性の微小粒子に封入して近赤外光で駆動することで、より強力かつ賢く働かせる新しい手法を探ります。目的は腫瘍細胞をより正確に死滅させるだけでなく、免疫系を呼び覚まして全身のがん細胞を認識・駆逐し、将来の再発を阻止することにあります。 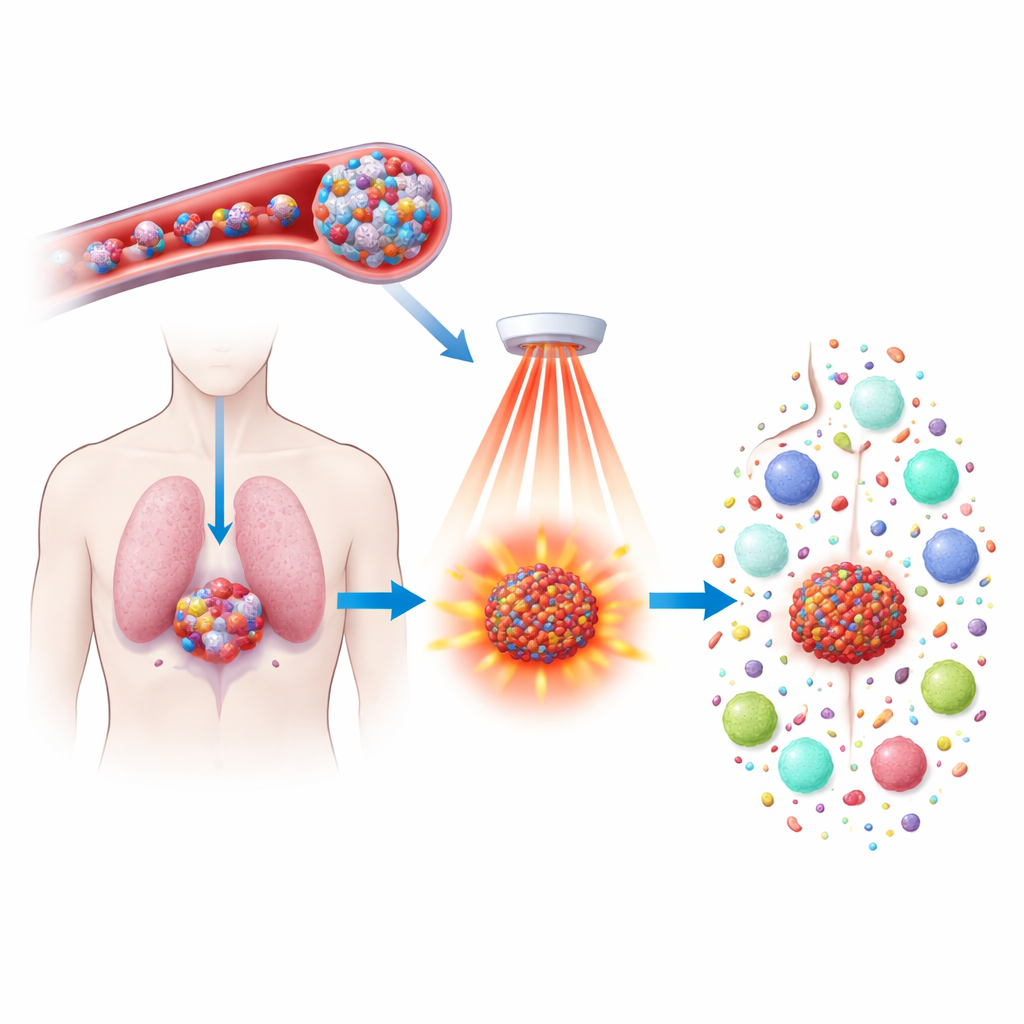
的確に目的地へ届く小さな運び手
研究者らは、フェロセンを含むポリマーからなる新しいタイプのナノ粒子を作製しました。フェロセンは鉄を含む分子で、腫瘍内で通常より高濃度に存在する過酸化水素と強く反応します。これらのポリマーは自己集合して水中に安定な球状を作り、ドセタキセルと光を吸収する色素IR808の両方を搭載できます。静脈注入後、粒子は小さく安定で血流中を巡り、血管がもろく透過性の高い腫瘍部位に漏出します。腫瘍の漏れやすい血管と高い過酸化水素濃度が粒子を徐々に弱め、内包物を放出させることで、治療が腫瘍に集中し健康な臓器へのダメージが抑えられます。
光で局所的なダメージを強化する
組織を比較的安全に貫通できる近赤外光を腫瘍部位に照射します。ナノ粒子内のIR808はこの光を吸収して熱に変換すると同時に、反応性酸素種を生成します。腫瘍が産生する過酸化水素と光で生じる酸化剤の組み合わせにより、粒子はより速く崩壊して薬剤を必要な場所で放出します。同時に、フェロセンの鉄はこれらの酸化剤を脂質を攻撃するより強力な種へと変換するのに寄与します。この化学的・熱的なピンポイント攻撃により、単独のドセタキセル治療や光治療よりも殺傷力が大幅に高まります。 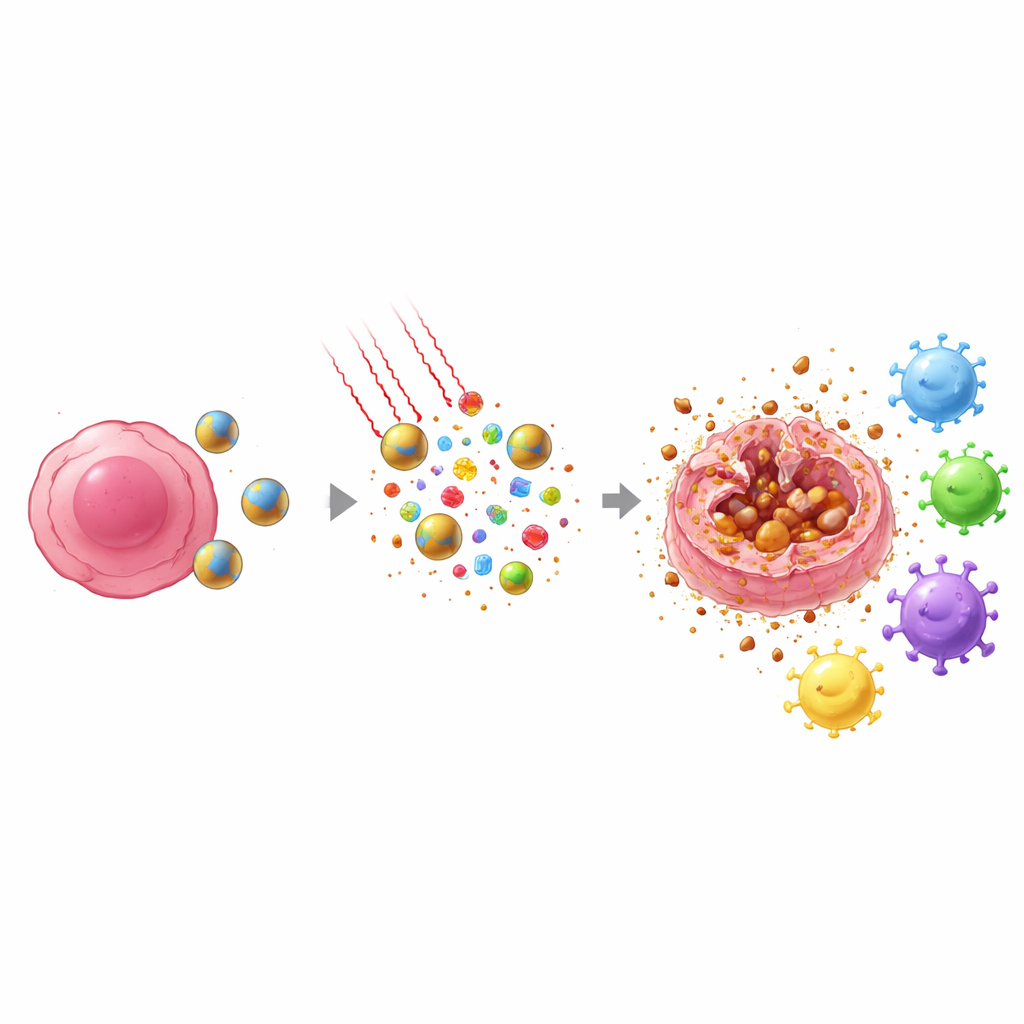
免疫系に信号を送る制御された燃焼
重要なのは、この治療での腫瘍細胞の死に方が通常の化学療法とは異なる点です。細胞が静かに分解して小片になるのではなく、多くはフェロトーシスと呼ばれる過程を経ます。フェロトーシスは鉄依存的で脂質を損傷する死で、細胞膜が破裂します。その際、細胞内の警報シグナルや腫瘍特異的な断片が周囲に放出されます。同時にドセタキセルは核タンパク質HMGB1を細胞辺縁へ押し出し、放出に備えます。熱、酸化剤、薬剤作用が合わさることで危険信号と抗原シグナルの放出が起こり、近傍の免疫監視細胞である樹状細胞がこれを検出してリンパ節へ持ち運びます。
局所攻撃から全身防御へ
マウス腫瘍モデルでは、この化学療法と光熱療法の併用は、照射した腫瘍を単独成分よりも効果的に縮小するだけでなく、免疫環境を変化させました。腫瘍内および排液リンパ節にはより成熟した樹状細胞と増加したキラーT細胞が観察されました。免疫が整った一部のマウスでは、2回の治療サイクル後に原発腫瘍が消失しました。後に別部位や反対側体側に新たに腫瘍を移植すると、これらの二次腫瘍の成長は遅延または抑制され、動物ががん特異的な免疫記憶を獲得したことを示しました。T細胞の疲弊を防ぐチェックポイント阻害抗体を併用すると肺転移がさらに減少し生存が延長され、局所治療が現代の免疫療法と組み合わせ得ることが示唆されます。
今後のがん医療にとっての意義
非専門家に向けた要点は、この手法がドセタキセルを全身毒から賢い多段階の抗がん戦略の一部へと変えることです。薬剤を光で活性化され、腫瘍自身の化学環境に応答する鉄含有ナノ粒子に封入することで、腫瘍内でのダメージを増やしつつ健常組織を温存します。引き起こされる細胞死の特異的パターンは腫瘍内からの“ワクチン”のように働き、免疫系にがんを認識させ記憶させます。これらの知見がヒトにも当てはまれば、このような化学療法–光熱併用システムは耐性のある“コールド”腫瘍を免疫療法に良く反応する“ホット”腫瘍へと変え、再発を減らし長期的な制御を改善する可能性があります。
引用: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
キーワード: がんナノメディシン, 光熱療法, フェロトーシス, がん免疫療法, ドセタキセル送達