Clear Sky Science · ja
導電性配位ナノザイム前駆体が発現するピロトーシス、クプロトーシス、フェロトーシスを正確に誘導しin situ癌ワクチンを実現
腫瘍を自らのワクチンに変える
がん治療は通常、腫瘍細胞を直接死滅させることを目的としますが、腫瘍自身をそれに対するワクチンに変えられるとしたらどうでしょうか。本研究は、体内を安全に移動し、腫瘍内部でのみスイッチが入るスマートなナノ粒子「前駆体」を記述します。これによりがん細胞は免疫系を強力に活性化する死に方を取らされ、一次腫瘍の縮小にとどまらず、遠隔の腫瘍や転移巣をも追跡・排除するように体を教育します。
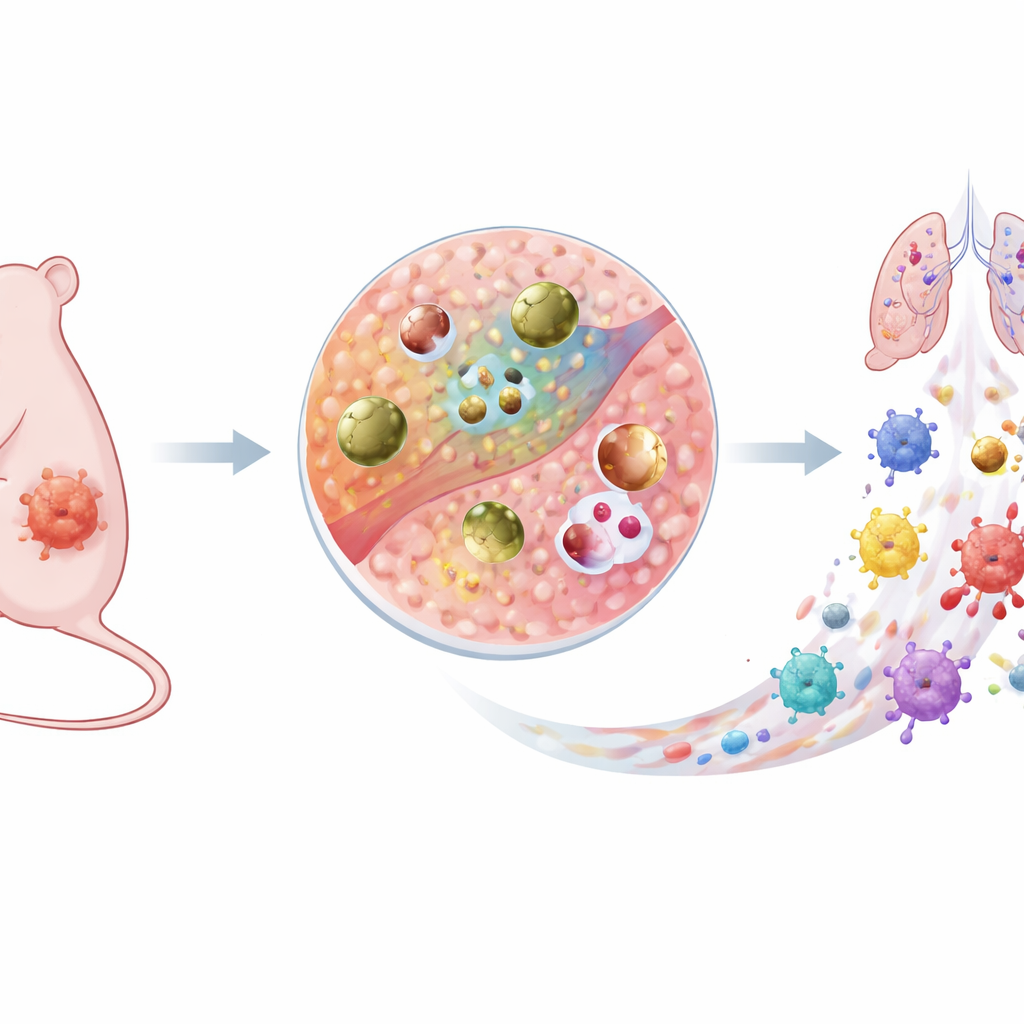
新しいタイプのスマートながん兵器
研究者らはCu–DHNと呼ばれる微小な銅ベース粒子を作製しました。これは循環中は休眠薬のように振る舞い、腫瘍に到達すると攻撃的ながん治療剤に変わります。銅イオン、無害な前駆体分子(1,5-ジヒドロキシナフタレン、DHN)およびアミノ酸システインから組み立てられ、導電性を持つ配位ネットワークを形成します。つまり、電子が粒子内部を容易に移動でき、この内部の“電子ハイウェイ”により粒子全体が化学反応に関与できます。重要なのは、Cu–DHNが腫瘍微小環境に特有の化学状態、すなわち抗酸化物質グルタチオンと過酸化水素が異常に高い環境にのみ応答するよう設計されている点です。
腫瘍の化学がスイッチを入れる仕組み
腫瘍内でCu–DHNは人工酵素のように働きます。グルタチオンと過酸化水素が同時に存在すると、まずグルタチオンを利用して銅イオンを高度に反応性のある状態にリセットし、次に過酸化水素を用いて持続的な高活性酸化剤(ヒドロキシラジカル)の発生を誘導します。これらの酸化剤は二重の役割を果たします。細胞成分を損傷するとともに、粒子内部に閉じ込められた無害なDHNを強力な抗がん化合物であるジャグローンに変換します。ジャグローンはさらに腫瘍の抗酸化防御を抑制し、過酸化水素濃度を増強して酸化ストレスの自己増幅ループを作り出します。このサイクルを始動するための化学的入力を持つのは腫瘍だけなので、その作用は腫瘍内に限定されます。
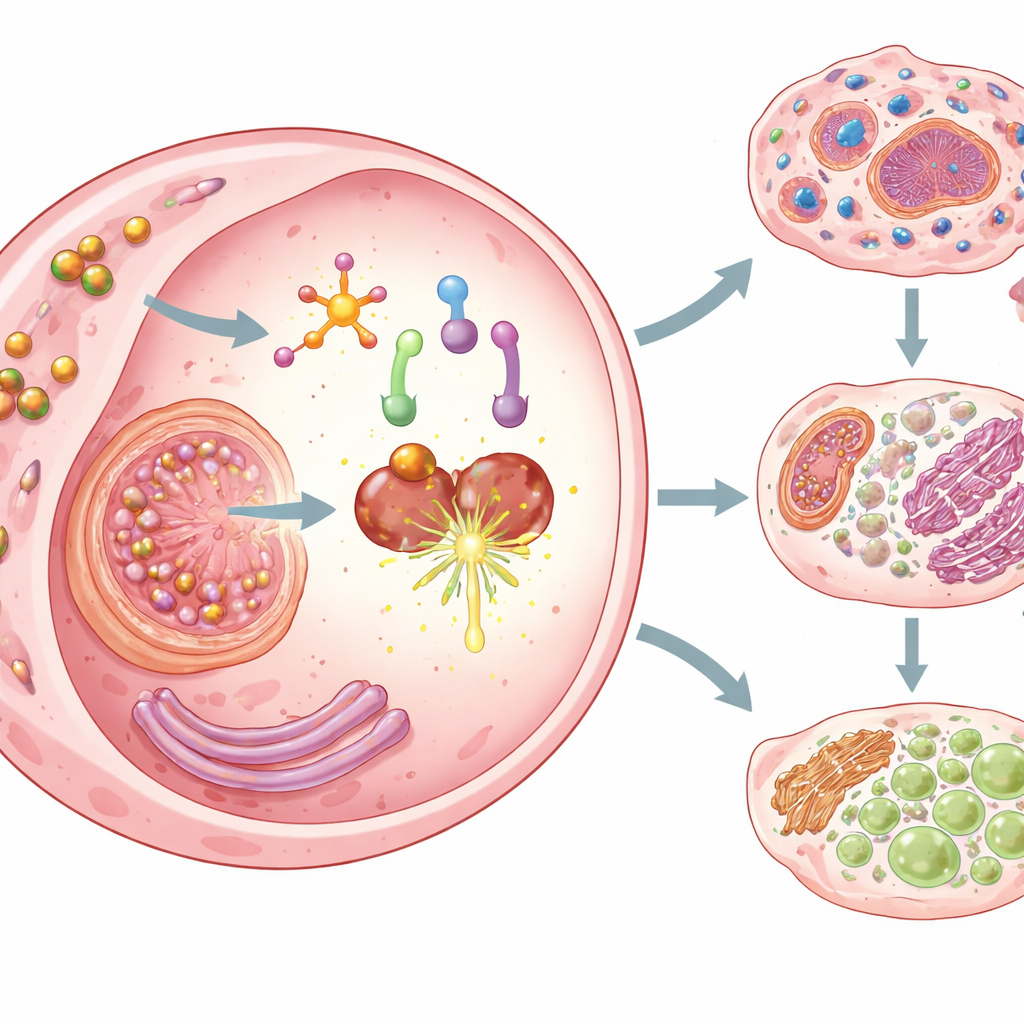
三種類の細胞死を同時に誘導する
活性化されると、Cu–DHNは単にがん細胞を毒殺するだけでなく、免疫系に特に目立つ三種類の制御された細胞死を誘導します。まず、ジャグローンは膜孔形成タンパク質であるガスデルミンDのエピジェネティックなサイレンシングを逆転させ、炎症を感知する複合体を活性化するため、細胞はピロトーシス—膜が破れて内部物質を放出する劇的な炎症性の死—に陥ります。次に、ナノ粒子に搭載された銅はがん細胞に効率よく取り込まれ、主要な代謝装置における銅の有害蓄積に関連するクプロトーシスを促します。第三に、グルタチオンの枯渇と保護酵素(GPX4)の機能阻害により、脂質過酸化に駆動されるフェロトーシスが促進されます。これらが組み合わさることで、がん細胞は効率的に死滅するだけでなく、免疫原性の高い形で死ぬことが保証されます。
局所攻撃から全身防御へ
ピロトーシスとそれに伴う酸化的損傷により、腫瘍細胞は多数の警報信号を放出します:腫瘍関連抗原、ATPやHMGB1のような危険分子、そして表面上のストレスマーカーです。攻撃性の高い乳がんマウスモデルでは、一次腫瘍へ単回注入されたCu–DHNにより近傍リンパ節の樹状細胞が強く活性化され、腫瘍を狙うCD8陽性T細胞が急増しました。これらの免疫細胞は未処理の反対側の腫瘍や肺にまで移動し、新たな腫瘍や転移結節の成長を遅らせ、ほぼ阻止しました。CD8陽性T細胞を遮断するとこの保護効果は大きく失われ、Cu–DHNが一次腫瘍をin situワクチンに変え、免疫系に他所のがんを認識・排除させることが確認されました。
高い効果とより安全なプロファイル
ピロトーシスベースの治療で懸念される重要な点は、同じ膜孔形成タンパク質を有する正常組織が害を受けるリスクです。活性型のジャグローンを直接投与すると、マウスでは肝臓、腎臓、血液に重大な毒性が生じます。対照的に、Cu–DHNは活性化に必要な化学トリガーの組合せが健常組織には存在しないため健康組織では不活性のままです。マウスでは、Cu–DHNは活性ジャグローンと同等の腫瘍殺傷および抗転移効果を示しつつ、臓器障害、血液の異常、体重減少を回避しました。簡潔に言えば、本研究は導電性を備えたスマートなナノ粒子が体内で静かにしておき、腫瘍内でのみ目覚め、がん細胞を免疫を刺激する形で死に至らしめることで、正確かつ自己完結型のがんワクチンプラットフォームとして機能し得ることを示しています。
引用: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
キーワード: がん免疫療法, ナノメディシン, ピロトーシス, がんワクチン, 腫瘍微小環境