Clear Sky Science · ja
NF1変異乳がんに対する患者由来多器官オルガノイドプラットフォームによる薬物動態・薬力学指標に基づく個別化治療
なぜこの研究が患者にとって重要か
多くのがん患者は、ある人にはよく効く一方で別の人には効かない薬や、しばしば強い副作用を伴う薬を投与されています。本研究は、患者自身の細胞から作製したラボ内のミニ臓器を用いて体外で治療を検証する新しい方法を示しています。対象は治療が難しいNF1遺伝子の変化によって駆動される乳がんで、遺伝子修復的アプローチと分子標的薬の併用が、より安全で効果的、かつ真に個別化された治療につながる可能性を示しています。
患者の身体のミニチュアを作る
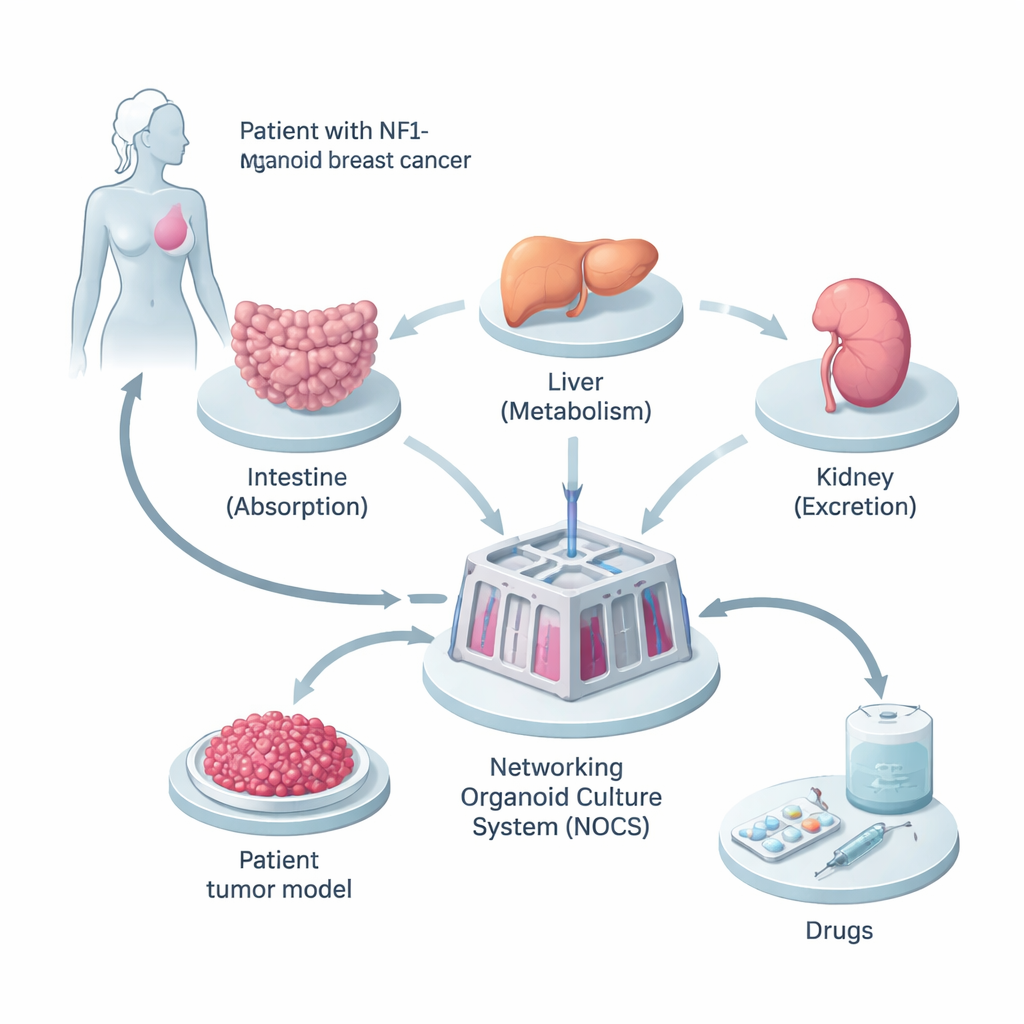
研究者らは、NF1遺伝子に生殖細胞系列の変異を持つ乳がん患者から採取した組織から出発しました。彼らは患者の正常な皮膚様細胞を人工多能性幹細胞にリプログラムし、これらからほぼあらゆる細胞型に分化可能な細胞を得ました。そこから、薬物が吸収、代謝、排泄される主要な部位である小腸、肝臓、腎臓の3種類のミニ臓器を作製しました。同時に、患者のがん細胞から3次元の腫瘍「スフェロイド」を作り、原発腫瘍で見られた細胞構成や遺伝的変化を保存しました。
生体に近い薬剤試験回路
これらのミニ臓器をより実際の身体に近づけるため、チームはそれらを液体で満たされた装置「Networking Organoid Culture System(NOCS)」でつなぎました。このセットアップでは、小腸、肝臓、腎臓、腫瘍のコンパートメント間を培養液が循環し、血流を模倣します。薬剤は経口投与や注射のような方法で添加でき、センサーやポンプで“血流”の速度や更新頻度を制御します。これにより、薬剤の吸収量、分解速度、腫瘍に対する作用の強さを、患者特異的かつヒト由来のモデルで追跡することが可能になりました。
エクソンスキッピングによる壊れた遺伝子の修復
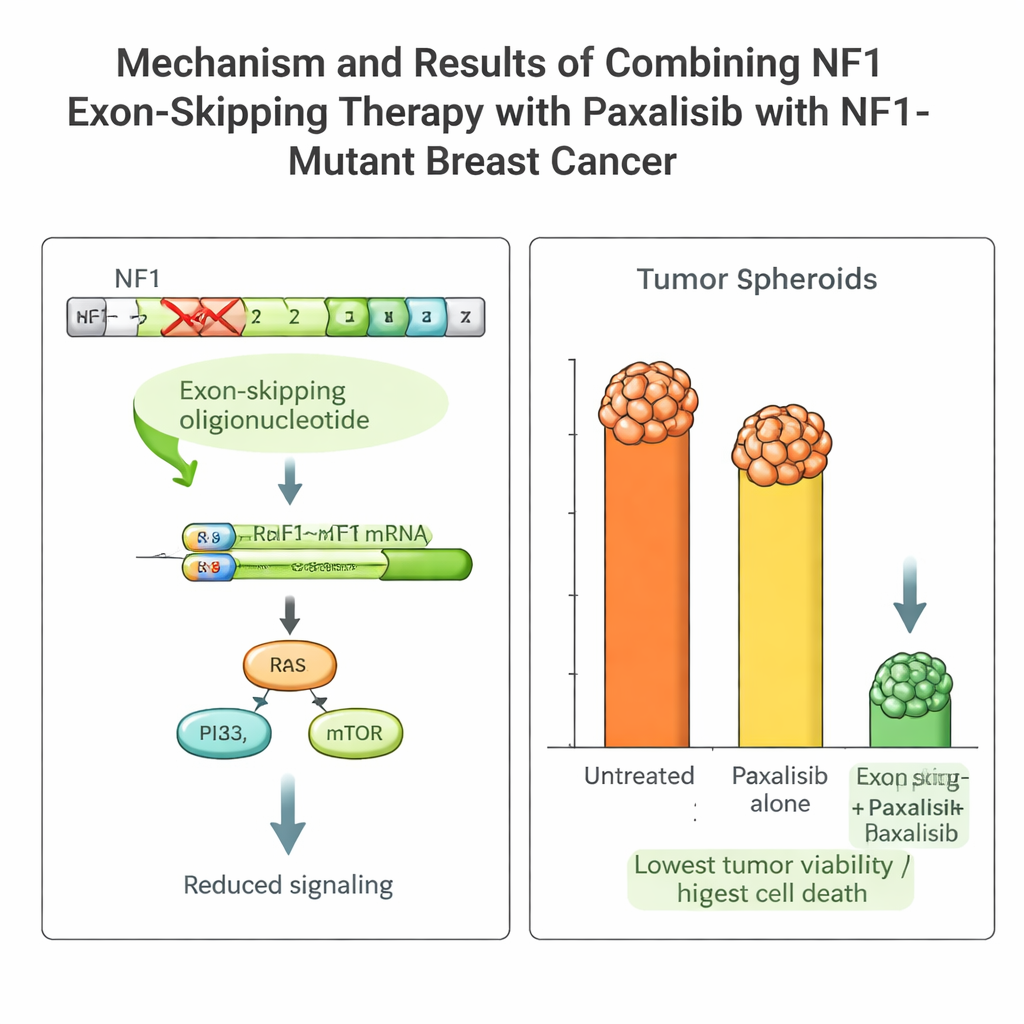
患者の腫瘍は増殖シグナルを持続的にオンにする有害なNF1変異を含んでおり、多くの標準薬が効きにくい状態でした。チームはアンチセンスオリゴヌクレオチドと呼ばれる短い遺伝材料を設計し、細胞のRNA処理機構にNF1遺伝子の欠陥部分(エクソン2)を飛ばさせることで問題を回避させました。数日間持続するウイルスベクターを用いて安定した「エクソンスキッピング」を患者のがん細胞に誘導すると、短縮されたが機能を持つNF1タンパク質が産生され、過剰な増殖シグナルが抑えられ、腫瘍細胞の薬剤感受性が向上しました。
PK/PD指標で適切な標的薬を選ぶ
このプラットフォームを用いて、チームはNF1の下流に位置するPI3K–mTOR経路を阻害する複数の先進的薬剤を比較しました。彼らは薬物動態(体内での薬の扱われ方)と薬力学(腫瘍に対する薬の作用)をマウスとNOCSの両方で測定しました。パキサリシブ(Paxalisib)という薬剤が際立っており、小腸での吸収が良好で、体内で有効な濃度が持続し、動物モデルとオルガノイド装置で類似の挙動を示しました。NF1エクソンスキッピングと組み合わせると、パキサリシブは患者由来腫瘍細胞に対する殺傷力が著しく高まり、増殖の大幅な抑制とプログラム細胞死の明確な指標がNOCSおよび患者由来腫瘍を移植したマウスの両方で観察されました。
臓器間での利益とリスクのバランス
小腸、肝臓、腎臓モデルが同一回路に組み込まれていたため、研究者らは臓器損傷の早期兆候も観察できました。パキサリシブは腸と腎のモデルでストレス応答や障壁の弱化を引き起こし、肝臓では負担の兆候が見られましたが、試験した用量では細胞生存率の大きな低下は確認されませんでした。この種のヒト組織を用いた全身的な視点は、腫瘍縮小だけでなく、薬剤が患者に投与される前に健康な臓器にどのような影響を与えるかを比較する手段を提供します。
将来のがん医療にとっての意義
簡単に言えば、この研究は単純化された患者特異的な「チップ上のミニ身体」を作り、さまざまな薬剤や遺伝子修正アプローチがどのように作用し相互作用するかを試験できることを示しています。このNF1変異乳がん患者にとって、最適な戦略はNF1エクソンスキッピング療法と経口薬パキサリシブの組み合わせであり、両者の併用は単独治療よりも腫瘍成長をはるかに抑制しました。さらに開発され、より多くの患者で検証されれば、このようなプラットフォームは医師が各人の遺伝情報と生物学に合わせた治療計画を選ぶ手助けとなり、成功の可能性を高めつつ不要な毒性を減らすことが期待されます。
引用: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
キーワード: 個別化腫瘍学, 乳がん, オルガノイド, NF1変異, 分子標的治療