Clear Sky Science · ja
卵巣がん患者の免疫療法を強化するための、脂質駆動性免疫代謝経路を腹膜の転移に応用する
腹部の脂肪が卵巣がんに重要な理由
卵巣がんはしばしば大網と呼ばれる腹部の脂肪性組織に転移します。この部位は脂肪細胞と免疫細胞が豊富で、単なる受動的な存在以上の役割を果たします。本要約で示す研究は、大網の転移巣で免疫細胞が脂質をどのように利用・処理するかが、現代の免疫療法の恩恵を受ける患者がごく一部にとどまる理由を説明し得ることを示しています。また、治療効果を広げる可能性のある薬剤併用や、スキャンに基づく検査法の提案も示唆しています。
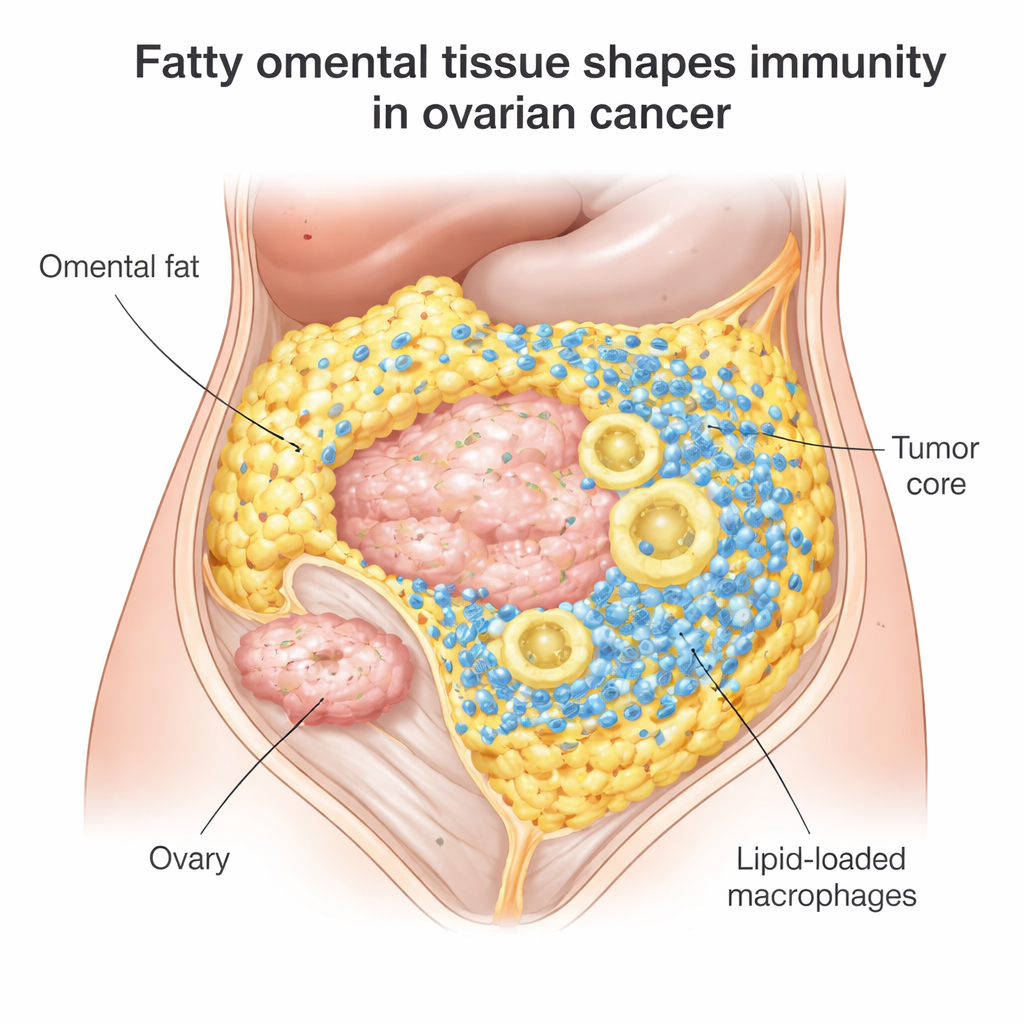
腹部脂肪の中の隠れた戦場
上皮性卵巣がんの多くの女性は最初に手術と化学療法に反応しますが、70~80%で再発し、ニボルマブやペムブロリズマブのような免疫チェックポイント阻害薬が効果を示すのは約10~15%にすぎません。研究者らは脂肪細胞が集まる大網転移に注目しました。100を超える腫瘍サンプルを詳しく調べたところ、大網の腫瘍はキラーT細胞や大きな掃除屋細胞であるマクロファージに満ちていることが分かりました。しかし問題がありました。これらのT細胞は腫瘍コアに浸潤するのではなく、腫瘍と脂肪の境界に集積する傾向があり、本当に必要とされる腫瘍内部まで到達していませんでした。
ある免疫細胞を養い、別の免疫細胞を圧倒する脂肪
さらに解析を進めると、これらの脂肪を含む腫瘍中のT細胞は、近傍の脂肪細胞から脂質を取り込み局所環境へ適応していることが明らかになりました。これにより代謝的に“健全”に保たれ、遺伝子発現や試験管内試験で患者自身の腫瘍細胞を認識して殺す能力があることが示されました。一方で、大網に存在する多くの腫瘍関連マクロファージは脂肪滴で過度に満たされていました。脂質で満たされたこれらのマクロファージは、活性酸素種に関連する酸化ストレスの兆候を示し、免疫抑制的で腫瘍を支持する状態へと偏っていました。言い換えれば、同じ脂肪に富む環境が有効なT細胞を養う一方で、マクロファージを有害なモードに追いやり全体の免疫攻撃を弱めているのです。
既存薬で過食状態のマクロファージを再プログラムする
研究チームは次に、ストレス状態にあるこれらのマクロファージを味方に変えられるかを検証しました。新鮮な腫瘍片を培養して二つのアプローチを試しました。一つはCCR5を遮断する抗HIV薬マラビロクスを用いる方法で、CCR5は腫瘍–脂肪境界で豊富に見られるシグナルCCL5の受容体です。もう一つは脂肪酸を取り込む主要な“スカベンジャー”受容体であるCD36を阻害する方法です。いずれの処置もマクロファージ内の脂質負荷を減らし、酸化ストレスや有害な脂質過酸化のマーカーを低下させ、炎症シグナルの放出を引き起こしました。重要なのは、これらの処置がキラーT細胞の増殖と脂肪縁から腫瘍コアへの移動を促し、外部から免疫細胞を追加しなくとも局所免疫活性を高めた点です。
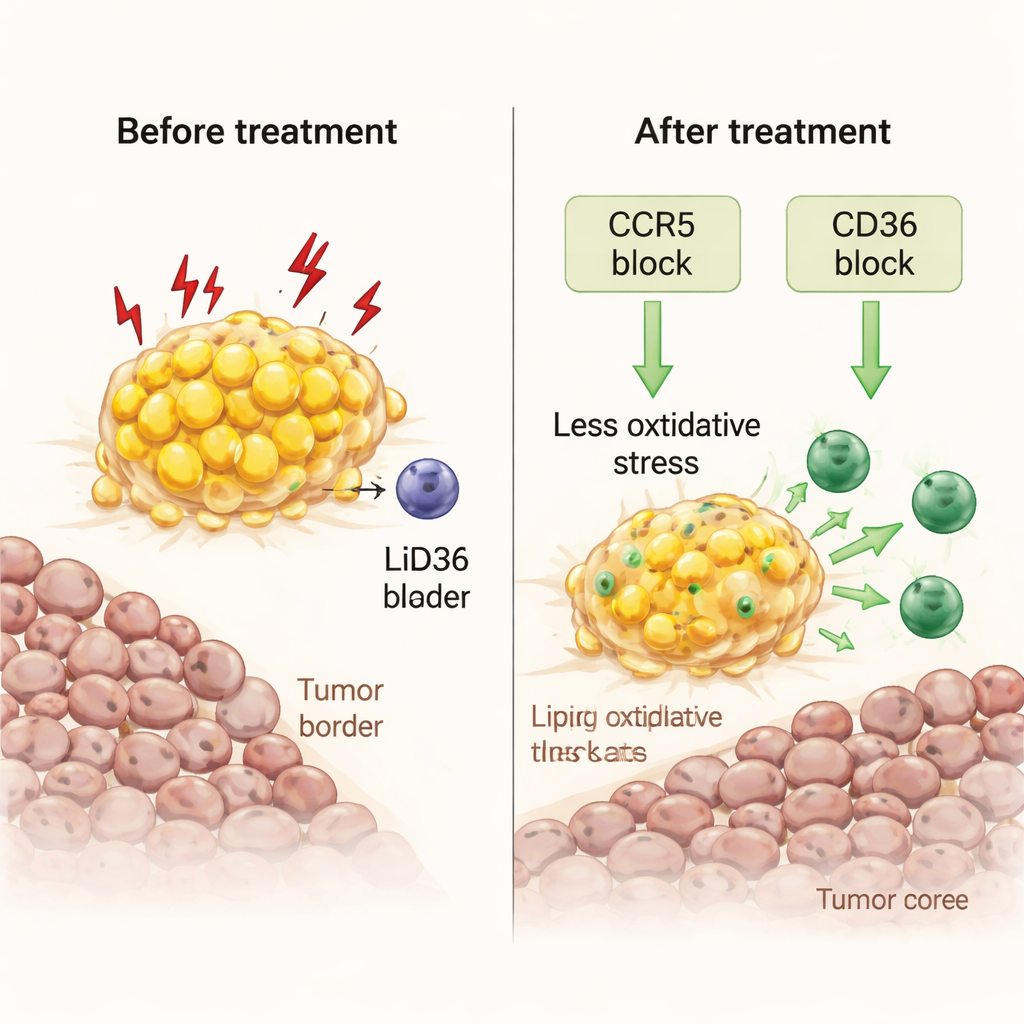
細胞経路から現実的なモデルと患者へ
これらの考えをより現実的な状況で検証するため、チームはヒト様免疫系をもつヒト化マウスを使い、脂肪豊富な組織にヒトの乳がんを移植しました。マラビロクス治療は患者由来サンプルと一致する形でヒトマクロファージを再プログラムし、脂質やストレスの署名が減少し、サイトカイン産生が増え、T細胞関連経路を強化しました。臨床的には、研究者らは化学療法耐性卵巣がんに対する日本のニボルマブ試験を再解析しました。薬剤の恩恵を受けた患者は全員、手術サンプルで大網転移が確認されました。CTやMRIスキャンと体脂肪分布の機械学習解析を組み合わせて、腫瘍が内臓脂肪に近接している可能性を非侵襲的に判定する決定木を構築し、1例の前向きケースではこの方法が後にニボルマブに反応した患者を正しく予測しました。
将来の治療に向けての意義
専門外の方への要点は、「卵巣がんが体内のどこに成長するか」と「近接する脂肪が免疫細胞をどう変えるか」が、免疫療法の効果を強く左右し得るということです。脂肪に富む大網転移は活発なT細胞を抱える一方で、過度に脂肪を取り込んでストレスを受けたマクロファージが免疫攻撃を鈍らせています。これらのマクロファージの脂質負荷を軽減し酸化ストレスを和らげること――CCR5阻害剤(マラビロクスなど)やCD36標的薬、あるいはそれらに関連する戦略の併用――により、部分的に遮断された免疫応答を腫瘍に対する全面的な攻撃に転換できる可能性があります。同時に、大網関与を示す画像診断指標は、どの患者が免疫チェックポイント阻害薬の恩恵を受けやすいかを選別する助けとなり、卵巣がん治療により個別化され効果的なアプローチをもたらす可能性があります。
引用: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
キーワード: 卵巣がん, 大網の脂肪, 免疫療法, 腫瘍関連マクロファージ, 脂質代謝