Clear Sky Science · ja
心筋細胞でのKLF15活性を高める:ヌクレアーゼ欠損dCas9VPRによる病的リプログラミングと線維化を防ぐ新手法
失敗する心臓のリプログラミング
心不全は何百万人にも影響を及ぼし、多くは長年の高血圧や弁疾患の後に徐々に進行します。こうした状態では、心筋細胞は肥大するだけでなく「胎児期」に特徴的な遺伝子プログラムを再活性化し、心臓は瘢痕組織で満たされます。本研究は、DNAを切断することなく、心筋細胞内の保護的な調節因子であるKLF15の活性をやさしく高めることで、心臓自身の遺伝子制御機構を健康な状態へ向けて戻す新しい方法を探ります。
心筋細胞がアイデンティティを失うとき
健康な成人心臓では、心筋細胞は効率的に脂肪を燃料として利用し、安定した遺伝子発現パターンを維持しています。慢性的な圧負荷を受けたマウスで単一細胞RNAシーケンスを用いて解析したところ、心臓が正常な機能から拡大し最終的に心不全に至る過程で、個々の心筋細胞がどのように変化するかが詳細にマッピングされました。研究者らは、代謝と増殖のバランスを保つKLF15という転写因子が、病的細胞で最も顕著に活動変化を示すことを見いだしました。ストレスが高まるにつれてKLF15の発現は低下し、胎児期やストレス関連遺伝子を抑える機能が弱まりました。同様のKLF15低下は、拡張型および肥大型心筋症の患者由来のヒト心臓でも確認され、この撹乱が種を超えて保存されていることを示しています。
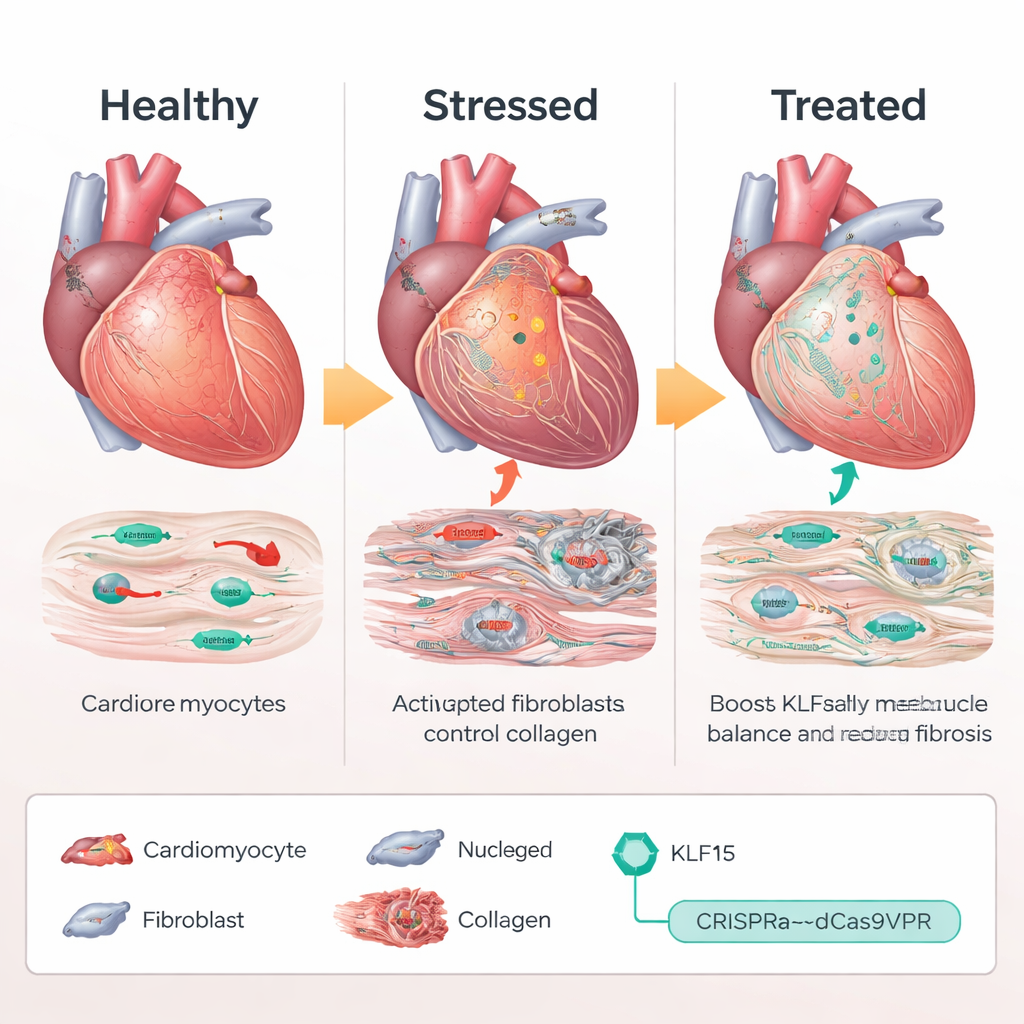
ハサミではなくボリュームノブとしてのCRISPR
KLF15遺伝子のコピーを追加したりDNAを切断したりする代わりに、チームはdCas9VPRと呼ばれるCRISPRベースの「活性化」システムを用いました。これは天然のKlf15遺伝子の近傍に結合してその発現を高めます。心筋細胞のみでこのCRISPR活性化因子を発現するように作られたマウスでは、アデノ随伴ウイルス(AAV9)でガイドRNAを送り込みKlf15プロモーターを標的にしました。慢性的な圧負荷下で、Klf15を活性化するガイドを受け取ったマウスはほぼ正常なKlf15レベルを維持しました。彼らの心筋細胞は小さく保たれ、駆出能の低下が小さく、生存率が対照群より改善しました。分子レベルではストレス・胎児遺伝子が抑制され、代謝やカルシウム取り扱い遺伝子が回復し、不健康な転写プログラムが大部分リセットされたことを示しました。
細胞間クロストークによる線維化の抑制
心不全は病んだ筋細胞だけでなく、コラーゲンを産生して硬い瘢痕組織を形成する支持細胞である線維芽細胞にも駆動されます。単一細胞解析と組織イメージングにより、心筋細胞でKlf15を回復させると線維芽細胞の活性化と全体的な線維化が減少することが示されました。遺伝子治療が線維芽細胞を直接標的にしていないにもかかわらずです。研究チームはこの効果を分泌タンパク質AZGP1に帰しました。心筋細胞でKlf15を高めると、AZGP1の産生と分泌が増加しました。マウス心臓とヒトの幹細胞由来心組織の両方で、増加したAZGP1は線維芽細胞の線維化を駆動する主要経路であるTGF-β/SMADシグナルを抑え、α-SMAやPOSTNといったマーカーのレベルを低下させました。重要な点として、心筋細胞単独でのAZGP1過剰発現は筋細胞自体のリプログラミングを引き起こさず、KLF15が主に心筋細胞を直接保護しつつ、AZGP1をメッセンジャーとして線維芽細胞を抑制することを示しています。
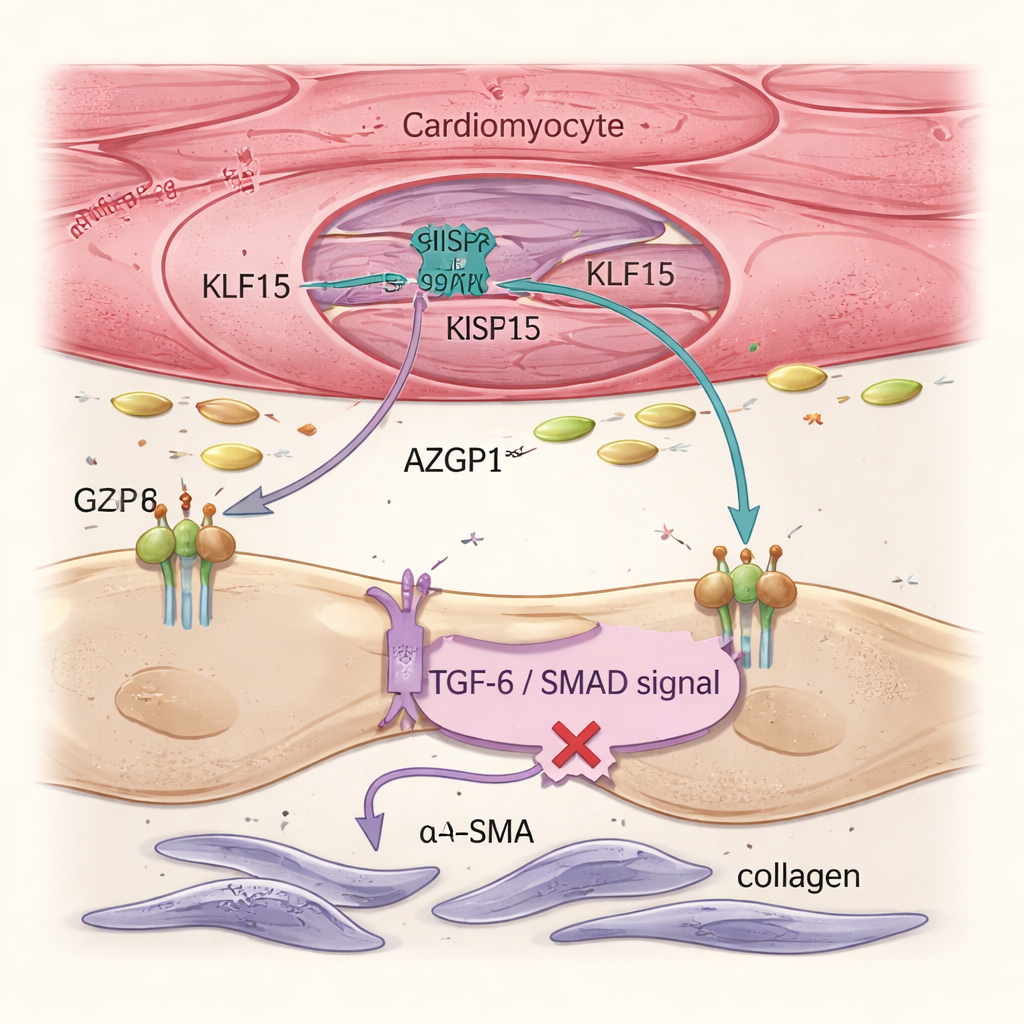
ヒト組織モデルが保護回路を裏付ける
これらのメカニズムがヒト細胞でも成り立つかを検証するため、研究者らは三次元のエンジニアードハートティッシュで培養したヒトiPS細胞由来心筋細胞を用いました。高血圧を模した機械的負荷を加えると、これらの組織はKLF15を失い、ストレスおよび胎児遺伝子をオンにし、硬化して収縮力が弱まり、疾患の特徴を再現しました。CRISPRaによるKLF15回復はこの機能低下を防ぎ、力の発生を維持し、遺伝子発現を成熟した代謝や構造方向へ戻しました。詳細な実験は、よく知られた線維化促進シグナルであるTGF-β1がSMAD2/3経路を介してヒト心筋細胞のKLF15を低下させることを示し、慢性的なストレスが不適応的なリモデリングを引き起こす仕組みを説明しました。最後に、研究チームは単一のAAV9ベクターに収まる小型のCas9バリアントに基づくコンパクトな「ミニ」CRISPRaシステムを心筋細胞特異的プロモーターで駆動するように設計しました。心不全患者の精密切片培養において、このベクターはKLF15レベルを上昇させ、培養数日にわたって収縮性能を改善しました。
より穏やかな遺伝子治療の設計図
専門外の方への核心は、心筋細胞内部で単一の保護的調節因子を慎重に上げることで、細胞のアイデンティティを安定化させ、瘢痕化を抑える信号を送れるということです。DNAを切断しないCRISPRベースの活性化因子を用いることで、人工的な遺伝子を挿入するのではなく、心臓自身の遺伝子を微調整します。本研究は機械的ストレスと有害なリモデリングを結ぶTGF-β → KLF15 → AZGP1という経路を定義し、マウス、ヒト細胞モデル、ヒト心臓組織切片においてKLF15回復がこの連鎖反応を断ち切り得ることを示しました。まだ前臨床段階ではありますが、本論文で示されたコンパクトで心筋細胞標的のCRISPRaシステムは、ゲノムを書き換えるのではなく遺伝子活動を再プログラムすることで、一般的な非遺伝性心不全の治療に向けた実行可能なロードマップを提供します。
引用: Schoger, E., Kim, R., Bleckwedel, F. et al. Enhancing KLF15 activity in cardiomyocytes: a novel approach to prevent pathological reprogramming and fibrosis via nuclease-deficient dCas9VPR. Sig Transduct Target Ther 11, 76 (2026). https://doi.org/10.1038/s41392-026-02593-9
キーワード: 心不全, KLF15, CRISPR活性化, 心臓線維症, AZGP1