Clear Sky Science · ja
外因性エプスタイン・バーウイルス核抗原1はADAR1駆動の免疫療法耐性を誘導する
なぜありふれたウイルスががん治療で重要なのか
多くのがんは、体の免疫系を解き放つ免疫療法薬で治療されるようになりました。それでも多くの患者が恩恵を受けられないのは、腫瘍が免疫の攻撃から身を隠す術を身につけるためです。本研究は、極めて一般的なウイルスであるエプスタイン・バーウイルス(EBV)が、腫瘍の免疫防御をどのように遮断してこれら強力な薬剤に抵抗させるか、そして新しいタイプの設計分子がその防御を再び活性化できる可能性を明らかにします。
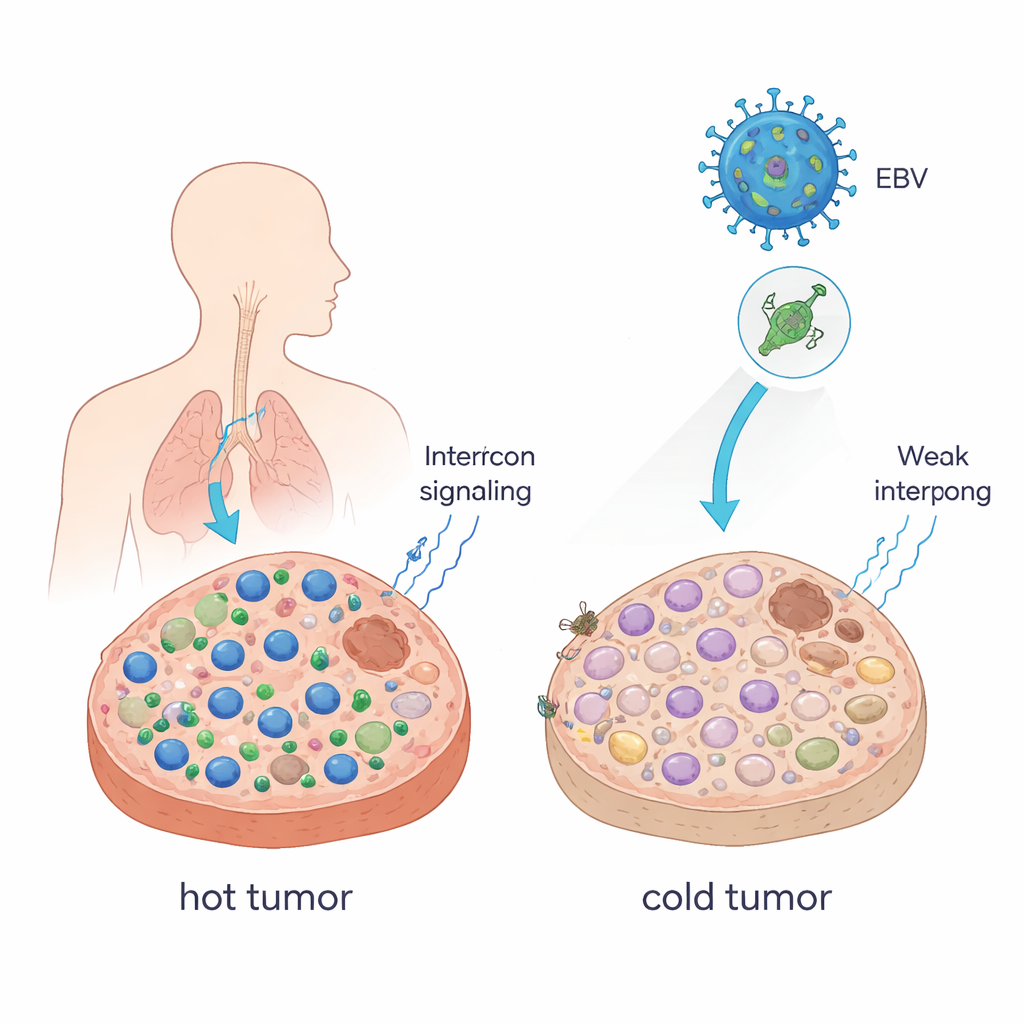
“ホット”な腫瘍を“コールド”に変える
臨床では、がんを攻撃するT細胞が豊富な場合を「ホット」、そうでない場合を「コールド」と表現します。ホットな腫瘍は通常、抗PD-1抗体などの免疫チェックポイント阻害(ICB)薬に良く反応しますが、コールドな腫瘍はしばしば反応しません。著者らは、単一のEBVタンパク質であるEBNA1が腫瘍をよりコールドで回避的な状態へと押しやることを示しました。マウスの腫瘍細胞にEBNA1の産生を強制し、免疫系が健在なマウスで増殖させると、腫瘍は大きくなり、CD8+ T細胞やナチュラルキラー細胞が少なくなり、免疫抑制性のマクロファージが増えました。免疫細胞を動員する重要なメッセンジャーであるインターフェロンのシグナルも強く抑制されました。EBVと強く関連する鼻咽頭癌の患者試料でも、EBNA1を発現する腫瘍は正常組織に比べてCD8+ T細胞が少ないことが観察されました。
ウイルスが細胞のRNA制御機構に短絡する仕組み
EBNA1が腫瘍環境をどのように変えるかを解明するため、研究者らはEBNA1と物理的に相互作用するヒトタンパク質を探索しました。注目したのはIGF2BP3というタンパク質で、これはメッセンジャーRNA上の小さな化学マーク(m6A)を読み取り、mRNAの安定性や翻訳を高め得ます。EBNA1は複数の細胞種、EBV陽性のがん細胞を含めてIGF2BP3に強く結合しました。患者腫瘍のデータは、IGF2BP3の高発現がインターフェロン関連遺伝子の活性低下やCD8+ T細胞浸潤の減少と相関することを示しており、このウイルスと宿主の提携が抗腫瘍免疫を弱め得ることを示唆しています。
危険信号を沈黙させるRNA編集酵素の増強
さらに詳しい解析は、この相互作用の主要な標的としてADAR1を浮かび上がらせました。ADAR1は二本鎖RNAの中の特定の「A」を「I」に変換するRNA編集酵素です。こうした編集は、細胞内のウイルス様RNAを内在するセンサーにとって危険性が低いものに見せかけ、インターフェロン応答を減弱させ得ます。著者らは、EBNA1・IGF2BP3・翻訳因子EIF4G1がADAR1のmRNA上で三者複合体を形成することを見いだしました。この複合体はm6A付加を増やし、翻訳装置を呼び寄せ、ADAR1のmRNA量を増やさずにタンパク質産生を選択的に高めます。その結果、腫瘍細胞はインターフェロン関連遺伝子の近傍にある反復配列でより多くのRNA編集を行うようになります。これらの編集は、本来であればMDA5やPKRのようなセンサーを活性化する未編集二本鎖RNAのプールを減らし、インターフェロン産生を鈍らせて腫瘍が免疫の攻撃から隠れるのを助けます。
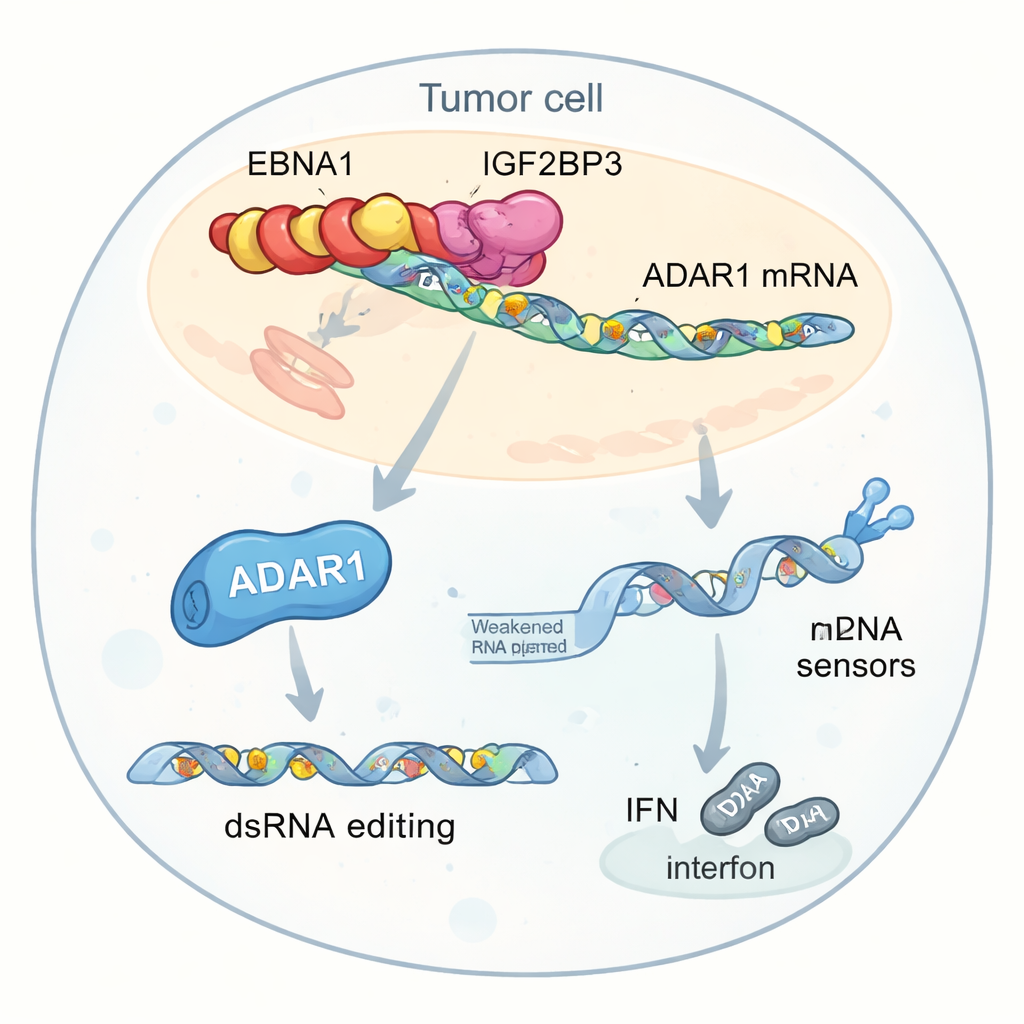
インターフェロン減少と免疫療法の弱化
EBNA1を発現する腫瘍細胞を実験室でT細胞や抗PD-1抗体にさらすと、対照細胞より殺されにくく、放出するインターフェロンも少なかった。直接インターフェロンで処理しても、EBNA1保有細胞は感受性が低く、内部のRNAセンサーの活性化も弱かった。ADAR1のレベルを低下させるとこれらの効果は部分的に逆転し、センサー活性とインターフェロンシグナルが回復しました。遺伝学的およびシークエンシング実験は、EBNA1発現細胞が特定のRNA領域でAからIへの編集イベントをより多く示し、特にインターフェロン刺激後に顕著であることを確認し、ウイルスによるADAR1増強が危険信号を無力化する助けとなっているという考えを支持しました。
免疫攻撃を再活性化する設計型分解剤
研究チームは次に、腫瘍からEBNA1を除去すれば免疫療法への脆弱性を回復できるかを検討しました。彼らはPROTAC分子EP-1215を設計し、EBNA1に細胞の廃棄機構による分解タグを付けるようにしました。低用量でEP-1215は効率的にEBNA1を分解し、ADAR1タンパク質レベルを低下させました。マウス実験では、EP-1215単独のEBNA1陽性腫瘍への効果は限定的で、抗PD-1単独も弱かった。しかし両者を組み合わせると腫瘍は劇的に縮小し、CD8+ T細胞の浸潤が増え、インターフェロンを産生するT細胞が増加しました。ヒト免疫細胞を有するヒト化マウス模型のEBV関連腫瘍でも、組み合わせ療法は単独治療を上回り、明らかな肝臓や腎臓の毒性は認められませんでした。
将来のがん治療にとっての意味
非専門家向けに言えば、要点はこうです:ありふれたウイルスががん細胞の内部アラーム系を静かに書き換え、本来であれば免疫細胞を惹きつけ活性化する化学信号を消してしまうことがある。EBNA1は宿主のRNAリーダー(IGF2BP3)と翻訳因子(EIF4G1)を乗っ取り、RNA編集酵素ADAR1を過剰に生産させることで、免疫センサーが認識するRNA構造を編集して消してしまう。EP-1215のような設計されたPROTACでEBNA1を分解することで、研究者らはこれらの危険信号を回復させ、抵抗性のある腫瘍を既存のチェックポイント阻害薬に再び応答させることができました。もし同様の戦略が人で安全かつ有効であると確認されれば、EBNA1のようなウイルス性の協力因子を標的にすることは、コールドでEBV関連の腫瘍をホットな標的に変え、現代の免疫療法が効くようにする新たな方法を提供する可能性があります。
引用: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
キーワード: エプスタイン・バーウイルス, 免疫療法耐性, ADAR1, RNA編集, 鼻咽頭癌