Clear Sky Science · ja
SARS-CoV-2侵入におけるコレステロール依存的膜融合の分子機構
呼吸器ウイルスにとってコレステロールが重要な理由
COVID-19の原因ウイルスであるSARS-CoV-2は、外被と宿主細胞膜を融合させることで細胞内に侵入します。本論文は、一見単純だが重要な問いを提示します:心血管疾患で知られる脂質であるコレステロールが、その融合段階にどの程度影響を与えるのか?著者らは、ウイルス膜中のコレステロールが感染効率を単に微調整するだけでなく、スパイクタンパク質を強力なドッキングプラットフォームへと組織化し、侵入を容易かつ確実にすることを示します。
ウイルス侵入の最小モデルを作る
この過程を解きほぐすため、研究者たちはリポソームと呼ばれる小さな脂質の泡を用いて試験管内にウイルスと細胞の出会いを再構築しました。一方のリポソームにはSARS-CoV-2スパイクを搭載してウイルス膜を模し、もう一方にはACE2受容体を載せて宿主細胞表面を模しました。これらを混合し、スパイクを融合準備状態へと“切断”する特定の酵素で活性化すると、人工膜同士が融合し、蛍光色素が一方の泡からもう一方へ移動しました。この単純化された系により、両側の脂質組成—コレステロール濃度を含む—を正確に調整し、融合が段階的にどのように進むかを観察できました。 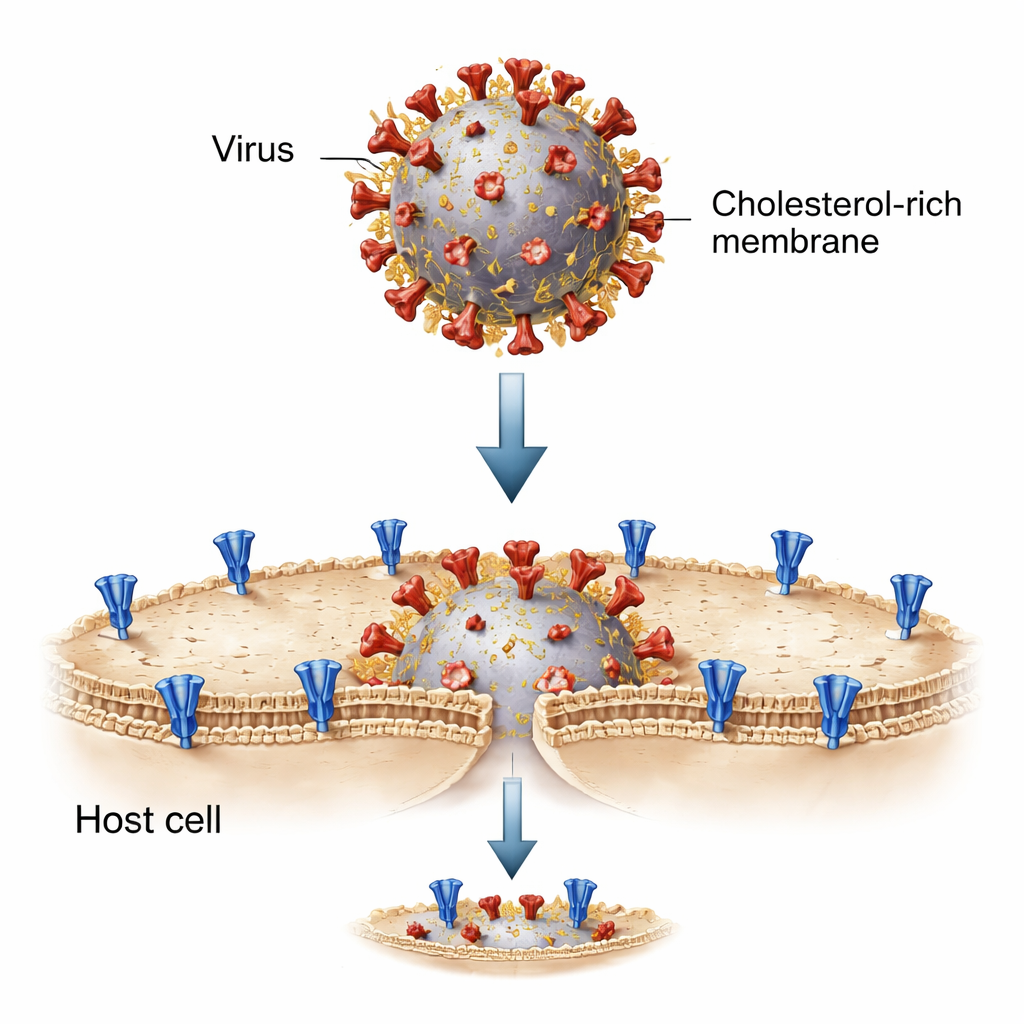
コレステロールは融合よりもドッキングを強化する
コレステロールを増減させたところ、スパイクを載せた膜にコレステロールを加えると融合の頻度が増すことがわかりましたが、それは予想されるような直接的な影響ではありませんでした。高コレステロールは、すでに付着している二つの膜が実際に融合する確率を劇的に変えるものではありませんでした。代わりに、スパイク搭載小胞がまずACE2搭載小胞にドッキングする頻度を大きく高めました。単一粒子イメージングでは、スパイクがコレステロールに富む膜にある場合に成功するドッキング事象が大幅に増え、一方でドッキング済みの対が完全に融合に至る確率はほぼ一定のままでした。興味深いことに、ACE2側にコレステロールを加えてもほとんど効果がなく、非常に高濃度ではむしろ融合を阻害することがあり、主要な推進力は宿主側ではなくウイルス側のコレステロールであることを示唆しています。
モデル膜から生細胞へ
研究者らは次に、同様のパターンが生細胞でも成り立つかを調べました。ヒト細胞をスパイクまたはACE2を発現するように設計し、混合すると大きな融合構造(合胞体)が形成されるのを観察しました。スパイク発現細胞からコレステロールを除去すると合胞体形成はほとんど止まり、コレステロールを復元すると融合が回復しました。並行して行ったSARS-CoV-2の“疑似ウイルス”(コロナウイルスのスパイクを用いて細胞へ入るが無害なウイルス粒子)を用いた実験でも、ウイルス膜からコレステロールを取り除くと感染が大きく低下し、再導入すると用量依存的に感染が増加しました。対照的に、ACE2発現細胞側のコレステロールだけを変えてもほとんど変化はありませんでした。すべてのアッセイにおいて一致したメッセージはこうです:スパイクを含む膜のコレステロールが効率的な侵入に不可欠である、ということです。
スパイククラスター:コレステロールの秘めたる武器
なぜウイルス側のコレステロールがそれほど重要なのか?高解像度イメージングは、コレステロールが豊富なときにスパイクタンパク質が密なクラスターを形成する傾向があり、コレステロールが枯渇するとより散在することを明らかにしました。単一分子測定はさらに踏み込み、コレステロール豊富な条件下でこれらのクラスターにより多くのスパイク分子が含まれることを示しました。著者らはこの効果を、スパイクの尾部にあるシステイン(システイン残基)に富む領域(CRR)に起因することを突き止めました。この領域はウイルス膜内部に位置し、パルミトイル化という脂質性の“アンカー”で修飾され、コレステロール濃厚なパッチに親和的です。スパイクの尾部を切り詰めるか、10個のシステインをすべて変異させてパルミトイル化を阻害すると、スパイクはコレステロールとともにクラスター化せず、コレステロールによるドッキングと融合の増強効果は消失しました。 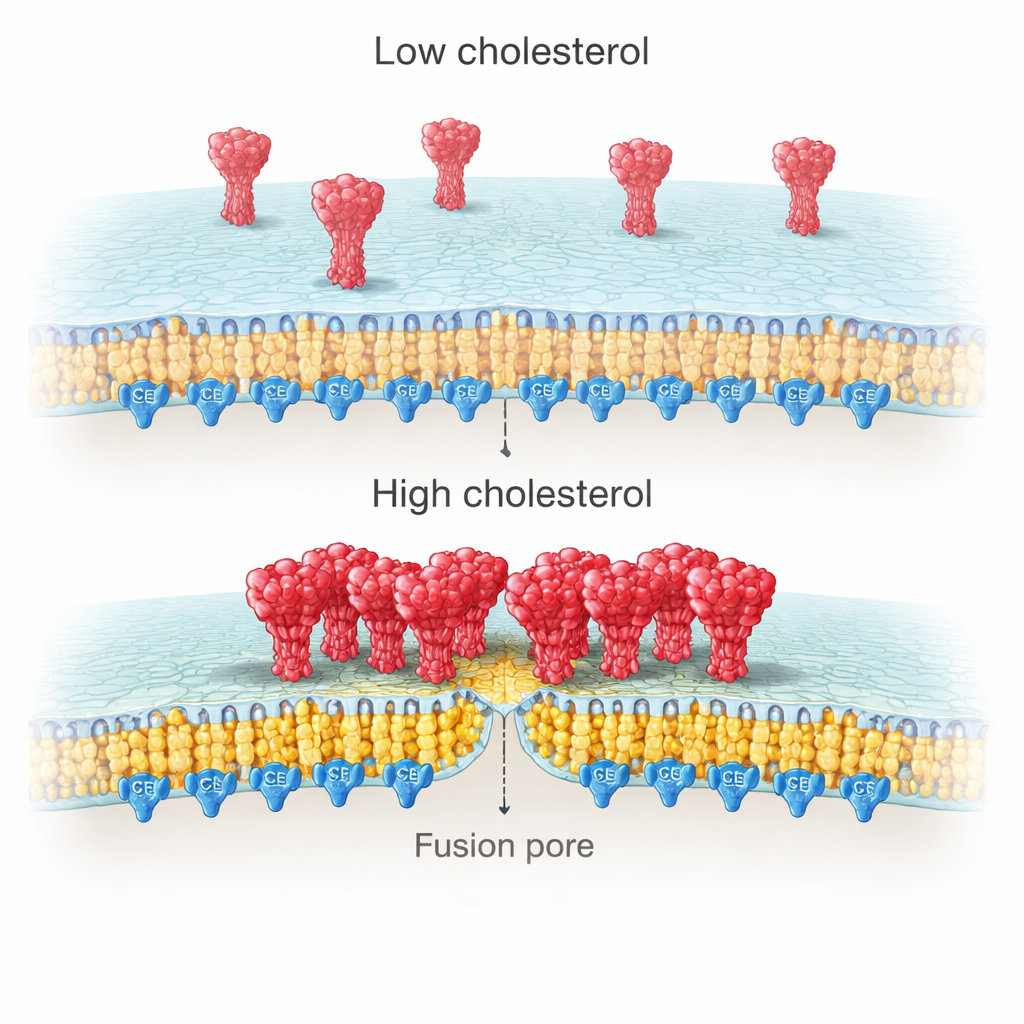
将来の治療にどう役立つか
簡潔に言えば、本研究はコレステロールがウイルス膜を融合プラットフォーム化することで、多数のスパイクタンパク質をそのパルミトイル化された尾部領域を介して密集させると結論づけています。これらのクラスターは宿主細胞のACE2へのドッキングをより効率的に行い、各出会いが成功した融合と感染につながる確率を高めます。非専門家向けの要点は、コレステロールがウイルス被膜の受動的な成分にすぎないのではなく、スパイク装置を能動的に組織化する要素であるということです。これは、スパイクのシステインに富みコレステロール感受性の尾部領域やそれをパルミトイル化する酵素が、さまざまなコロナウイルス変異株に対して有効な広範な抗ウイルス戦略の有望なターゲットになり得ることを示唆しています。
引用: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
キーワード: コレステロール, SARS-CoV-2スパイク, 膜融合, ウイルス侵入, パルミトイル化