Clear Sky Science · ja
PKC-eta は Hippo–YAP シグナル伝達経路を調節して乳がんの転移を促進する
この研究が重要な理由
トリプルネガティブ乳がん(TNBC)は、早期に広がりやすく標的治療がないため最も危険な乳がんの一つです。本研究は、がん細胞内の特定の酵素である PKC‑eta(PKCη)が、腫瘍の離脱、体内移動、新たな腫瘍の播種を助けるマスター・スイッチのように働くことを明らかにします。このスイッチを理解することで、研究者らはそれをオフにできる小さな天然ペプチドも特定し、この凶悪な病態に対する新たな治療法の可能性を示しています。 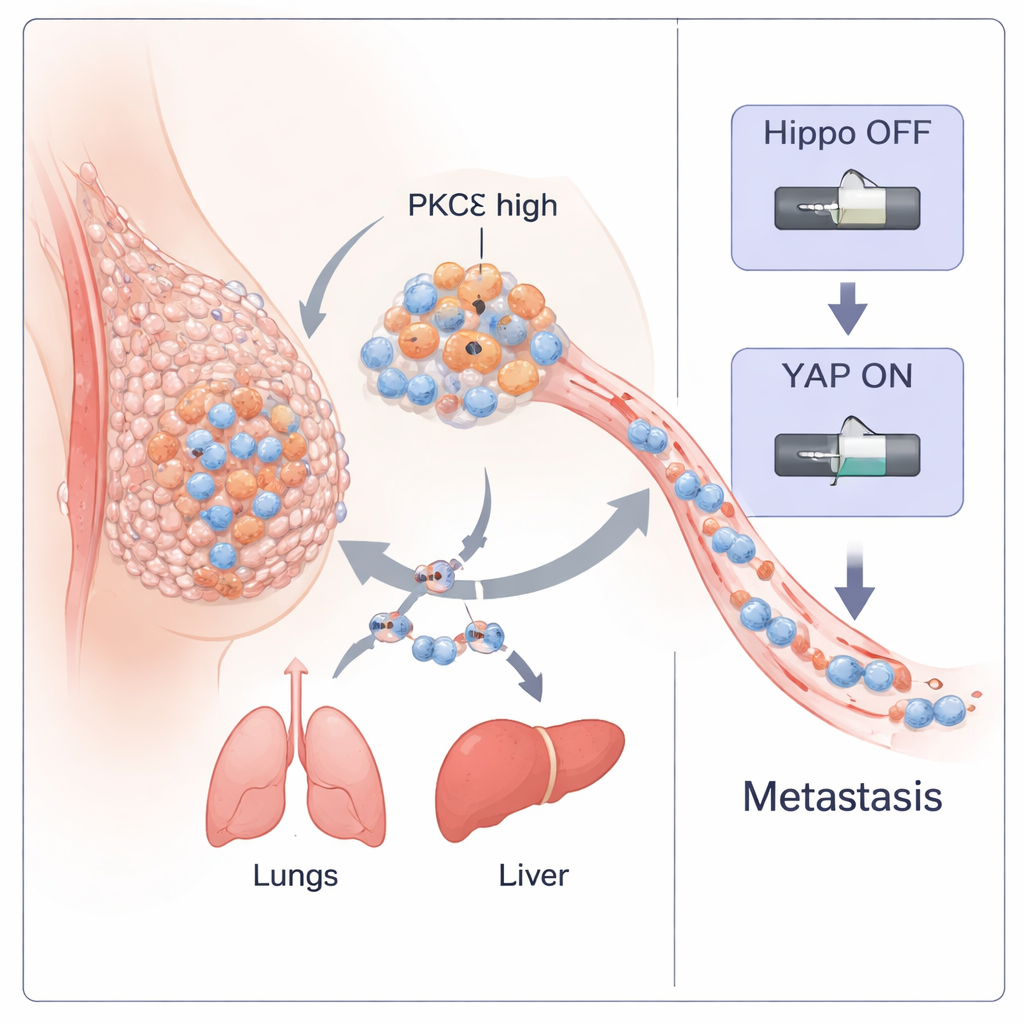
侵襲性の高い乳腫瘍に潜むドライバー
研究チームはまず大量の乳がん患者データを解析しました。その結果、PKCη をコードする遺伝子 PRKCH が「クラウディン低発現(claudin‑low)」として知られるサブタイプで特に高く、これは TNBC と強く重なり、幹様で高い運動能を持つ細胞が豊富であることが分かりました。複数の患者コホートにおいて、PRKCH の高い腫瘍は上皮–間葉転換(EMT)の署名を強く示していました。EMT は秩序だった細胞接着が緩み、形を変えて浸潤性を高める過程です。PRKCH レベルは原発腫瘍よりも転移巣で高く、ヒト TNBC 組織のタンパク質染色でも高悪性度・進行癌で核周囲に活性化した PKCη がより多く見られました。これらの結果は、PKCη が腫瘍の侵襲性と転移と密接に結びついていることを示唆します。
培養皿からマウスまで:PKCη が拡散を助長することを証明
因果関係を検証するため、研究者らは CRISPR 遺伝子編集を用いて、マウス由来の高転移性 TNBC 細胞株(4T1)とヒト由来細胞株(MDA‑MB‑231)の両方から PKCη を除去しました。PKCη がないと、細胞はより「上皮」状態へとシフトしました:E‑カドヘリンや EpCAM といった接着タンパク質が増加し、ビメンチンやN‑カドヘリンといった古典的な間葉マーカーは減少しました。PKCη 欠失細胞はコロニー形成能が低下し、移動・侵襲能が落ち、浮遊時の細胞死に感受性が高まり、がん幹細胞様の性質が著しく低下しました(CD44high/CD24low や ALDH 陽性細胞の減少、球形成能の低下)。マウスに注入すると、PKCη 欠損細胞は原発腫瘍が小さく、肺・肝・脳などへの転移が著しく少なく、マウスの生存期間も延びました。PKCη を元に戻すとこれらの変化は逆転し、この酵素が TNBC の進行と拡散を能動的に促進することが確認されました。
PKCη が増殖制御経路をどう乗っ取るか
次に、PKCη がどうやってこの転移促進力を発揮するかを詳細に調べました。患者データは、PKCη レベルが Hippo 経路により制御される強力な遺伝子スイッチタンパク質 YAP と同調して増減することを示しました。Hippo 経路は通常増殖を抑える細胞の「安全ブレーキ」です。PRKCH あるいは YAP1 の高発現は患者予後不良を予測し、両方が高いと遠隔転移非罹患生存率が特に悪化していました。TNBC 細胞では PKCη を除くと総 YAP レベルが低下し、核から細胞質へと移動して不活性化されました。生化学的実験により、PKCη は YAP に物理的に結合し、特異的に Ser128 部位にリン酸化を付加することが示されました。この修飾は YAP を安定化し、核へ移行して EMT、幹性、転移を駆動する遺伝子をオンにするのを助けます。PKCη が欠如すると、YAP は代わりに Ser127 や Ser397 といった別の部位でリン酸化され、14‑3‑3 タンパク質に結合して細胞質に閉じ込められ、最終的に分解されます。さらに PKCη は AKT 酵素の自然なブレーキである PTEN を高め、AKT 活性を低く保つことで、通常なら YAP を不活化する上流の Hippo キナーゼを抑制します。こうして PKCη は YAP を直接活性化すると同時に、間接的に Hippo の「ブレーキ」をオフに保ちます。 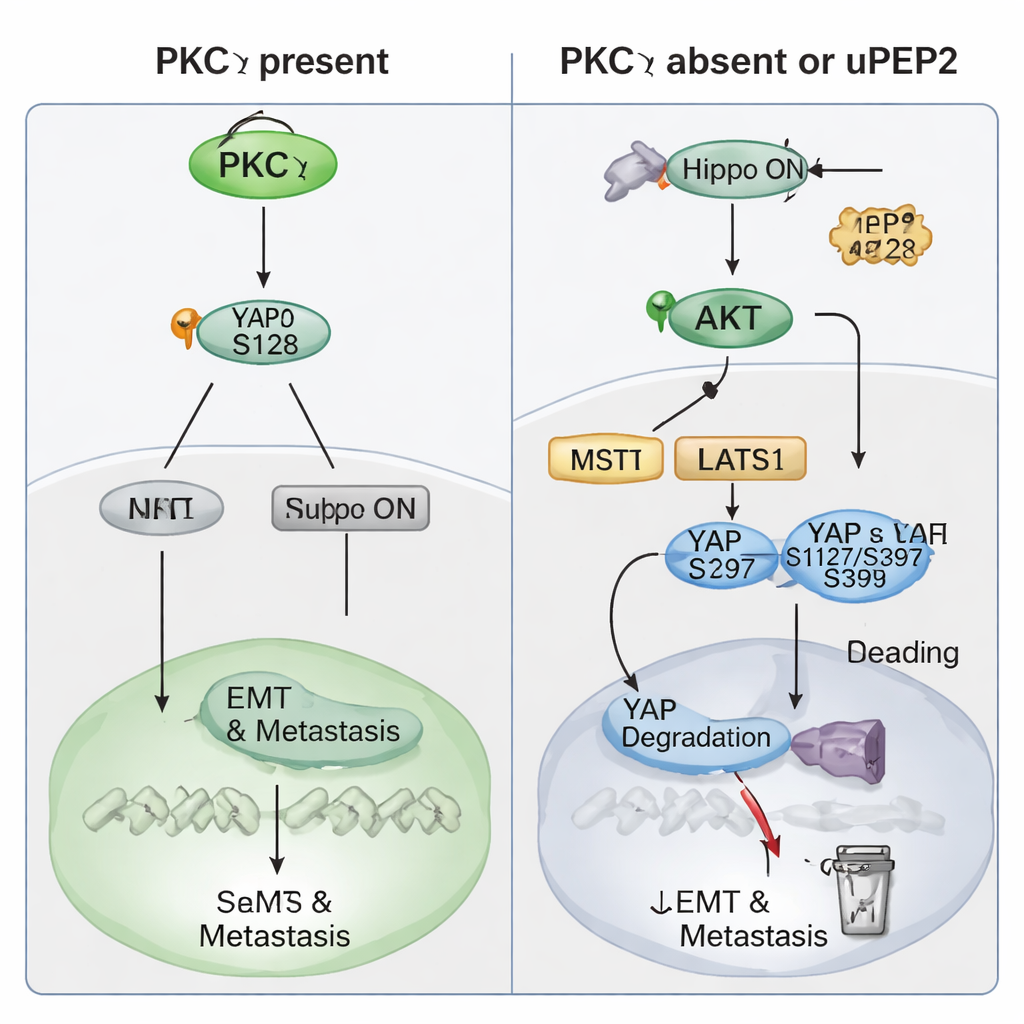
がんスイッチを無力化する小さなペプチド
興味深いことに、PKCη 遺伝子は短い上流開口フレーム(uORF)を持ち、uPEP2 と呼ばれるマイクロペプチドをコードしています。以前の研究は uPEP2 が PKCη や関連酵素に結合して阻害できることを示していました。本研究では、合成 uPEP2 で TNBC 細胞を処理すると PKCη ノックアウトと類似した効果が現れました:移動・侵襲・幹様挙動は低下し、EMT マーカーはより非侵襲的なプロフィールへ変化し、YAP レベルは低下しその“不活化”リン酸化標識は増加しました。マウス腫瘍では uPEP2 が原発腫瘍の PKCη と YAP を減少させ、YAP の不活化を増やし、肝臓や肺の微小転移が減少していました。機序的には、uPEP2 は PKCη の分解を促進し、Hippo 経路を再び作動させて YAP を細胞質に留めて分解へと導きます。
将来の治療にとっての意味
一般読者向けに言えば、本研究は PKCη を、最も侵襲的な乳がんが自然の増殖制御システムを無効化して YAP の“アクセル”を踏むことで緩み、移動し、遠隔臓器に定着するのを助ける要となる因子として同定したということです。PKCη を除去するか、天然の小ペプチド uPEP2 を用いて分解させることで、Hippo の安全ブレーキを回復させ、YAP を静め、前臨床モデルで転移を大幅に減少させることができました。なお本研究は細胞株および免疫不全マウスで行われた実験段階の成果であり、さらなる検証が必要ですが、PKCη とその YAP との相互作用は新しい TNBC 治療の有望な標的であり、uPEP2 に似た薬剤が将来的にこの治療困難ながんの拡散を防いだり抑制したりする助けになる可能性を示唆しています。
引用: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
キーワード: トリプルネガティブ乳がん, PKC-eta, Hippo-YAP 経路, 上皮–間葉転換, がん転移