Clear Sky Science · ja
Serpina3cは出生前プレドニゾン曝露で誘発される代謝機能異常関連脂肪性肝疾患から子孫を保護する
この研究が未来の子どもたちにとって重要な理由
多くの女性が妊娠中に重篤な自己免疫疾患や炎症性疾患を抑えるためにプレドニゾンを必要とします。医師は母体にとっては命を救うことがあると知っていますが、子どもの長期的な健康にどのように影響するかについてははるかに理解が進んでいません。本研究は差し迫った問いを投げかけます:妊娠中にプレドニゾンを服用することが、特に不健康な食事と組み合わさると、子どもの肝臓を将来的に脂肪肝にかかりやすく静かに準備してしまうのか?もしそうなら、そのリスクを逆転させる方法はあるのか?
世界的に増加する肝疾患の問題
代謝機能異常関連脂肪性肝疾患(MASLD)は、現在最も一般的な慢性肝疾患のひとつで、世界人口の約3分の1に影響を及ぼし、さらに増加すると予測されています。これには単純な肝脂肪蓄積、炎症を伴う「脂肪性肝炎」、線維化、肝硬変、さらには肝がんまで含まれます。MASLDは肥満、高血圧、2型糖尿病と強く結びついています。近年、科学者たちはこの病気の種が出生前にまかれる可能性があることを認識するようになりました。胎児が栄養不良や汚染物質、薬剤などのストレスにさらされると、その影響が一生の病気リスクを形作るという考えは「健康と疾患の発達起源」として知られています。 
出生前プレドニゾンが引き起こす「最初の打撃」
出生前プレドニゾンが肝臓に与える影響を調べるため、研究者らは妊娠ラットとマウスにヒトの低用量臨床投与を模した用量の薬を投与しました。その後、子孫を出生前から若年成人期まで追跡しました。子宮内でプレドニゾンに曝露された仔動物は単独でも体が小さく、肝臓の脂質処理に異常の徴候をすでに示していました:脂滴の増加、肝臓中のトリグリセリド増加、エネルギー源としての脂質利用の低下。成長するにつれても、通常の食事であっても肝臓により多くの脂肪を蓄えていました。後に高脂肪食、すなわち西洋型の外食中心の食事パターンに相当する食事で挑戦すると、その差は劇的になりました。プレドニゾン曝露の子孫はより重度の脂肪肝、炎症を発症し、雄では明らかな線維化の兆候も見られました。血糖コントロールも悪化し、より広範な代謝トラブルを示しました。
保護する肝タンパク質が失われる
さらに詳しく調べるために、チームは大規模な遺伝子プロファイリングを用いて雄雌双方の子孫の肝臓で共有される分子変化を探しました。ひとつの遺伝子が際立ちました:Serpina3c、分泌性タンパク質であり自然の酵素阻害因子ファミリーに属します。両性で、出生前プレドニゾンは胎児晩期から成人期に至るまで肝臓と血流中のSerpina3cを鋭くかつ持続的に低下させました。研究者が健康なマウスの肝臓で意図的にSerpina3cを減少させると、その動物も高脂肪食下で特に脂肪肝と糖代謝不良になりやすくなりました。逆に、出生後にプレドニゾン曝露の子孫の肝臓でSerpina3cを増強すると、肝脂肪の蓄積が大幅に減り、グルコース代謝が改善し、炎症や線維化も軽減されました。
プレドニゾンが肝臓の制御スイッチを書き換える仕組み
研究者らは次に、出生前プレドニゾンがどのようにSerpina3cを抑えるのかを問いただしました。彼らはプレドニゾンの活性型であるプレドニソロンが、肝細胞に存在する薬剤感知タンパク質であるグルココルチコイド受容体を過剰に活性化することを見出しました。この受容体はHDAC3という別のタンパク質と協働し、ヒストンタンパク質から小さな「アセチル」標識を除去してDNAの包装を引き締めます。動物の肝臓と培養肝細胞の両方で、プレドニソロンはSerpina3c遺伝子の部位でグルココルチコイド受容体とHDAC3の活性を高め、H3K27と呼ばれる重要な部位のアセチル化マークを剥ぎ取りました。これらのマークが失われると遺伝子の活動は低下し、Serpina3cタンパク質量は減少しました。受容体やHDAC3を遮断するか脱アセチル化を阻害すると、これらのアセチルマークが回復し、Serpina3cが増加し、肝細胞における脂質と糖の取り扱いが改善しました。
肝内で起こる有害な連鎖反応
Serpina3cの低下は二次的な有害なカスケードを引き起こしました。通常、Serpina3cはキマ―ゼのような酵素を抑えて、組織内でホルモンであるアンジオテンシンIIを局所的に産生するのを抑制します。Serpina3cが不足すると、キマ―ゼの量と活性が上昇し、肝臓内でより多くのアンジオテンシンIIが生成され、肝細胞上の受容体AT1Rが過剰に活性化されました。この局所ホルモンの急増は酸化ストレス、インスリン抵抗性、脂肪蓄積、炎症、線維化を促進することが知られています。プレドニゾン曝露動物と肝特異的にSerpina3cがノックダウンされたマウスの両方で、キマ―ゼ–アンジオテンシンII–AT1R経路が作動し、本来は脂肪燃焼やグルコース取り込みを支える主要遺伝子群が抑制されていました。出生後にSerpina3cを回復させるとこの経路は沈静化し、より健全な代謝が復活しました。 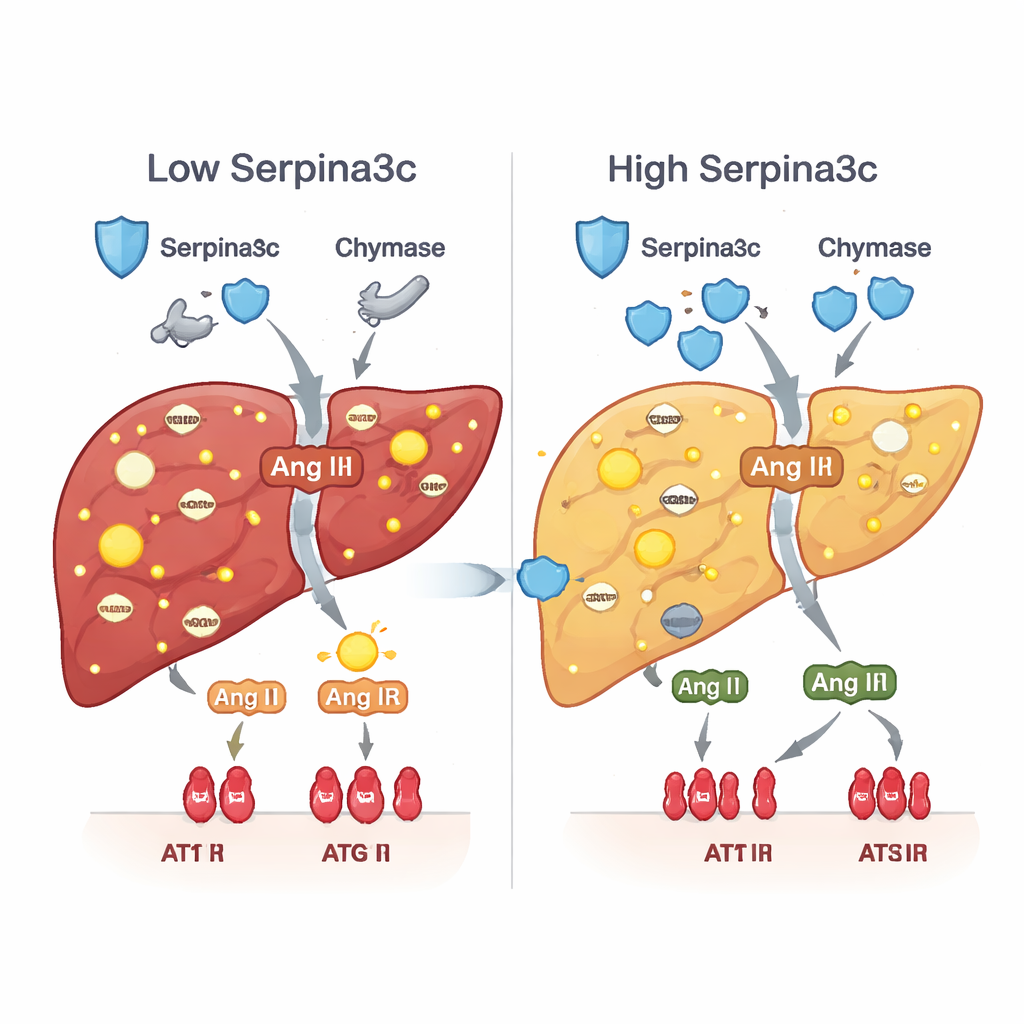
患者と家族にとっての意味
非専門家向けの主なメッセージは、妊娠中に服用された薬が発達中の肝臓に分子的な指紋を残し、それが成人期まで持続し得るということです。本研究では、プレドニゾンは「最初の打撃」として働き、エピジェネティックな変化—DNA包装タンパク質への化学的標識—を介して保護タンパク質(Serpina3c)を低下させ、後の「二次の打撃」である高脂肪食のような要因がより容易に脂肪肝を引き起こすようにしました。励みになる点は、このリスクが固定的ではなかったことです:出生後に肝臓でSerpina3cを再増強すると肝障害が著しく減少しました。これらの結果はげっ歯類で得られたものであるものの、妊娠中にプレドニゾンを必要とした母親の子どもをどのようにモニターし支援するかという重要な疑問を提起し、Serpina3cおよびキマ―ゼ–アンジオテンシンII系が出生前に始まる脂肪肝疾患の予防や治療の有望な標的になり得ることを示しています。
引用: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
キーワード: 出生前プレドニゾン, 脂肪肝疾患, エピジェネティクス, Serpina3c, 発達起源