Clear Sky Science · ja
抗ウイルス薬の創薬と開発:課題と今後の方向性
なぜより優れた抗ウイルス薬がまだ必要なのか
COVID-19パンデミックは、新たなウイルスがどれほど速く日常生活を一変させ得るか、そしてワクチンだけでは不十分な場合に良い医薬品にいかに依存しているかを示しました。本総説は過去60年にわたる抗ウイルス薬開発を振り返り、どのようにして将来のウイルス脅威に対してより速く、より賢く、より広範な防御を構築できるかを問いかけます。研究者が抗ウイルス薬をどのように発見し、設計し、投与するか、COVID-19から何を学んだか、人工知能やナノテクノロジーのようなツールがどのように状況を変え得るかを、一般読者にも分かりやすく説明しています。
最初の抗ウイルス薬から現在の武器庫まで
抗ウイルス医薬は比較的若い分野です。1960年代の最初の承認薬であるイドクスウリジンは、DNAの構成要素を変えることでウイルスの複製を遅らせ得ることを示しましたが、正常な細胞にも有害であり、眼科局所投与に限られました。その後登場したアシクロビルは、主に感染細胞内で活性化される画期的なヘルペス薬であり、有効かつ安全に使える薬の代表例になりました。1980年代にはジドブジンがHIVの初の治療薬になり、現在HIVを管理可能な慢性疾患に変えた現代的な併用療法への道を開きました。数十年にわたり、より優れた化学合成とコンピュータ支援設計により、インフルエンザ、B型・C型肝炎、HIV、そして最近ではSARS‑CoV‑2に対するより精密な薬が生まれました。本総説はこのタイムラインをたどり、各ブレークスルーがウイルスを出し抜く新たな手法をどのようにもたらしたかを示します。
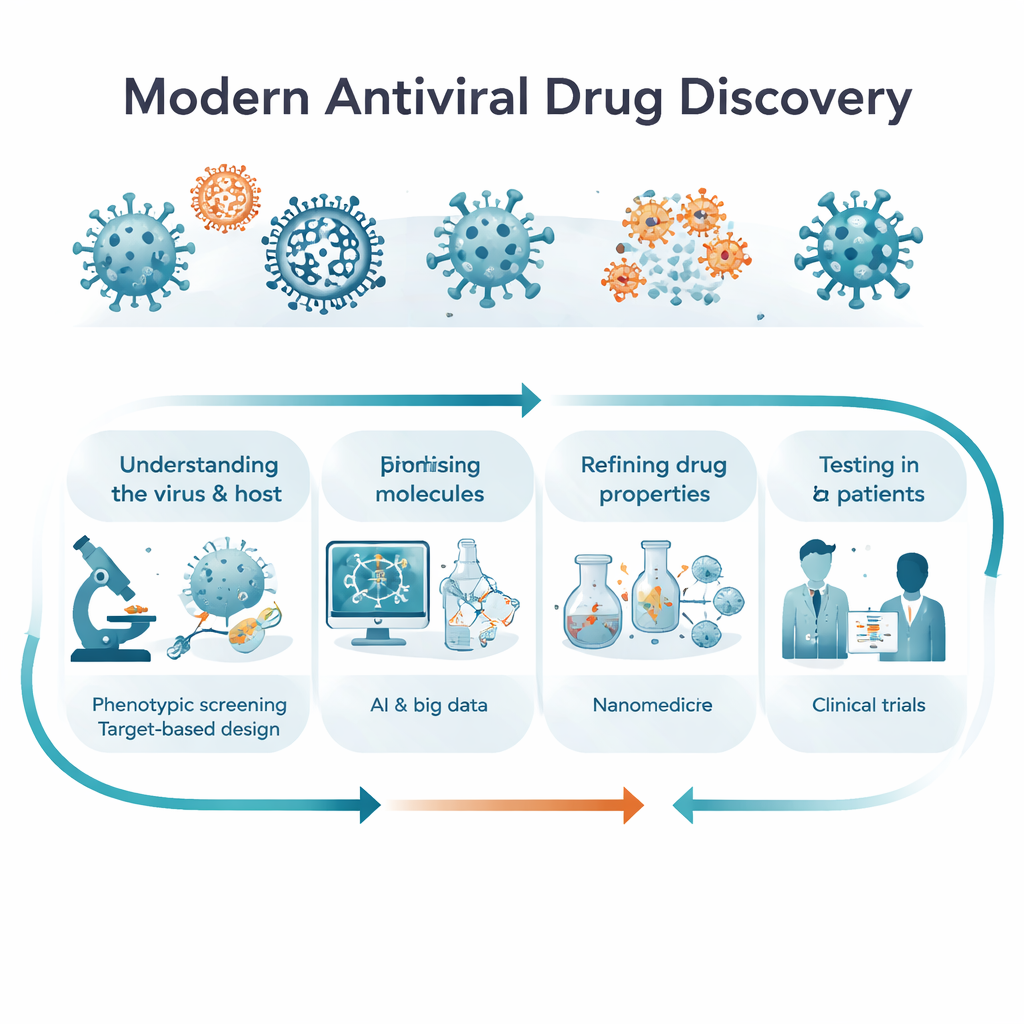
良い薬を見つける二つの方法:細胞を観察するか、標的を狙うか
研究者は一般に二つの補完的な道筋をたどって新たな抗ウイルス薬を探します。「フェノタイプ(表現型)ベース」の探索では、特定のタンパク質から始めるのではなく、感染した細胞やモデル生物に何千もの化合物を曝露して、どれがウイルスを抑え細胞を生かすかを単純に問います。これにより、複数の経路に作用するような驚くべき初のクラス薬が発見されることがあります。一方「ターゲットベース」の探索では、研究者はまずポリメラーゼやプロテアーゼ、免疫シグナルのような感染に不可欠なウイルスまたは宿主のタンパク質を同定し、その標的を阻害または調節する分子を設計します。記事はこれらの戦略がどう異なるか、研究の異なる段階でなぜそれぞれ重要か、そして将来のプロジェクトが幅広い観察から精密な分子理解へとスムーズに移行するために両者をどのように融合させる可能性があるかを説明します。
ウイルスとその支援システムの痛むところを狙う
現代の抗ウイルス薬は単に一つのウイルス酵素を塞ぐ以上の働きをします。本総説はウイルスのライフサイクルを、細胞への侵入からゲノム複製、放出までたどり、それぞれの段階を妨げる薬の種類を浮き彫りにします。ある化合物はウイルス酵素や構造タンパク質に直接結合します。別のものはウイルスが依存する宿主因子――細胞表面受容体や重要な代謝酵素、インターフェロンやトール様受容体のような自然免疫経路など――を標的にします。宿主の“補助”タンパク質に作用することで、急速に変異するウイルスが回避する可能性を減らせます。著者らはまた、ウイルスが組み立てられる細胞内の膜を伴わない“液滴”を破壊する小分子や、単に阻害するのではなく選択的にウイルスタンパク質やRNAを分解するような新しい発想も紹介しています。
より良い分子の設計:形状・特性・送達
初期の“ヒット”を有用な薬に転換するには、活性の最大化以上のことが必要です。化学者は分子の形状や電荷を調整して、鍵と錠のように標的に適合させ、しばしば高分解能のタンパク質構造やシミュレーションに導かれます。また水溶性、安定性、代謝特性を調整して、薬が適切な組織に到達し、十分な時間活性を保ち、不必要な毒性を避けられるようにします。記事は側鎖の追加や塩形成のような小さな変化が、耐性を持つHIVやコロナウイルス株に対する活性を高めつつ安全性を改善する事例を示します。さらに、前駆体薬(プロドラッグ)について、体内で変換されて活性化される不活性または低活性の形態としての役割や、肝臓を標的にする糖タグや不安定なmRNAや核酸薬を安全に細胞内へ運ぶ脂質ナノ粒子のような標的送達システムについても説明します。
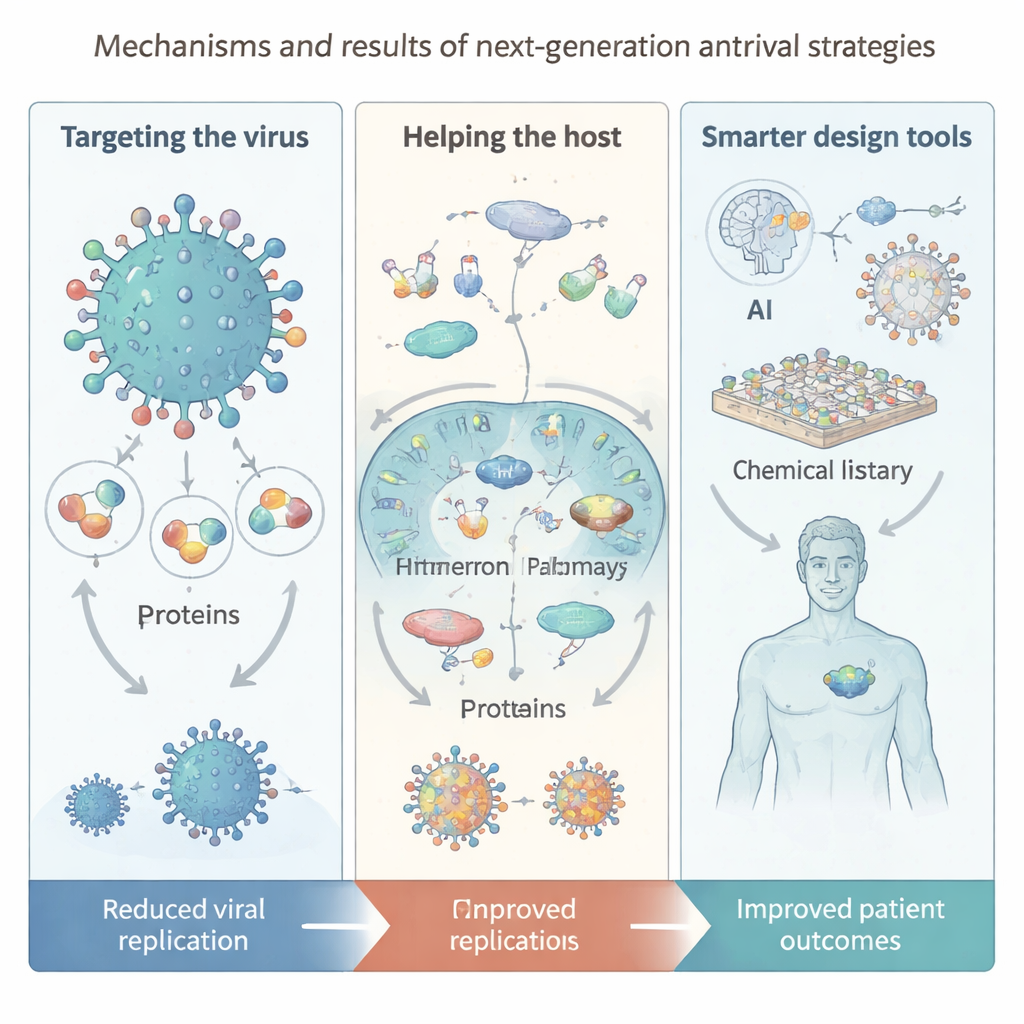
新しいツール:人工知能、巨大ライブラリ、ナノテック
本総説の主要なテーマの一つは、技術が抗ウイルス探索をどのように再形成しているかです。人工知能は現在、タンパク質構造の予測、何十億もの候補分子を含む「仮想」ライブラリの検索、新規化合物や薬物併用の提案を支援しています。DNAエンコードライブラリやマクロサイクリックペプチドプラットフォームは膨大な化学空間を超高速でスクリーニングでき、同時に自動合成・精製システムが構築と評価のサイクルを加速します。送達の面では、ナノテクノロジーがウイルス様粒子、スマートポリマー、ウイルス被膜を直接損傷したり免疫応答を鋭くしたりする“ナノザイム”を提供します。ただし著者らは、AIモデルが依然として高品質なデータに依存していること、多くの生成分子が合成や試験が難しいこと、そしてこれらのツールが中心的になるにつれて安全性、公平性、プライバシーの問題に対処する必要があると注意を促します。
抗ウイルス薬創薬の行く先
一般読者に向けた記事の主要なメッセージは、重く受け止めるべき点と希望です。ウイルスは速やかに変異し、一つの錠剤ですべての脅威に永続的に効くわけではありません。しかし、COVID‑19から学び、ウイルスと宿主の相互作用の理解を深め、スマートな化学、先端生物学、AI、ナノテクノロジーを組み合わせることで、科学者はより機敏な抗ウイルスの道具箱を構築しつつあります。将来の治療は範囲が広く、忍容性が良く、ウイルスだけでなく感染過程における脆弱な“弱点”を標的に合わせて設計される可能性が高いです。これらの科学的進展を次のパンデミックが来る前に手頃で実用的な医薬品へと変えるためには、分野横断的、産業界、国際間の継続的な協力が不可欠です。
引用: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
キーワード: 抗ウイルス薬の創薬, COVID-19治療薬, 宿主標的型抗ウイルス薬, 創薬における人工知能, 医療におけるナノテクノロジー