Clear Sky Science · ja
細胞傷害性CD4+ T細胞:起源、生物学的機能、疾患および治療標的
ヘルパー細胞がキラーに変わるとき
免疫系は通常、役割が簡潔に説明されます:ある細胞は問題を見つけ、別の細胞が実際に戦う。この論文はその線引きを曖昧にする驚くべき集団、すなわち細胞傷害性CD4 T細胞に焦点を当てます。長く「ヘルパー」細胞として防御を調整する役割で知られてきたCD4 T細胞の一部は、自ら武装したキラーになり得ます。こうした可変性を持つ細胞がどう生じ、何を行い、がん、ウイルス感染、自己免疫疾患、心疾患といった病態にどう寄与するかを理解することは、免疫を強化したり、有害な炎症を抑えたりする新しい道を開く可能性があります。 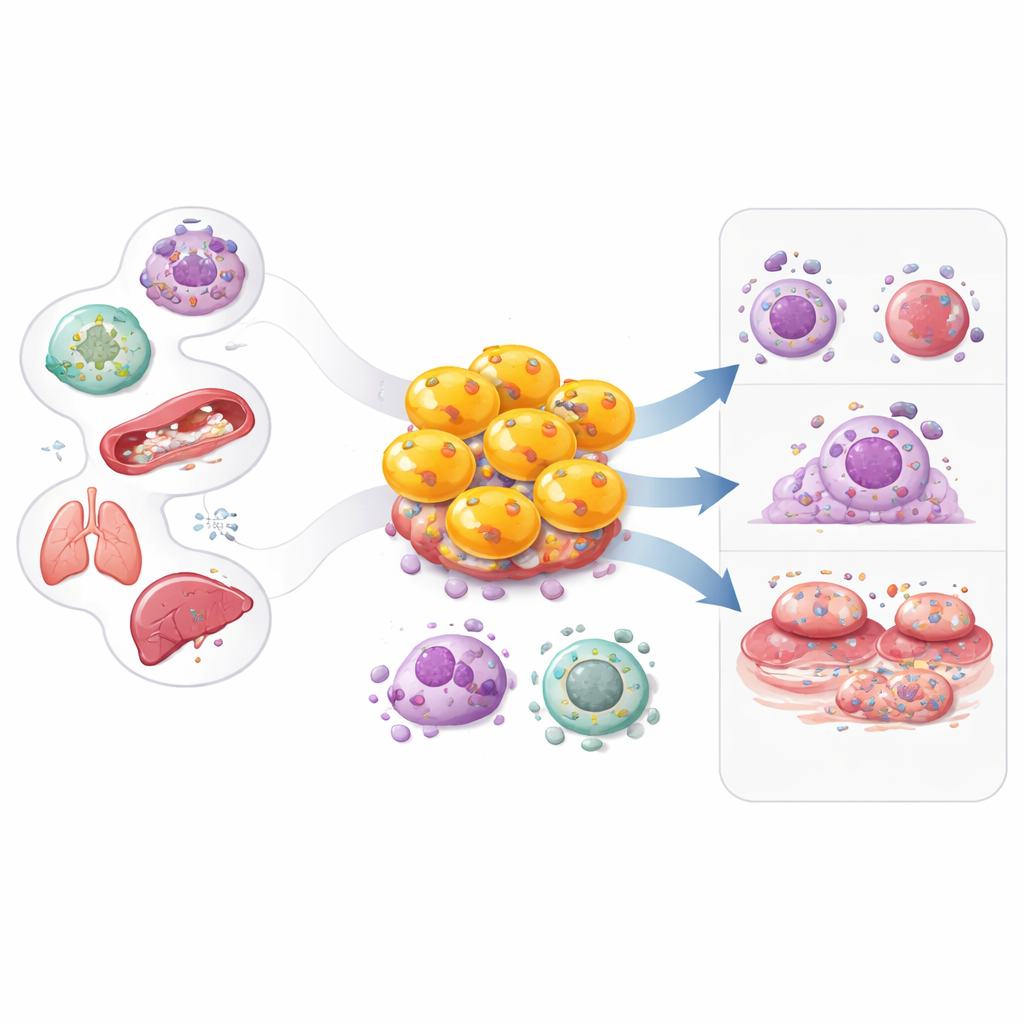
柔軟な防御者はどのようにして現れたか
1970〜80年代後半の初期研究は、CD4 T細胞の一部が、古典的なCD8「キラー」T細胞と同様に、適切な免疫フラグを示す細胞を直接殺せることを示しました。当初、多くの研究者はこれらの所見を培養実験の人工的産物として片付けました。しかし、その後の数十年にわたるインフルエンザの動物モデルや、関節リウマチ、心疾患、慢性ウイルス感染、がん患者での研究は、細胞傷害性CD4 T細胞が実在し臨床的に重要であることを確認しました。フローサイトメトリーや単一細胞RNAシーケンスなどの現代的手法によりその多様性が描き出され、これらの細胞が慢性感染、腫瘍、老化、いくつかの炎症性疾患で増殖し、長期間持続し得ることが明らかになりました。
これらのキラー・ヘルパーはどこから来るのか
総説では、細胞傷害性CD4 T細胞は主に二つの経路で生じると説明しています。一つの考え方は、これらがナチュラルキラー細胞によく似ており、多くの同じ表面受容体や細胞傷害性分子を共有しているため、関連する発生経路をたどるというものです。しかし、蓄積された証拠は別の見方を支持します:大部分は普通のヘルパーCD4 T細胞、特にTh1様の細胞として始まり、慢性的な抗原曝露や強い炎症シグナルの下で終末分化した細胞傷害性状態へと「再教育」されるという考えです。このシフトは、インターロイキン2、7、15などの外的シグナルと、Runx3、T-bet、Eomes、Blimp-1、Hobitといった内部の転写スイッチのネットワークによって制御され、パーフォリン、グランザイム、死を誘導するリガンドの遺伝子発現を立ち上げます。
彼らはどうやって殺し、炎症を形作るか
機能的には、細胞傷害性CD4 T細胞は主に二つの攻撃経路で作用します。顆粒経路では、標的細胞と密着してパーフォリンやグランザイムを含む顆粒を放出し、穴をあけて細胞内からプログラムされた細胞死を誘導します。死リガンド経路では、FasリガンドやTRAILのような分子を表面に提示し、標的細胞の対応する受容体と結合して内的な自殺プログラムを起動させます。直接的な殺傷に加え、これらの細胞はインターフェロンγ、腫瘍壊死因子、増殖因子などの炎症性メッセンジャーを大量に放出し、他の免疫細胞を呼び寄せ活性化し、血管を再構築し、局所組織の挙動を変えます。古典的なヘルパーとは異なり、制御性T細胞などの通常の“ブレーキ”に抵抗しやすく、アポトーシスに陥りにくいため、慢性疾患で蓄積することが多いです。 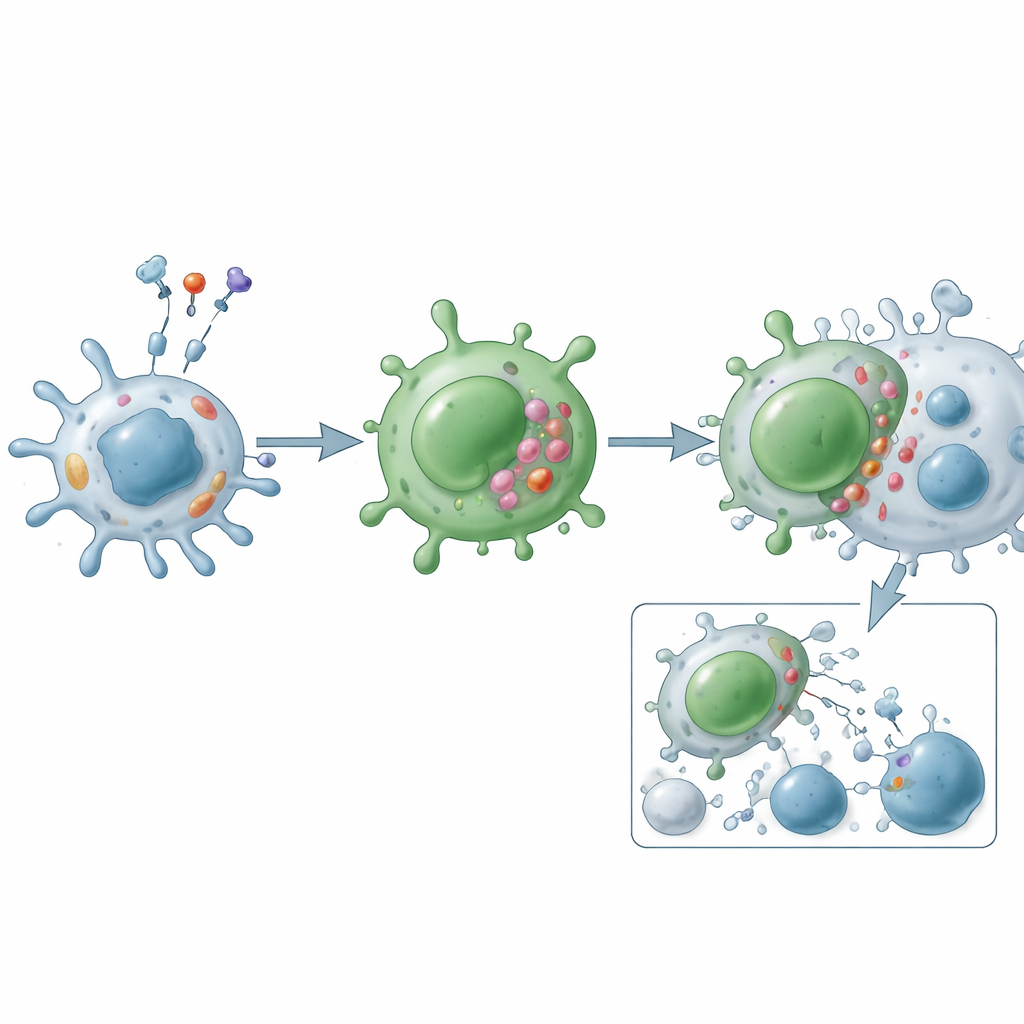
感染やがんでは味方、自己免疫や心疾患では敵
この両刃の振る舞いは多くの状況で見られます。慢性B型肝炎、HIV、COVID-19では、CD8キラーが疲弊している際に細胞傷害性CD4 T細胞がウイルス制御に寄与し、その存在はより良い制御や回復と関連することがあります。固形腫瘍や血液がんでは、適切な免疫マーカーやストレスシグナルを提示する腫瘍細胞を直接認識でき、チェックポイント阻害剤やCAR-T細胞治療などの免疫療法への反応を改善する可能性があります。一方で、同じメカニズムが有害に働く場合もあります:ループス、関節リウマチ、炎症性腸疾患、冠動脈疾患、心房細動、巨細胞性動脈炎、移植拒絶などでは、拡大した細胞傷害性CD4 T細胞が組織に浸潤し、血管や臓器を損傷し、長期にわたる炎症を増幅させ、しばしば予後悪化と相関します。
リスクのある道具を治療へ変える
細胞傷害性CD4 T細胞は保護的にも破壊的にもなり得るため、論文はこの集団を単に消すのではなく細かく調節することを目指した新興の治療戦略を強調します。一つのアプローチは、OX40や4-1BBのような共刺激受容体、炎症性サイトカイン、イオンチャネル、または生存経路を標的とする選択的阻害剤で有害な活動を抑える方法です。別の方法は、遺伝子改変T細胞やCAR-T細胞を含む養子細胞療法でその殺傷力を利用することで、CD4細胞由来の細胞傷害性T細胞はCD8のみの製品より長期持続することが多いと報告されています。第三の戦略は、長寿命でウイルス特異的なCD4キラーをワクチンや病原体由来のペプチドを介して腫瘍へ向け直すことを提案します。これらの研究は、細胞傷害性CD4 T細胞を単なる生物学的好奇心に留めず、感染やがんに対する防御をより精密に強化しつつ組織損傷性の炎症を軽減する将来の治療の中心的な手段として位置づけます。
将来の免疫療法の新たなレバー
専門外の読者にとっての要点は、「ヘルパー」CD4 T細胞はかつて考えられていたよりはるかに多才であるということです:一部は完全に武装したキラーに切り替わり、持続感染やがんから我々を守る一方で、自己免疫、血管損傷、移植拒絶を促進することもあります。総説は、これらの細胞を追跡し、いつ役立ちいつ害をなすかを予測し、薬剤や設計された療法でその振る舞いを調整する方法を学べば、肝炎やHIVから関節炎、結腸炎、心疾患、白血病に至る広範な慢性疾患の治療法を再構築できると主張します。免疫系を単に上げ下げするのではなく、将来の療法はこのような強力な細胞種、すなわち細胞傷害性CD4 T細胞を有益な標的へ向け、自己組織から遠ざけるよう操舵する方向へ向かう可能性が高いです。
引用: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
キーワード: 細胞傷害性CD4 T細胞, 免疫細胞の可塑性, 慢性炎症, がん免疫療法, 自己免疫疾患