Clear Sky Science · ja
臓器線維症の解読:メカニズムの洞察と新たな治療戦略
治癒が有害な瘢痕化に転じるとき
多くの人は瘢痕を皮膚の跡と考えますが、同様の瘢痕化プロセスが臓器内部を静かに変形させることがあります。本レビューは、肺、心臓、肝臓、腎臓で過剰な内部瘢痕化――線維症――がどのように進展するか、なぜ現在それが世界的な公衆衛生上の重大な脅威になっているか、そして新しい技術や治療法がいかにして医師がその進行を遅らせ、場合によっては逆転させる可能性を持つかを説明します。
臓器機能を脅かす瘢痕
線維症は損傷を修復しようとする体の試みとして始まります。損傷後、細胞はコラーゲンなどのタンパク質のメッシュを形成して弱った組織を補強します。損傷が軽度または短期であれば、このプロセスは収束して正常な構造が回復します。しかし、感染、毒素、高血圧、過剰な脂肪、免疫攻撃などで損傷が重篤または反復すると、修復システムが「オン」の状態に固定されてしまいます。密な瘢痕組織が蓄積し、臓器の構造を歪め、徐々に機能を奪っていきます。レビューは、世界人口の約4分の1が肺の特発性肺線維症から心不全、肝硬変、慢性腎臓病に至る線維化性疾患に影響されていると指摘しています。それでも現在承認されている薬剤はピルフェニドン、ニンテダニブ、レスメチロム、セマグルチドなどごくわずかで、既存の瘢痕を消失させるというよりは主に進行を遅らせるに留まります。
多様な細胞種、共通の有害な結果 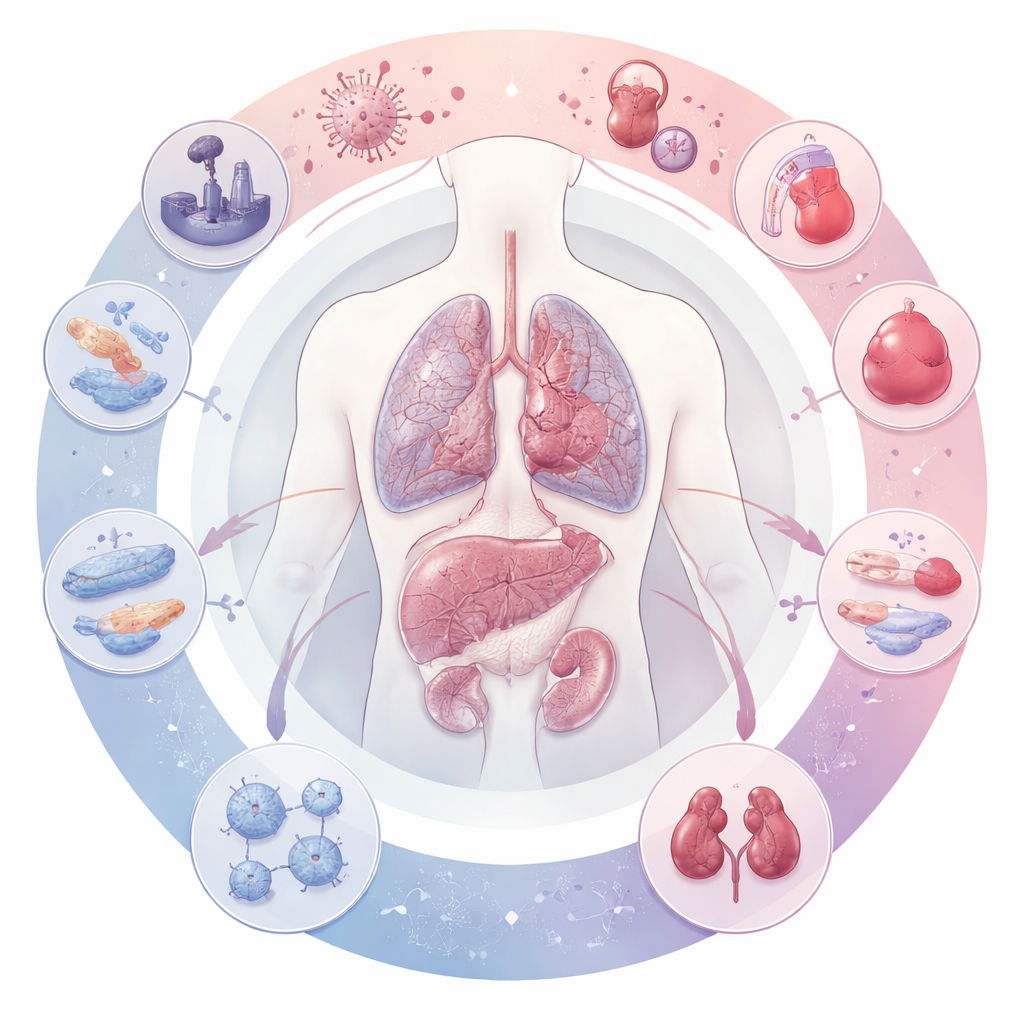
Figure 1.

かつて科学者は線維症を主に細胞外マトリックスを作る線維芽細胞のせいにしてきましたが、本記事は実態がはるかに複雑であることを示します。各臓器では、表面を覆う上皮細胞、血管内皮細胞、特定の免疫細胞などいくつかの細胞種が攻撃的な瘢痕産生細胞である筋線維芽細胞に変換し得ます。同時に、肺の肺胞細胞、心筋細胞、肝臓の肝細胞などの正常な実質細胞は専門的機能を失い、ストレスや老化状態になって危険信号を放出します。免疫細胞が集まり、炎症性および増殖因子を放出します。時間とともに、この絡み合った「線維化ニッチ」――変化した細胞、シグナル分子、硬化したマトリックスの網――が臓器を慢性的な損傷と瘢痕のループに閉じ込めます。
異なる臓器、共通のパターン
引き金は臓器ごとに異なりますが、瘢痕化の物語は類似したステップをたどります。肺では吸入粒子、ウイルス感染、放射線が繊細なガス交換面を傷つけ、通常は再生する細胞が半分治った状態で停滞して強い線維化シグナルを出します。心臓では心筋梗塞や長期の圧負荷が心筋細胞を死滅またはストレス状態にし、線維芽細胞が隙間を硬いコラーゲンで埋めて駆出能を損ない、電気伝導を乱します。肝臓では慢性ウイルス性肝炎、アルコール、脂肪過多が肝細胞を傷害し、肝板間に位置する星状細胞を活性化してコラーゲン製造機に変え、臓器内の血流を再配線します。腎臓では高いエネルギー依存性の尿細管細胞が毒素や低酸素に応答して死滅、老化、あるいは代謝の再プログラミングを起こし、それが免疫細胞の動員や血管周囲の線維芽細胞の活性化を招きます。これらの違いにもかかわらず、最終的な結果は驚くほど似通っており、血管の狭窄、構築の歪み、機能の進行性喪失が生じます。
シグナル回路と新興治療 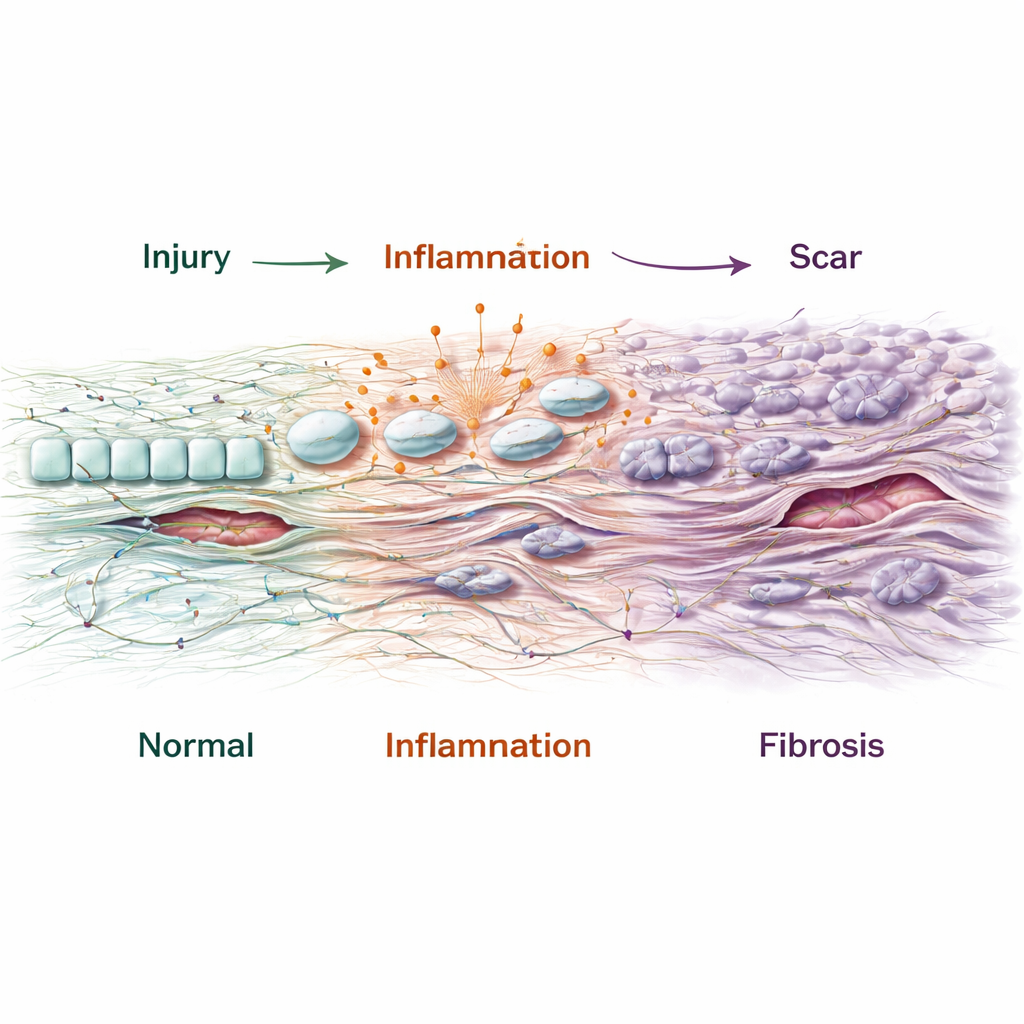
Figure 2.

こうした細胞ドラマの背後には共通のシグナル回路――線維症を継続させる生化学的な「配線図」――があります。レビューはTGF-β、Wnt/β-カテニン、MAPキナーゼ、JAK–STAT、PI3K–AKT、インテグリン、内質網ストレス応答などの中心的経路を強調しています。これらの経路は細胞の増殖、アイデンティティ変化、マトリックス分泌を支配します。多くの臓器で再利用されるため、これらを調節する薬剤は原理的に複数組織の線維症を治療し得ます。著者らはこれらの主要経路を標的とする多数の臨床試験中の実験薬――スモールモレキュール、抗体、受容体ブロッカー――に加え、FGF19やFGF21のような保護的ホルモンを模倣する生物学的治療を一覧化しています。さらに、キメラ抗原受容体(CAR)T細胞や過剰に活性化した線維芽細胞や星状細胞を選択的に排除するよう設計された改変マクロファージ、ナノ粒子で送達される遺伝子・RNAベースの戦略といったより急進的なアプローチも論じられています。
ビッグデータから個別化抗瘢痕薬へ
この記事の主要なテーマの一つは新しい研究ツールの力です。シングルセルシーケンシングと空間マッピングにより、研究者は病変臓器の個々の細胞を観察し、時間や場所による変化を追跡できるようになりました。マルチオミクスアプローチはDNA、RNA、タンパク質、代謝データを組み合わせて、様々な線維化疾患で繰り返し出現する特定の線維芽細胞、内皮細胞、マクロファージのような有害および保護的な細胞亜種を定義します。同時に、高度な臓器モデル――3Dオルガノイド、オルガンオンチップシステム、生体組織スライス――は実験室でヒト様の瘢痕化を再現し、より迅速で現実的な薬剤試験を可能にします。人工知能はこれらの複雑なデータセットで新しい薬剤標的を見つけ、分子を設計し、時には生検スライドを人より一貫して読み取るよう訓練されており、線維症の診断とモニタリングにおいてより客観的な手段を提供しています。
患者にとってこれが重要な理由
一般読者にとっての中心的メッセージは、線維症は漠然とした、回復不能な「摩耗」現象ではなく、測定可能でますます操作可能な特定の多段階プロセスだということです。正常な修復が暴走する共通のルールを解き明かし、関与する主要な細胞種や経路をマップすることで、研究者たちは症状の緩和を超える治療の基盤を築いています。著者らは、標的薬、細胞療法、AI支援診断を組み合わせて各患者の損傷と瘢痕形成のパターンに合わせて個別化する未来を想定しており、長期的な目標は単に線維症を遅らせることではなく、損なわれた臓器が真に回復するのを助けることにあります。
引用: Chen, X., Zhang, J., Guo, L. et al. Decoding organ fibrosis: mechanistic insights and emerging therapeutic strategies. Sig Transduct Target Ther 11, 82 (2026). https://doi.org/10.1038/s41392-025-02532-0
キーワード: 臓器線維症, 組織の瘢痕化, 慢性炎症, 抗線維化療法, シングルセルオミクス