Clear Sky Science · ja
IFFO1はLaminA/C–PGC1α軸を介してミトコンドリア分裂と脂肪酸合成を協調させ、乳がんを抑制する
この研究が重要な理由
乳がんは依然として女性のがん死因の主要な一つであり、腫瘍の一部は増殖と転移を続け、現行治療をすり抜けてしまいます。本研究は、IFFO1というこれまで見過ごされがちだった細胞内の“ブレーキ”を明らかにし、腫瘍成長の二つの中核エンジン――細胞のエネルギー工場であるミトコンドリアと、脂質を合成・蓄積する能力――を抑えることで乳がんを鈍らせることを示しました。このブレーキの理解は、複数の乳がんサブタイプに有効となり得る新たな治療アプローチの可能性を示唆します。
乳房細胞内に潜む守護者
研究者らは30名の乳がん患者からの試料と、大規模な公開がんデータベースを調べ始めました。その結果、IFFO1タンパク質の発現は腫瘍組織で周囲の正常乳組織より一貫して低いことが分かりました。病期が進むほどIFFO1は減少し、腫瘍でのIFFO1発現が高い患者は生存率が高い傾向がありました。培養した乳がん細胞でIFFO1を過剰発現させると、細胞の増殖、分裂、移動能力が大幅に低下し、腫瘍の拡大や転移に必要な挙動が抑えられました。さらにIFFO1は、がん細胞が脱落して他組織へ侵入するのを助ける上皮–間葉転換(EMT)という細胞プログラムも抑制しました。
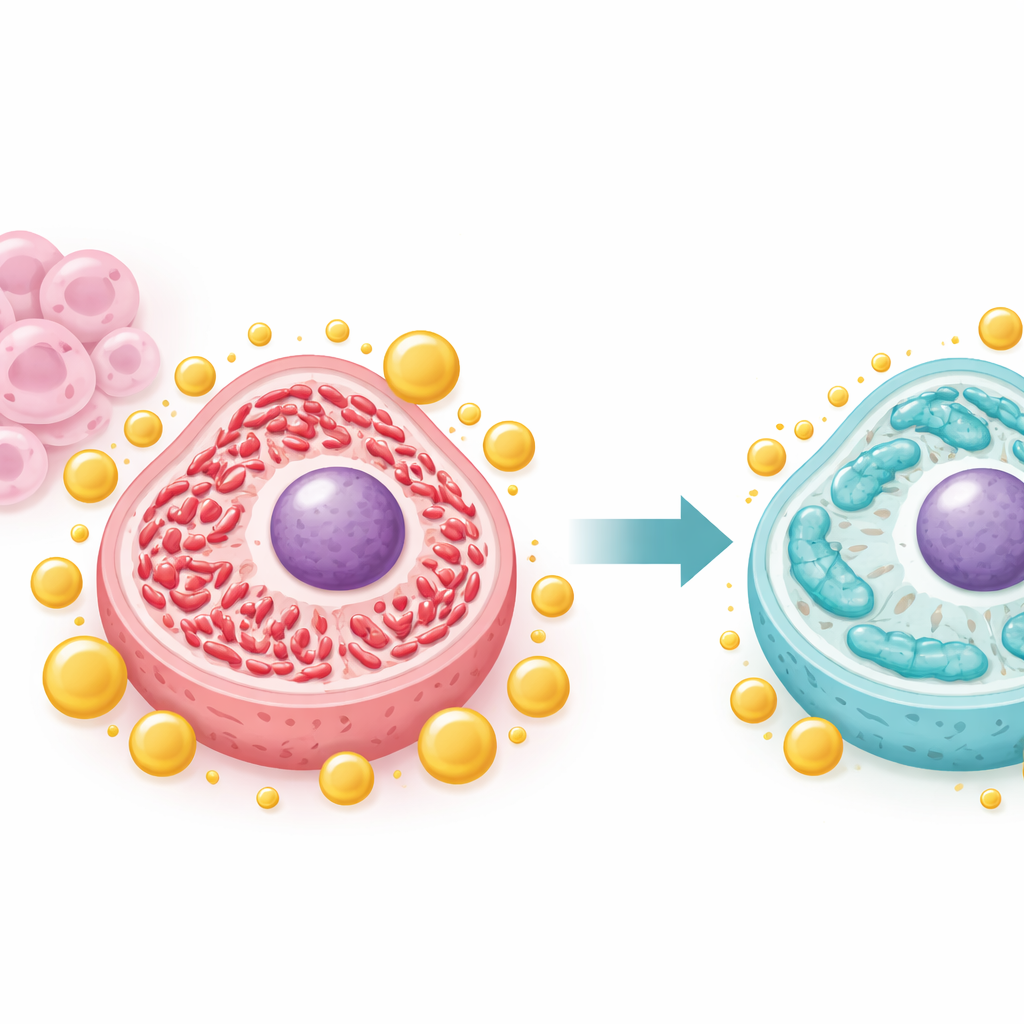
過剰に活性化したエネルギー工場を鎮める
がん細胞はしばしばミトコンドリアの形態を再編して急速な増殖を支えます。チームはIFFO1がミトコンドリアを高度に断片化した「分裂(fission)」状態から、より伸長した「融合(fusion)」状態へとシフトさせ、一般により健康で安定したミトコンドリアに関連する状態へ導くことを示しました。IFFO1が豊富な場合、Drp1やFis1などの分裂を促す主要タンパク質は減少し、融合を促すタンパク質は増加しました。顕微鏡観察ではミトコンドリアが長くなり断片化が減り、ミトコンドリアDNA量やエネルギー産出も攻撃的な細胞で見られる異常に高いレベルから低下しました。これらの変化は、IFFO1がミトコンドリアを制御不能な過活性状態に陥らせることを防ぎ、腫瘍の無制御な成長を支える構成を阻むことを示唆します。
脂肪の供給ラインを遮断する
急速に増殖する腫瘍はエネルギーだけでなく、新しい膜やシグナル分子を作るための脂質の安定供給も必要とします。本研究はIFFO1がこの代謝アクセルも抑えることを示しました。IFFO1を過剰に発現した細胞では、FASN、SREBP‑1、SCD1などの主要な脂質合成関連タンパク質が減少しました。酵素活性測定では脂肪合成活性の低下が確認され、化学的検査でも遊離脂肪酸、中性脂肪、コレステロールの減少が示されました。脂質を可視化する染料では脂肪滴の数や中性脂肪の総量が減少しました。逆に分裂促進タンパク質Drp1を増やすと脂質合成が促進され、Drp1をサイレンシングすると抑えられ、ミトコンドリア形態と脂質供給の間に直接的な結びつきがあることを支持しました。
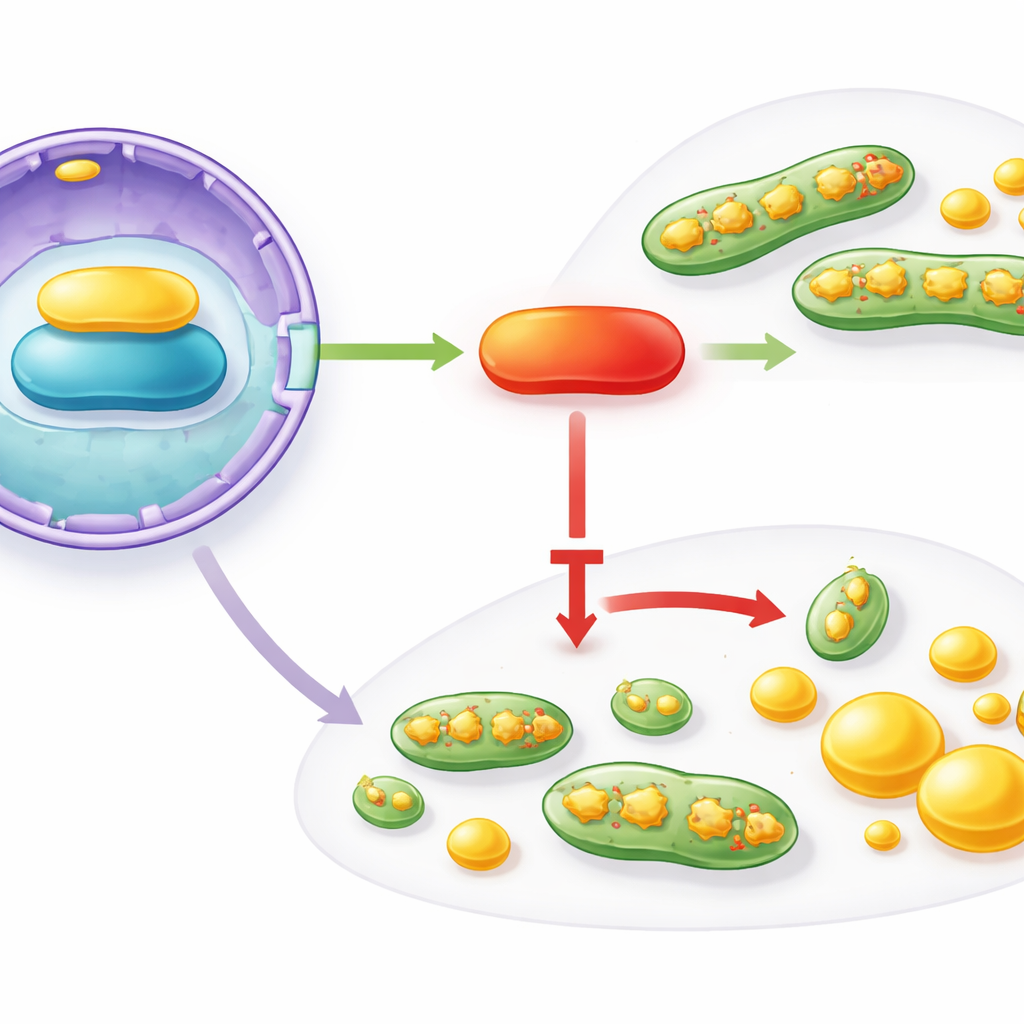
核からミトコンドリアへ至るシグナル連鎖
IFFO1はどのようにしてこれら広範な変化をまとめ上げるのか。著者らは、細胞核から出発してミトコンドリアと脂質合成機構に至る相互作用の連鎖を辿りました。IFFO1は核膜の構造タンパク質であるLamin A/Cに物理的に結合し、そのレベルを高めます。Lamin A/Cはミトコンドリアの健康と代謝を統括する主要制御因子PGC1αの活性を支えます。乳がん組織と細胞ではLamin A/CとPGC1αもIFFO1の減少を反映して低下していました。IFFO1を人工的に増やすとLamin A/CとPGC1αが上昇し、ミトコンドリアの分裂は減り脂質合成は弱まりました。Lamin A/Cをノックダウンするとこれらの利益は消えますが、PGC1αを回復させると再び戻り、IFFO1 → Lamin A/C → PGC1αという機能的な軸が腫瘍促進的なミトコンドリアと脂質の変化を抑えていることが示されました。
生体内でブレーキを試す
これらの細胞レベルの効果が実際の腫瘍に当てはまるかを検証するため、チームはIFFO1を付加したヒト乳がん細胞または付加していない細胞をマウスに移植しました。IFFO1を高発現する腫瘍は増殖が遅く、実験終了時の重量も軽く、脂肪蓄積の兆候が少なかったです。別のモデルでは癌細胞を血流に注入して肺転移を播種させると、IFFO1を過剰産生する細胞は肺の腫瘍結節の形成が著しく少なかったです。これらのマウス由来組織解析も細胞培養の所見を反映し、Lamin A/CとPGC1αの上昇、ミトコンドリア分裂の低下、脂質合成の減少が確認されました。
将来の治療への意味
総じて、本研究はIFFO1を細胞の構造的足場、エネルギー工場、脂質合成機構を結び付ける多層的な腫瘍抑制因子として提示します。IFFO1はLamin A/Cを安定化しPGC1αを増強することで、ミトコンドリアの過度な断片化を抑え、がん細胞が依存する脂質の過剰生産を断ち切ります。一般向けの要点は、このタンパク質が乳がんの成長と転移を支える「エネルギー」と「材料」の両方に対する内在的なブレーキの役割を果たしているということです。IFFO1の発現を高める薬剤や、Lamin A/C–PGC1α経路に対するIFFO1の作用を模倣する治療薬は、特に侵襲性や治療抵抗性の高い乳がんに対する新たな選択肢を将来的にもたらす可能性があります。
引用: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
キーワード: 乳がん, ミトコンドリア動態, 脂肪酸合成, 腫瘍代謝, PGC1α経路