Clear Sky Science · ja
ヌクレオチド合成に対する発がん性制御
なぜがん細胞は「構成要素」を重要視するのか
がんはしばしば「分裂を止めない細胞」と表現されます。しかし自己複製するには、これらの細胞はDNAやRNAを構成し多くの細胞プロセスのエネルギーにも関わる小さな構成要素、ヌクレオチドを絶えず供給される必要があります。本総説は、発がん遺伝子がどのように細胞の化学経路を書き換えてヌクレオチド生産を高めるか、腫瘍がこれらの分子を得る異なる経路をどう切り替えるか、そして医師が旧来の薬と新しい薬でこれらのトリックをどのように利用できるかを説明します。
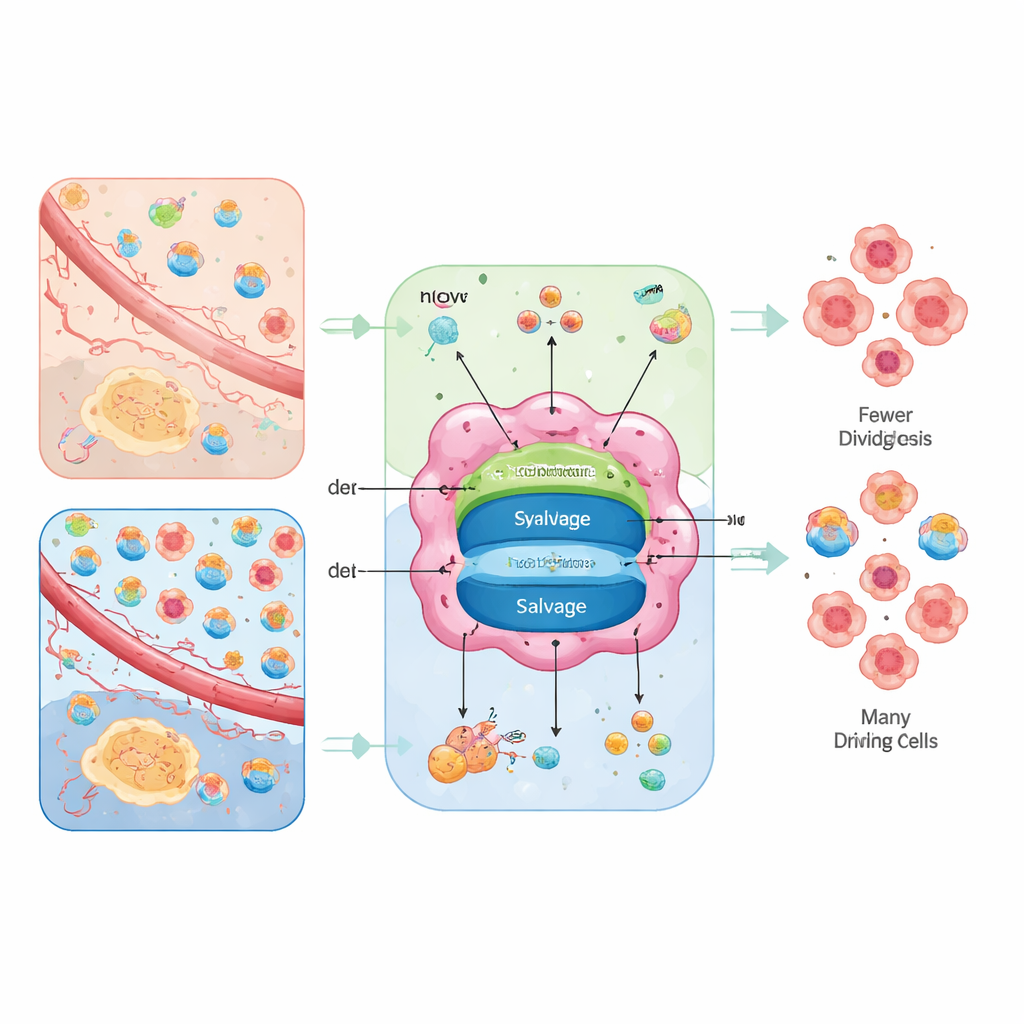
同じ構成要素へ向かう二つの道
細胞はヌクレオチドをゼロから合成することも、回収して再利用することもできます。「ゼロから」の経路はde novo合成と呼ばれ、グルコース、アミノ酸、二酸化炭素、重炭酸塩などの基本栄養素から環状構造を組み立てる、多段階でエネルギーを大量に消費する反応を経ます。一方、サルベージ経路は壊れた塩基やヌクレオシドを外部や細胞の廃棄物から取り込み、はるかに低いエネルギーコストで再生します。腫瘍は両方の選択肢を利用しますが、その比率は内部のエネルギー供給と周囲組織が何を提供するかに依存します。
腫瘍環境が選択をどう左右するか
著者らはヌクレオチド供給を「環境に形作られるルーティング」問題として位置づけます。アミノ酸はあるが遊離ヌクレオシドが乏しい栄養不足の領域では、がん細胞はde novo経路に大きく依存し、これらの段階を阻害する薬に脆弱になります。血流が良くヌクレオシドを十分に供給する領域やミトコンドリア機能が弱い領域では、腫瘍はサルベージに頼ることができ、ヌクレオシドの取り込みを阻むトランスポーター阻害剤に感受性を示します。両方の選択肢が使えると腫瘍は代謝的柔軟性を示して単剤を回避しますが、両方が閉ざされるとDNA複製が停滞し損傷が蓄積して細胞死やより分化した、攻撃性の低い状態への移行が起き得ます。
ヌクレオチド供給を支える隠れた回路
ヌクレオチド工場を稼働させ続けるにはいくつかの補助回路が必要です。ペントースリン酸経路は糖の骨格と還元力を供給し、グルタミンやミトコンドリアのエネルギー産生サイクルは窒素とアスパラギン酸を提供します。セリン、グリシン、葉酸の化学は環を完成させる1炭素単位を供与し、重炭酸塩が必要な炭素を導入します。PI3K–AKT–mTORC1、RAS–MAPK、MYCといったがんドライバーはこれらの経路を総動員し、主要酵素を増強し、不安定な中間体を効率的にチャネルする多酵素クラスターを組み立てることさえあります。対照的に、LKB1–AMPKやp53のようなストレスセンサーは通常ブレーキとして働き、エネルギー不足やDNAの健全性が脅かされるとヌクレオチド産生を抑えますが、これらのブレーキは多くの腫瘍で無効化されています。
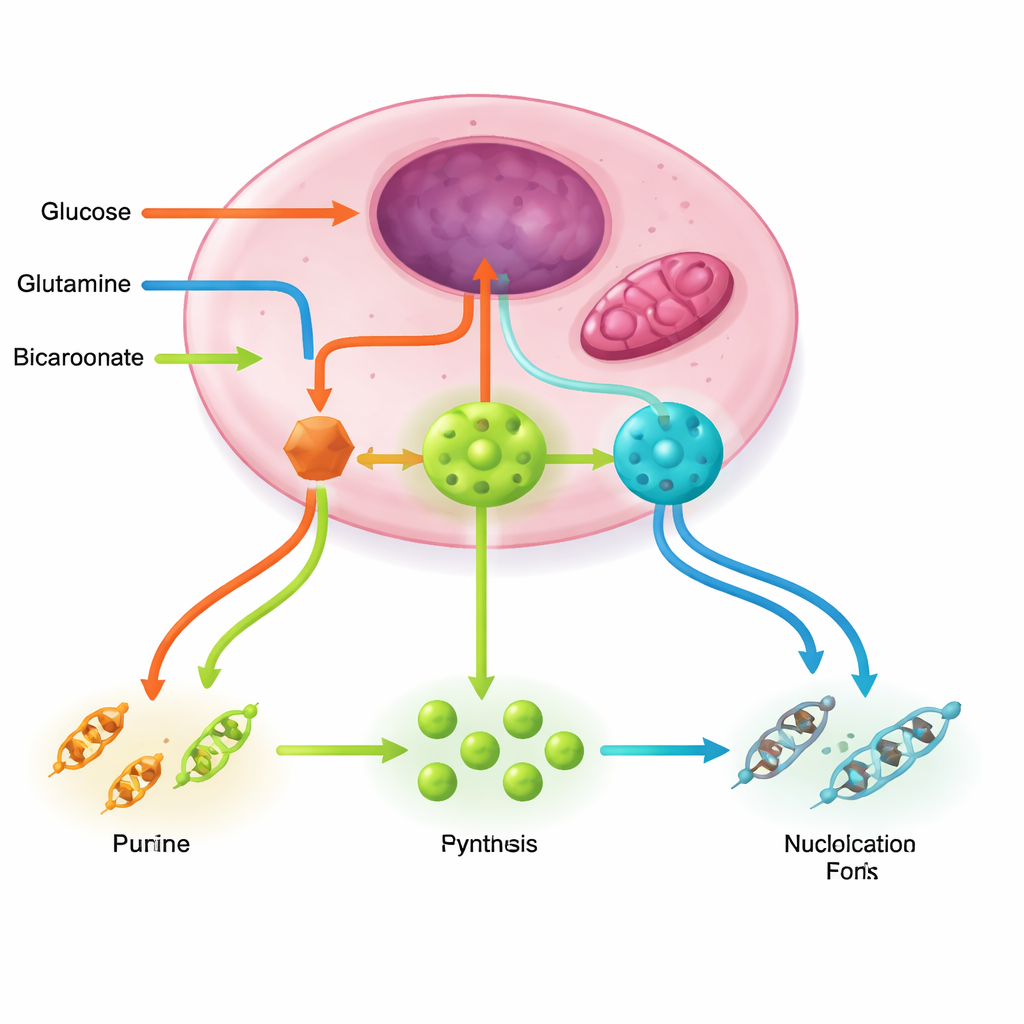
古い化学療法、新しい代謝ロジック
増殖の速い細胞はヌクレオチドに強く依存するため、初期の化学療法のいくつかはこの弱点を標的にしました。メトトレキサート、5‑フルオロウラシル、シタラビン、ジェムシタビン、各種プリン類似体といった古典的薬は、葉酸の利用を阻害するか、特定酵素を阻害するか、あるいは不良な構成要素としてDNAやRNAを毒することで作用します。本総説はこれらの薬をルーティングモデルの観点から見直し、副作用や耐性が一般的である理由を説明します:非がん組織もヌクレオチドを必要とし、腫瘍はひとつのノードが塞がれるとサルベージや並列経路を介してフラックスを迂回できることが多いのです。
次世代戦略と残された疑問
新しいアプローチは、ネットワークのがん特異的な部分を狙うことでより選択的であろうとしています。実験的薬剤はMTHFD2のようなミトコンドリアの1炭素酵素、ピリミジン酵素DHODH、IMPDHやPAICSのようなプリン酵素に対して開発中であり、多くはサルベージのトランスポーターも同時に阻む組み合わせで検討されています。著者らは、どの腫瘍がde novoかサルベージに依存するかを判断し、患者を経路標的療法に結びつけるための実用的マーカー—トランスポーターの発現レベル、血管密度、ミトコンドリアの健全性、特定の代謝酵素の発現など—を提案します。今後の課題としては、実際の腫瘍内でこれらの経路が時間と空間でどう変化するか、周辺の免疫細胞や間質細胞がヌクレオチドの利用可能性をどう形作るか、そして正常組織を圧倒せず複製ストレスを利用する耐容性のある投薬スケジュールをどう設計するかが挙げられます。総じて、本研究はヌクレオチド代謝の理解と標的化が細胞分裂の基礎的要求をがんに対する強力で個別化された手段に変え得ると主張しています。
引用: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
キーワード: ヌクレオチド代謝, がん代謝, de novo 合成, サルベージ経路, 代謝療法