Clear Sky Science · ja
新規のK6–K14ケラチン融合が誘導する細胞骨格の再編はcGAS–STING選択を介して癌の幹性と細胞可塑性を促進する
形を変えるがん細胞はどのように周囲を出し抜くか
がん細胞は単に異常増殖するだけでなく、生き残り、隠れ、転移するために自らの内部「骨格」を曲げたりねじったりする術を身につけます。本研究は、頭頸部がん細胞の内部に生じた特定の構造的な不具合がどのように核を破壊し、内在する危険アラームを作動させ、休眠状態に導き、最終的により攻撃的で浸潤性の高い幹様性を持つ細胞として復活させるかを明らかにします。この機械的なルートで進行するがんの進化を理解することは、再発や転移を阻止する新たな手段につながる可能性があります。
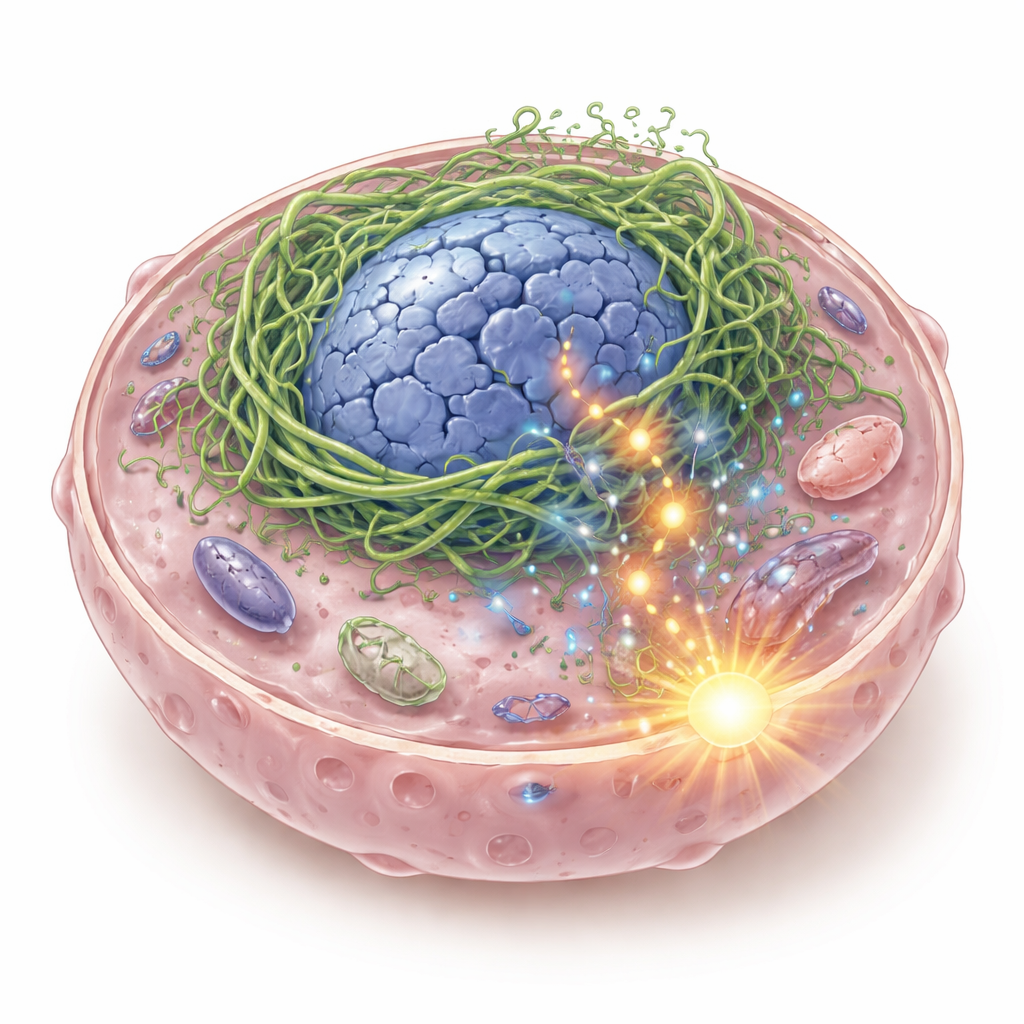
危険をはらむ壊れた内部足場
すべての細胞内には、細胞や核の形を保ち、物理的な力を感知する柔軟な足場がタンパク質フィラメントで作られています。著者らは、口腔や咽頭を含む上皮組織で一般的な足場タンパク質群であるケラチンに着目しました。頭頸部扁平上皮がんの一部では、2つのケラチン遺伝子が融合してできたK6–K14/V5というハイブリッドケラチンが見つかりました。この融合タンパク質ががん細胞で発現すると、滑らかな支持ネットワークを作るのではなく、核の周囲に強く凝集して核を空洞化し歪め、DNA切断を引き起こします。断片化したDNAは細胞質へ漏れ出し、通常ウイルスDNAの存在を検知して警報を鳴らす免疫検知系であるcGAS–STINGによって感知されます。
細胞死の圧力から隠れた生存へ
この核損傷の即時の影響はがん細胞にとって有害で、増殖は遅くなり多くが死にます。しかし一部は生き延びます。生存した細胞は物理的な周囲の影響を強く受けます。標準的な平坦なプラスチック培養皿ではそれらは徐々に消失しますが、実際の組織の質感に近い柔らかいコラーゲンゲル中で育てると持続し、新しい集団(3D‑V5細胞)として再出現します。遺伝子発現解析は、これらの細胞が継続するDNA損傷アラームに応答してオートファジー、つまり損傷部位や不良ミトコンドリアをリサイクルするセルフクリーニングプログラムを活性化することを示します。この反応により、彼らは除去される代わりに低活動の休眠状態に入ってストレスに耐えることができます。
休眠細胞は配線を変えて移動に備える
休眠中、これらの生存細胞は静かに内部プログラムを書き換えます。ケラチンタンパク質の組成を変え、「部分的」な上皮–間葉転換(pEMT)状態という中間的なアイデンティティを採り、いくつかの上皮特性は保ちつつ柔軟性と運動性を獲得します。彼らは球状形成や新しいクラスターを種をまく能力、すなわち癌の幹性の指標を著しく高めます。時間とともに機械的性質は回復し、核を再び硬化させ、強いアクチン繊維を再構築し、周囲のマトリックスを探り掴む長い突起を発達させます。またマトリックスメタロプロテアーゼ(MMP)と呼ばれる酵素を増やし、細胞外の網目を分解して浸潤の道を切り開きます。
支持的ニッチを作るために隣接細胞と対話する
これら再プログラムされたがん細胞は単独で行動するわけではありません。研究チームは、3D‑V5細胞が大量の小さな小包である細胞外小胞(extracellular vesicles)を周囲に放出することを観察しました。これらの小胞が近傍の口腔線維芽細胞に作用すると、線維芽細胞の遺伝子活動が変化し、腫瘍の成長を支持するがん関連線維芽細胞のような状態になります。やり取りされるシグナルの多くは増殖因子とその受容体からなるFGF–FGFR軸に関連しており、これが細胞増殖、可塑性、抵抗性を駆動することが知られています。培養系およびマウス腫瘍モデルの両方でFGFR活性を阻害するとこの増殖優位性は低下しました。動物では、3D‑V5細胞由来の腫瘍は分化度が低く、より浸潤性が高く、幹細胞マーカーが豊富で、注入部位から広がる傾向が強いことが示されました。
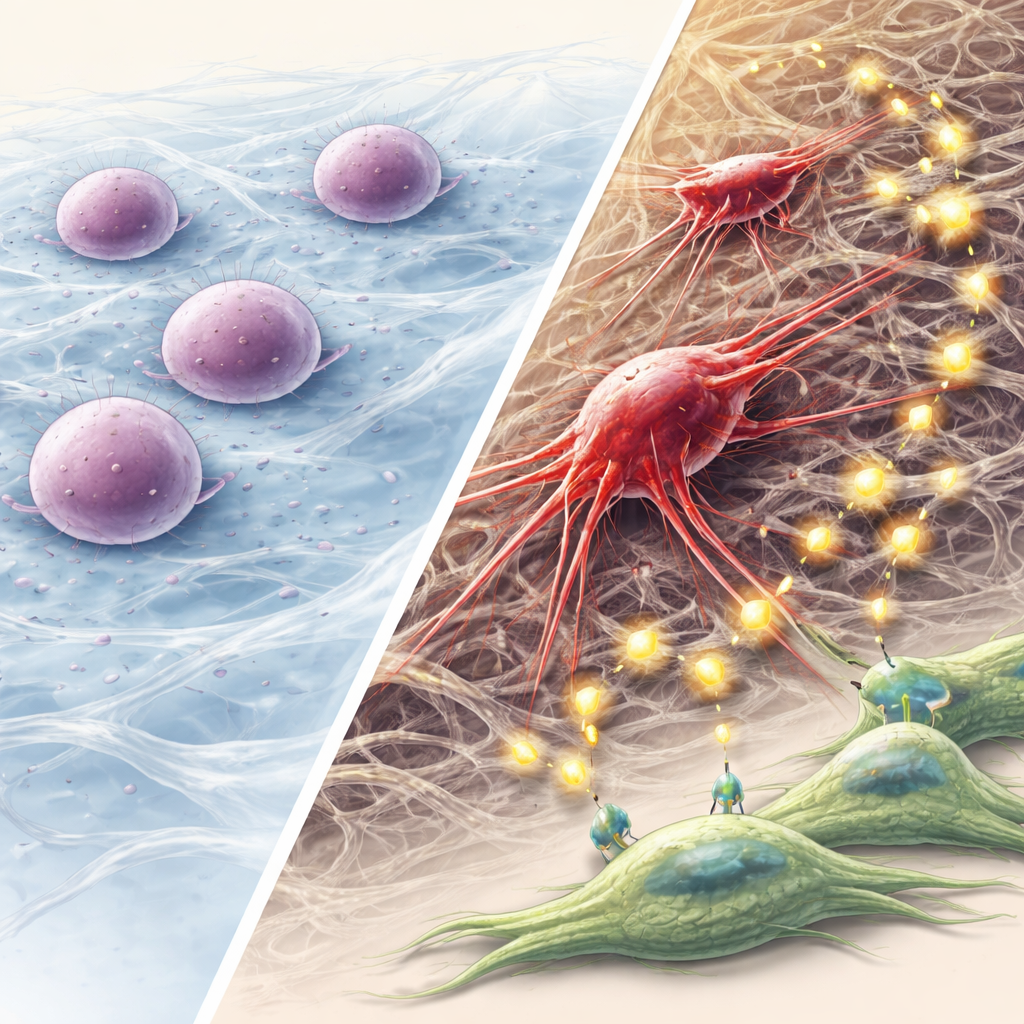
この機械的経路が攻撃的ながんで重要な理由
本研究は段階的モデルを提示します:ケラチン融合が細胞の内部足場を乱し、核を圧迫してDNA損傷アラームを作動させる;オートファジーにより一部の細胞は死ぬのではなく休眠に入る;時間とともにこれらの生存者は骨格を再編成し、幹様性と浸潤性を獲得し、小胞やFGFシグナルを通じて周囲の環境を再構築する。非専門家向けの核心メッセージは、細胞内部の物理的力や構造タンパク質が、遺伝子や化学物質と同じくがんの進化を左右する重要因子になり得るという点です。特にケラチン融合を持つ頭頸部がんにおいて、この機械的ストレス–オートファジー–FGF経路を標的にすることは、休眠した腫瘍細胞が再覚醒して拡散するのを防ぐ新たな戦略を提供する可能性があります。
引用: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
キーワード: 癌の幹性, 細胞骨格, 腫瘍休眠, 頭頸部癌, 機械的シグナル伝達