Clear Sky Science · ja
ヒストン脱メチル化酵素PHF2がSRXN1を制御することで肝細胞癌の腫瘍抑制因子として果たす役割
この肝臓がん研究が重要な理由
肝臓がんは世界で最も致命的ながんの一つであり、現行の薬剤は多くの患者で寿命をわずかに延ばすにとどまります。本研究は別の問いを立てます:従来のがんドライバー遺伝子を標的にするのではなく、肝細胞内でDNAがどのように収納され化学的にマーキングされているかを利用して、より精密な治療法を見つけられないか。研究者たちはPHF2というあまり知られていないタンパク質に注目し、それが肝細胞ががん化するのをどのように防いでいるかを解き明かします。
がんの制御システムの弱点を探す
がんは単に遺伝子の破綻だけで駆動されるわけではなく、どの遺伝子がオン・オフされるかを決める化学的タグやタンパク質複合体といった「エピジェネティック」な制御の異常にも支えられています。肝細胞癌では、多くのこうした調節因子が乱れています。研究チームは497種類のエピジェネティック調節因子を6つの肝がん細胞株で系統的に検査し、RNAを用いて各因子を一時的に減らしながらがん細胞の生存能を測定しました。この大規模スクリーニングは、がんが成長するために依存している調節因子と、本来腫瘍形成にブレーキをかける因子を明らかにすることを目的としています。
新たながん促進因子と保護因子の発見
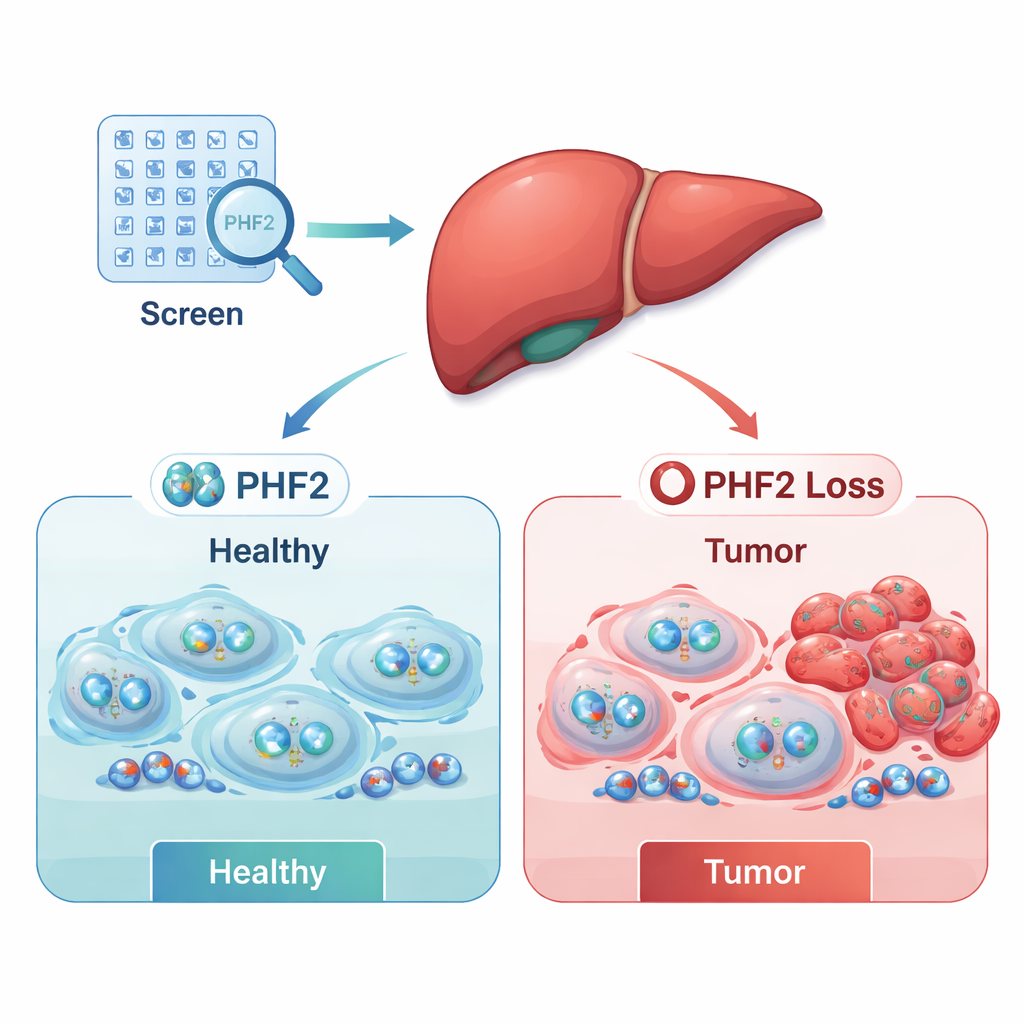
スクリーニングは大きく二つのグループを明らかにしました:欠失するとがん細胞の生存が損なわれる潜在的な“加速因子”(オンコジーン)と、欠失するとがん細胞の成長が促進される潜在的な“ブレーキ”(腫瘍抑制因子)です。実験データを大規模な公開患者データセットと組み合わせることで、臨床的に重要な候補を絞り込みました。SUPT7LやSMARCC1という二つの調節因子は腫瘍で活性が高く、予後不良と関連していました。対照的にPHF2は肝腫瘍でしばしば発現が低下しており、腫瘍でPHF2レベルが高い患者は一般に生存期間が長い傾向がありました。これらのパターンは、PHF2がヒトの肝臓がんにおいて腫瘍抑制因子として働く可能性を示唆します。
PHF2喪失が肝がん細胞に与える変化
PHF2をさらに詳しく検証するため、チームはPHF2の産生を安定的に低下させた肝がん細胞を作製し、その挙動を時間を追って観察しました。PHF2が減少した細胞は増殖が速く、細胞分裂の活性マーカーであるKi-67のレベルが高くなり、PHF2は通常増殖を抑える働きをしていることが示されました。これらの効果は特にすでに攻撃性の高い肝がん細胞株で顕著であり、PHF2の喪失自体が単独でがんを発生させるわけではないものの、腫瘍が形成された後に悪性細胞の増殖を加速し得ることを示唆しています。
細胞のストレス防御との意外な関連
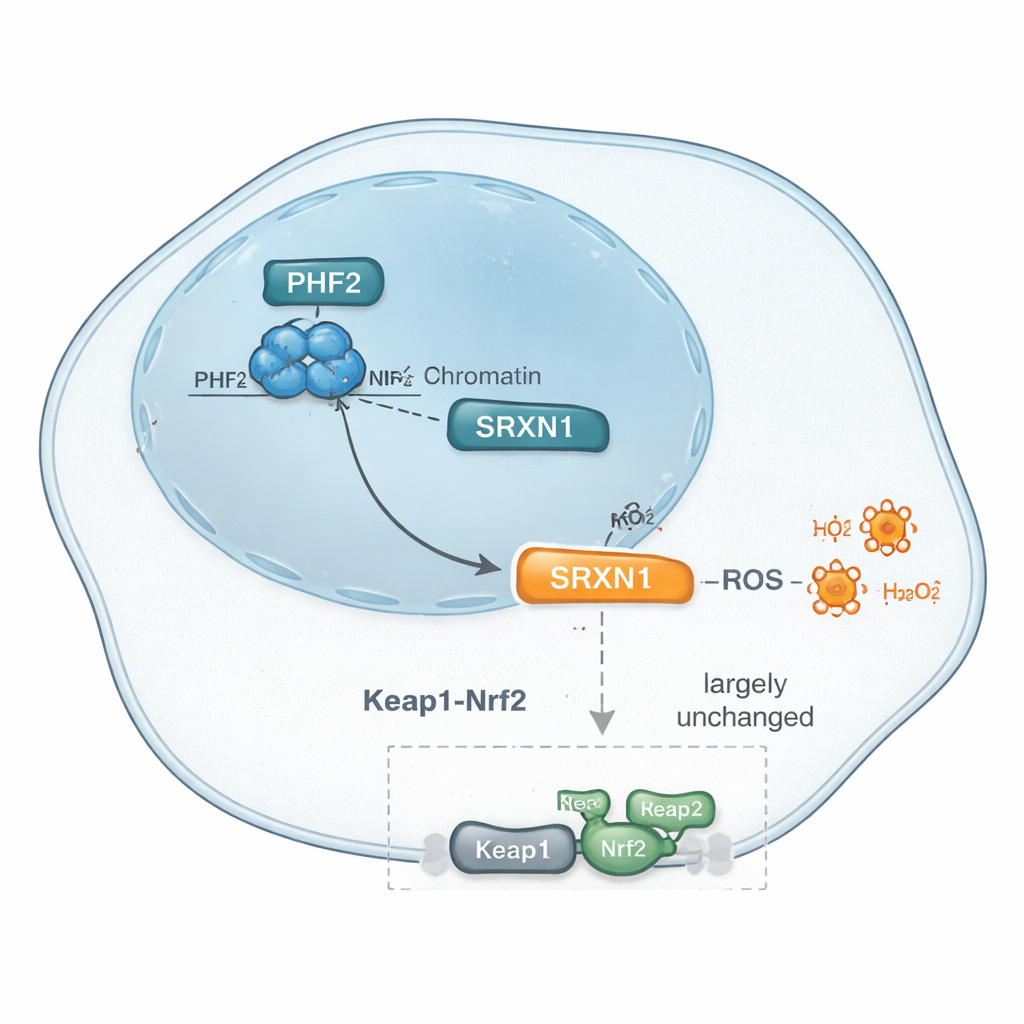
次に研究者たちは現代的なタンパク質プロファイリング法を用いて、PHF2が低下したときにレベルが変化する何千ものタンパク質を網羅的にカタログ化しました。多くの微妙な変化の中で際立ったパターンが一つありました:SRXN1というストレス保護タンパク質のレベルがPHF2喪失時に一貫して低下していたのです。SRXN1は活性酸素種のような化学的に反応性の高い副産物の管理に寄与し、これらはDNAやタンパク質を損傷する一方でがん細胞の適応を促すこともあります。データはPHF2がSRXN1レベルの維持に寄与しており、このバランスの変化が肝がん細胞の内部ストレスへの応答や最終的には増殖速度に影響を与える可能性を示唆します。
よく知られたストレス経路とは別に働く
SRXN1は通常、酸化ストレスに直面した際に多くの抗酸化遺伝子をオンにするマスター・ストレス応答スイッチであるNrf2によって制御されます。PHF2抑制でSRXN1が低下したことから、PHF2は単にこのよく知られたNrf2経路を介して働いているのではないかと研究者たちは問いかけました。彼らは主要なNrf2関連遺伝子とタンパク質を調べ、Keap1(Nrf2の抑制因子)を阻害してNrf2を活性化する薬剤で処理し、遺伝学的手法でKeap1を直接減らす試験を行いました。これらの試験を通じて、PHF2欠損細胞の応答は正常細胞のそれと大きくは変わらず、経路全体や転写因子解析でもNrf2が主要なプレーヤーとして浮上しませんでした。代わりに、ZNF384やNrf1など、いずれも肝がんと関連が報告されている他の因子が候補として挙がりました。総じて、PHF2がSRXN1や抗酸化応答を制御する仕組みは古典的なNrf2シグナリングを迂回する可能性があり、これら腫瘍における別個のストレス制御経路を示唆しています。
将来の治療への示唆
専門外の方への要点は、本研究がPHF2を肝臓がんにおける有望な保護因子として同定したことです:PHF2が存在し活性化されていると腫瘍細胞の増殖は遅くなり、PHF2が低下すると増殖優位が生まれ細胞のストレス処理の仕方が変わります。PHF2自体は従来の低分子薬で阻害または活性化するのが難しい可能性があるため、著者らはRNAベースの治療法や上流のシグナル伝達パートナーを介してPHF2の活性を高める薬剤など、新たな戦略を示唆しています。またPHF2の効果は文脈依存的であり—例えばp53などの他の変異とともに影響が異なる—将来の治療では患者選択が重要になると強調しています。総じてこの研究は、エピジェネティックな調節因子が肝臓がんの振る舞いをどのように形作るかに対する理解を洗練し、PHF2の腫瘍抑制的な影響を回復または模倣する治療設計の新たな道を開きます。
引用: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
キーワード: 肝細胞癌, エピジェネティック制御, PHF2, SRXN1, 肝臓がん治療