Clear Sky Science · ja
TRIM21を介したHILPDAの分解はPD‑L1のパルミトイル化を抑えて乳がんにおける抗PD‑1免疫療法の抵抗性を克服する
なぜ一部のがん免疫療法は効かなくなるのか
免疫を解き放つ薬剤、たとえば抗PD‑1療法は、侵襲的な乳がんを含む複数のがん治療を変革しました。しかし多くの腫瘍は最初から反応しないか、やがて回避策を見つけます。本研究はトリプルネガティブ乳がんにおけるそのような回避経路の一つを掘り下げ、腫瘍の脂質代謝を組み替えることと、既存薬のフェンレチニドを用いることで、標準的な免疫療法が効かなくなった場合でも免疫を再び有効にできる可能性を示しています。 
腫瘍を守る見えない助手
研究者らはHILPDAと呼ばれるあまり知られていないタンパク質に着目しました。これは以前より細胞がストレス下で脂肪を扱う仕組みに関係するとされてきました。抗PD‑1療法に感受性を保ったマウス乳腫瘍と抵抗性を獲得した腫瘍を比較すると、抵抗性腫瘍ではHILPDAの発現が著しく高いことが分かりました。大規模な患者データベースや乳がん患者の腫瘍サンプル解析でも、HILPDAは正常な乳組織より腫瘍でより多く存在し、特にトリプルネガティブ病変で顕著であり、HILPDA発現が高い患者は予後が悪い傾向にあることが確認されました。PD‑1阻害薬の恩恵を受けなかった患者の腫瘍でもHILPDAが多く認められ、このタンパク質が治療失敗に直結していることを示しています。
腫瘍が免疫環境を利用する仕組み
HILPDAが腫瘍内で実際に何をしているかを調べるため、研究チームは乳がん細胞をHILPDAを過剰発現させるか欠失させるよう改変し、それらをヒト免疫細胞と共培養するかマウスで増殖させました。HILPDAが高いと、腫瘍は制御性T細胞、骨髄由来抑制細胞、M2様マクロファージといった攻撃を弱める免疫細胞をより多く惹きつけました。同時にキラーCD8 T細胞やナチュラルキラー細胞の数と活性は低下し、毒性分子や炎症性シグナルの放出能も抑えられました。HILPDAを沈黙させると状況は逆転し、抑制的な細胞が減り、活性化したキラー細胞が増え、腫瘍増殖と転移が遅くなりました。重要なことに、HILPDAが低い腫瘍を持つ動物に抗PD‑1療法を投与すると腫瘍はよりよく縮小し、マウスの生存が延び、HILPDAが免疫療法の効果を左右することが示されました。
脂質合成、分子の鎧、そして免疫回避
さらに掘り下げると、HILPDAが腫瘍の代謝をどう変えて免疫防御を強化するかが明らかになりました。がん細胞内でHILPDAはシャペロンタンパク質HSP90に結合して転写因子KLF5を安定化させます。この三者が脂肪酸合成を促進し、とくにパルミト酸の合成を高めて腫瘍細胞に脂質滴を蓄積させます。これらの脂肪の一つがPD‑L1に付加されます。PD‑L1は腫瘍表面に存在し免疫細胞に「攻撃しないで」と信号を送るチェックポイントタンパク質です。研究チームは、PD‑L1の特定の部位にパルミト酸が付加されると、それが分子接着のように働き、PD‑L1を細胞膜に安定的に維持し分解を防ぐことを示しました。この付加部位を変異させると、PD‑L1の安定性は失われ、HILPDAが豊富でもがん細胞を守る能力が弱まりました。つまりHILPDA駆動の脂質合成はPD‑L1に化学的な修飾を供給し、腫瘍の免疫シールドを脆弱から強固なものへと変えているのです。
押せるブレーキ機構
どんなアクセルにもブレーキがあり、ここでのブレーキはTRIM21という別のタンパク質です。著者らはTRIM21がHILPDAを認識し、それを細胞の廃棄機構に送る分子の「フラグ」で標識することを発見しました。患者の乳腫瘍ではHILPDAが高い場合にTRIM21が低い傾向があり、TRIM21の低さは予後不良と関連しており、この自然のブレーキ機構ががんではしばしば弱まっていることを示唆します。研究チームは次にTRIM21を強化できる薬剤を探索し、ヒトでも試験されたことのあるレチノイド、フェンレチニドを同定しました。トリプルネガティブ乳がんの細胞および動物モデルで、フェンレチニドはTRIM21活性を高め、HILPDAの分解を促進し、脂質合成とPD‑L1の保護的修飾を減少させ、腫瘍増殖と転移を抑えました。もっとも注目すべきは、フェンレチニドと抗PD‑1療法を併用すると腫瘍が免疫攻撃に対してより脆弱になり、腫瘍微小環境でキラーT細胞やナチュラルキラー細胞が増え、抑制的な細胞が減少したことです。 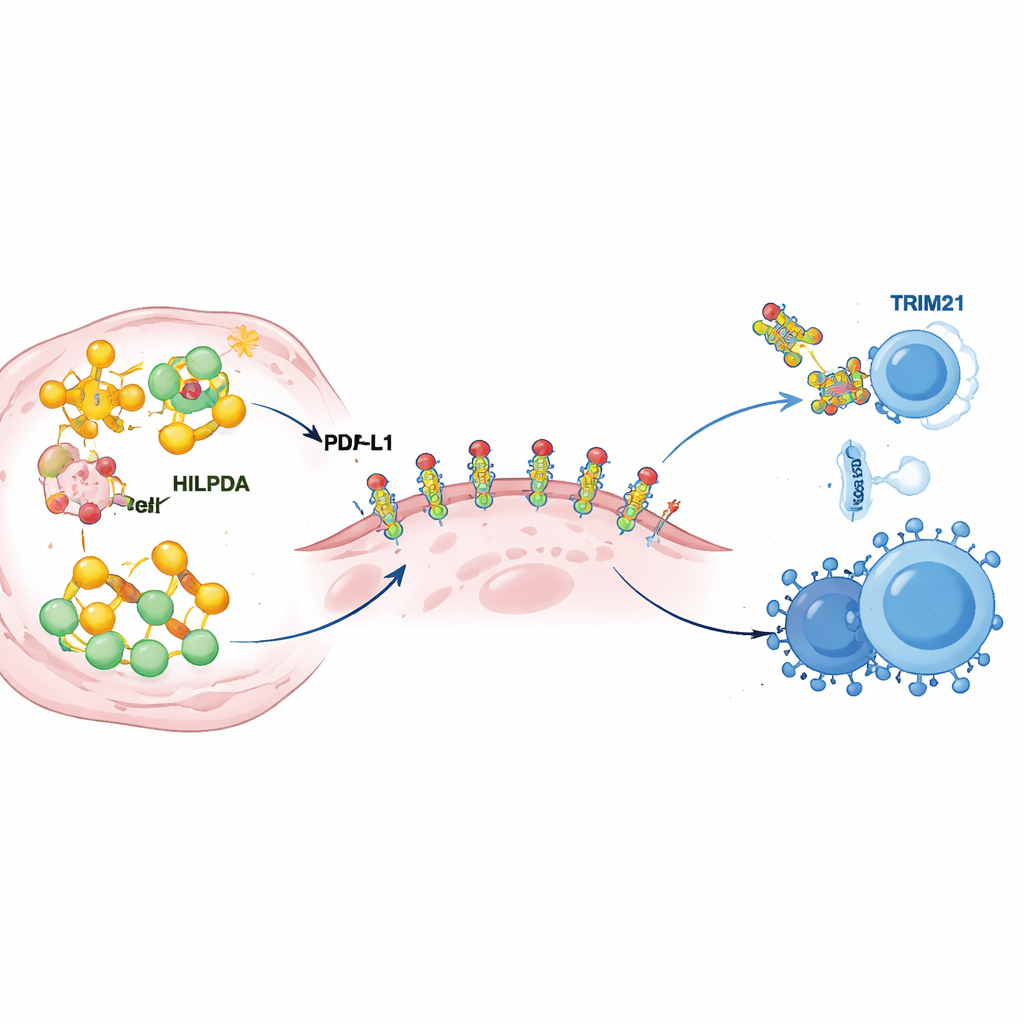
今後のがん治療に何を意味するか
本研究は、ストレスを受けた乳がん細胞がHILPDAを増やし、脂質合成を高め、表面のPD‑L1を化学的に強化してPD‑1阻害薬に直面しても免疫細胞の抑制を続ける一連の出来事を明らかにしました。TRIM21はHILPDAを分解してこの流れを崩せる内在的な安全装置として働きますが、腫瘍ではしばしば弱まっています。フェンレチニドがこの安全装置を再活性化できることを示したことで、代謝薬と既存の免疫療法を組み合わせて抵抗性を克服する実用的な方法が示唆されます。臨床試験で確認されれば、TRIM21–HILPDA–PD‑L1軸を標的にすることで、治療が難しいトリプルネガティブ乳がんの患者に免疫療法の恩恵を再びもたらす可能性があります。
引用: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
キーワード: トリプルネガティブ乳がん, 免疫療法抵抗性, PD‑L1のパルミトイル化, 腫瘍の脂質代謝, フェンレチニド