Clear Sky Science · ja
セレブロン(CRBN)は6-ホスホグルコン酸デヒドロゲナーゼ(6PGD)を負に制御して前立腺がんの転移を抑制する
この研究が重要な理由
前立腺から他の臓器へがんが広がると、治療は格段に困難になり、多くの場合致命的になります。本研究は、細胞内の“品質管理”タンパク質であまり知られていないセレブロン(CRBN)が、攻撃的な振る舞いに燃料を与える代謝酵素を分解することで前立腺がんの転移を抑える仕組みを明らかにします。この内在するブレーキ機構を理解することで、特に治療が難しい病型に対して転移を遅らせたり止めたりする新たな方策が示唆されます。
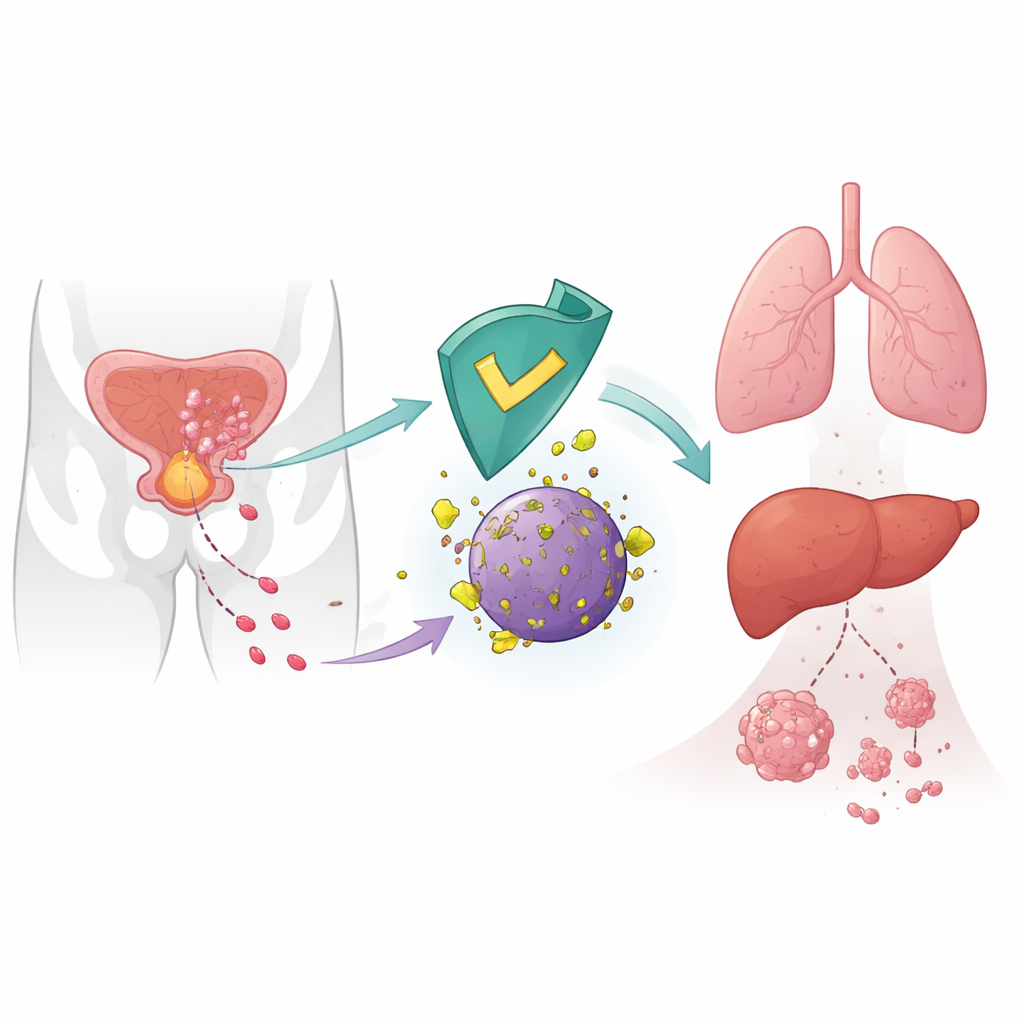
がんの拡散に対する内部ブレーキ
がん細胞は無作為に拡散するわけではなく、移動、浸潤、遠隔臓器の占拠に向けて内部の仕組みを再配線します。著者らは血液がんで使用されるサリドマイド類似薬の標的として知られるCRBNに着目しました。健康な細胞ではCRBNは特定のタンパク質に破壊の印を付ける分子廃棄装置の一部です。以前の研究は腫瘍でCRBN水準が低いことが予後不良と関連することを示唆していましたが、転移における直接的な役割は不明でした。本研究では、CRBNが6-ホスホグルコン酸デヒドロゲナーゼ(6PGD)という代謝酵素を分解の標的にすることで、前立腺がんの拡散を自然に抑える抑制因子として働くことを示します。
がんが乗っ取る代謝エンジン
6PGDは酸化型ペントースリン酸経路という代謝経路に位置し、細胞がNADPHを生成するのを助けます。NADPHは合成の材料を供給すると同時に抗酸化能を提供します。多くの腫瘍はこの経路を強化して増殖やストレス耐性を高めます。研究著者らは、患者由来の前立腺がん試料では正常前立腺組織に比べてCRBNが少なく6PGDが多い傾向があり、この不均衡は特に攻撃的ながんで顕著であることを見出しました。前立腺がん細胞株では、CRBNをノックダウンするかデザイナー化合物で分解すると6PGDのタンパク質量と酵素活性が上昇し、NADPHが増加しました。CRBNを回復させると逆に6PGDとNADPHが低下し、6PGDの遺伝子メッセージ(mRNA)は変わらなかったことから、タンパク質レベルでの制御であることが示されました。
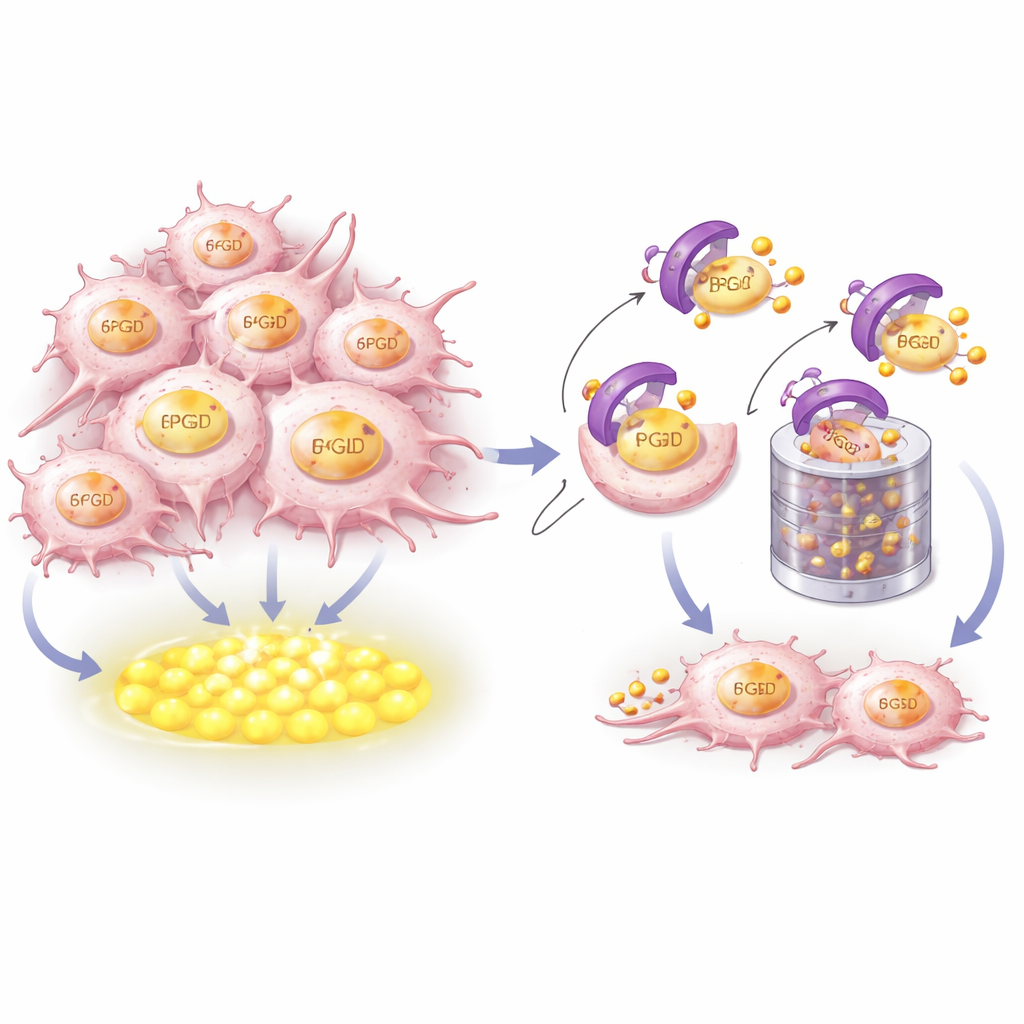
CRBNが燃料源を認識して破壊する仕組み
CRBNが6PGDを制御する仕組みを理解するために、研究者らは構造モデリングと生化学的実験を組み合わせました。CRBNは6PGDの末端近くにある短い高度に保存されたヘリカルな領域を物理的に掴むことを示しました。両タンパク質の重要なアミノ酸残基が密接に結合するドッキング界面を形成します。これらの接触点が変えられると、CRBNはもはや6PGDに結合できず、ユビキチンを付けて分解に導くことも、プロテアソームと呼ばれる細胞のシュレッダーに送ることもできなくなりました。注目すべきは、この認識面は免疫調節薬がCRBNに結合するポケットとは別であり、CRBNによる6PGDの制御は薬剤誘導効果ではなくCRBNの本来のハウスキーピング機能の一部であるという点です。
変化した代謝から細胞の遊走へ
この分子レベルのやり取りの結果は細胞の振る舞いのレベルで明確に現れます。CRBNを欠く前立腺がん細胞では、増加した6PGDとNADPHが細胞の運動性や人工バリアを越える浸潤と結びつき、転移能の指標となりました。CRBNを過剰発現させると細胞は移動性と浸潤性が低下し、増殖速度自体は変わりませんでした。遺伝子発現プロファイリングは、CRBNが上皮細胞の密着性に関連するCDH1の発現を高め、組織分解や移動に関連するMMP1の発現を下げることを示しました。重要なのは、これらの変化はCRBN–6PGDの直接結合を必要とし、6PGDの酵素活性を阻害することで逆転できたため、代謝の変化が転移行動の変化につながることが結び付けられた点です。
動物モデルや他のがんからの証拠
研究チームはマウスでこれらの仮説を検証しました。前立腺がん細胞を血流や脾臓に注入すると、余分なCRBNを産生するように設計した細胞は対照細胞より肝臓や肺にできる転移結節がはるかに少なく、生体内での抗転移作用が裏付けられました。CRBNを欠くように作られたマウスではいくつかの臓器で6PGDタンパク質量が高くなっていました。グリオブラストーマ、肺、腎のがん細胞株でも同様の傾向が見られ、CRBNを除去すると6PGDが増え、細胞の移動と浸潤が促進され、遺伝学的または薬剤による6PGD阻害がこの攻撃的な挙動を抑えました。これらの観察は、CRBN–6PGDによる転移抑制が前立腺がんに特有の現象ではないことを示唆します。
将来の治療への示唆
総じて、本研究はCRBNが代謝の門番として作用し、がん細胞が解放されて移動・播種するために必要なエネルギー供給を抑えることを提案します。CRBNが失われるか低下すると6PGDが蓄積し、NADPH産生が急増し、転移を促進する変化が起きやすくなります。臨床への示唆としては二つの可能性が考えられます:CRBNと6PGDの量を測定することで転移リスクの高い腫瘍を特定する手がかりになり得ること、そしてCRBN機能を高める治療やCRBN低下腫瘍における6PGDを選択的に抑える治療が、前立腺がんや他のがんの転移を遅らせたり予防したりする新たな方法を提供する可能性があることです。
引用: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
キーワード: 前立腺がんの転移, がんの代謝, セレブロン, 6PGD酵素, NADPH経路