Clear Sky Science · ja
多機能RNAヘリカーゼDDX39AはWISP1の選択的スプライシングを調節して免疫抑制的なマクロファージ分極を誘導し、膠芽腫の進展を促進する
この脳腫瘍研究が重要な理由
膠芽腫は治療後に再発しやすく薬剤耐性を示す、最も致命的な脳腫瘍の一つです。本研究は、腫瘍細胞内の単一の分子的「スイッチ」が腫瘍の増殖を助けるだけでなく、周囲の免疫細胞を戦う側から腫瘍を守る側へと変えてしまう仕組みを明らかにします。この連鎖反応をたどることで、研究者たちは既存の抗精神病薬の一つがこの有害なネットワークを破るために再利用できる可能性も特定しました。
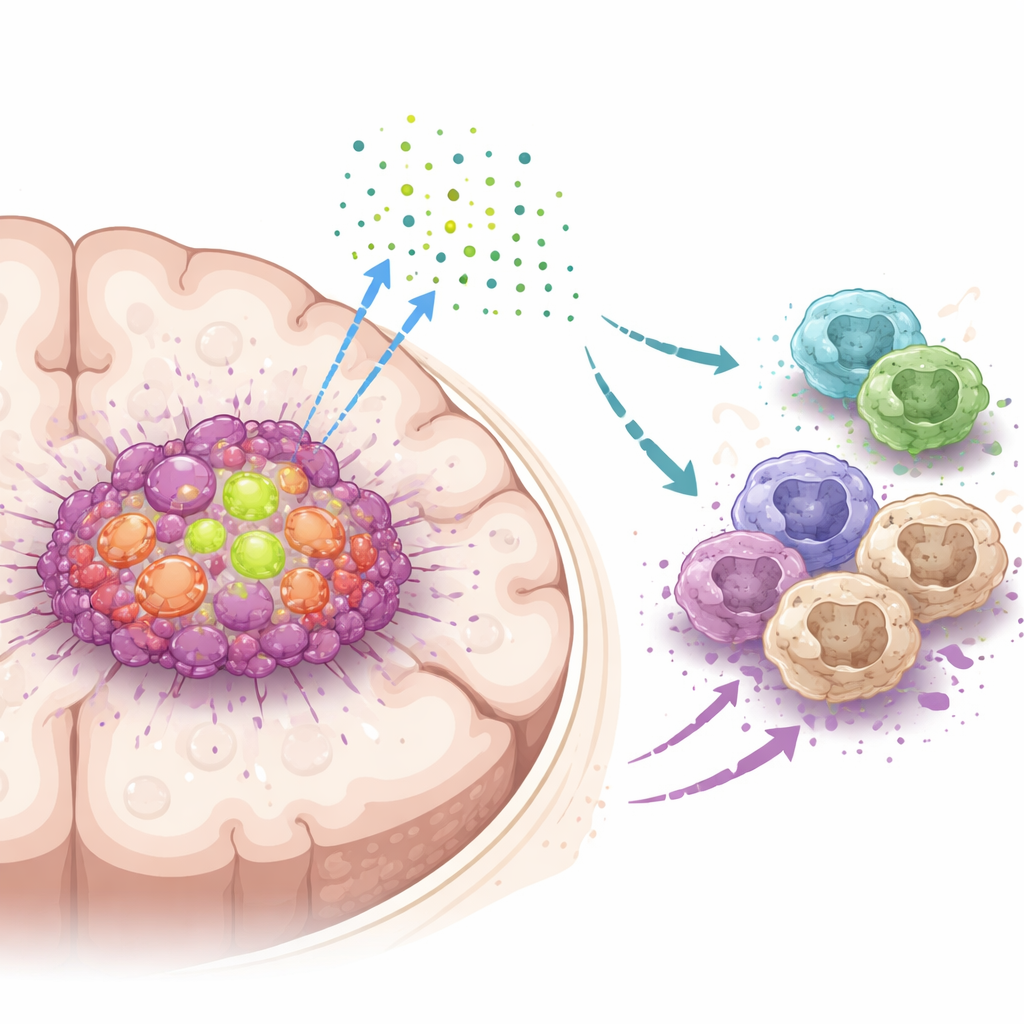
脳腫瘍細胞内の重要な補助因子
研究チームはDDX39Aと呼ばれるタンパク質に着目しました。これはRNAの処理を助ける分子機械です。大規模な患者データセットと腫瘍サンプルを解析したところ、DDX39Aは正常な脳組織に比べ膠芽腫で著しく活性化しており、その量は腫瘍の悪性度とともに増加していました。単一細胞解析では、DDX39Aが特に増殖の速い腫瘍細胞や腫瘍内にいる特定の免疫細胞(マクロファージ)に豊富であることが示されました。腫瘍内のDDX39Aが高い患者は予後が悪い傾向があり、このタンパク質が攻撃的な病態と密接に結びついていることを示唆しています。
この補助因子が成長と浸潤を促す仕組み
DDX39Aが実際に何をしているかを検証するため、研究者らは遺伝学的手法で膠芽腫幹様細胞のDDX39Aを抑え、培養系とマウスの脳腫瘍モデルで挙動を観察しました。DDX39Aを減らすと、腫瘍細胞の増殖が遅くなり、周囲組織への浸潤能が低下し、アポトーシス(プログラム細胞死)が起こりやすくなりました。また、がん幹様細胞は新たな腫瘍球(tumorsphere)を形成する能力を大きく失い、自己再生能が損なわれていることが示されました。マウスではDDX39Aを低下させた腫瘍は小さくなり、動物の生存期間が延び、DDX39Aが腫瘍進展を能動的に促す因子であることが確認されました。
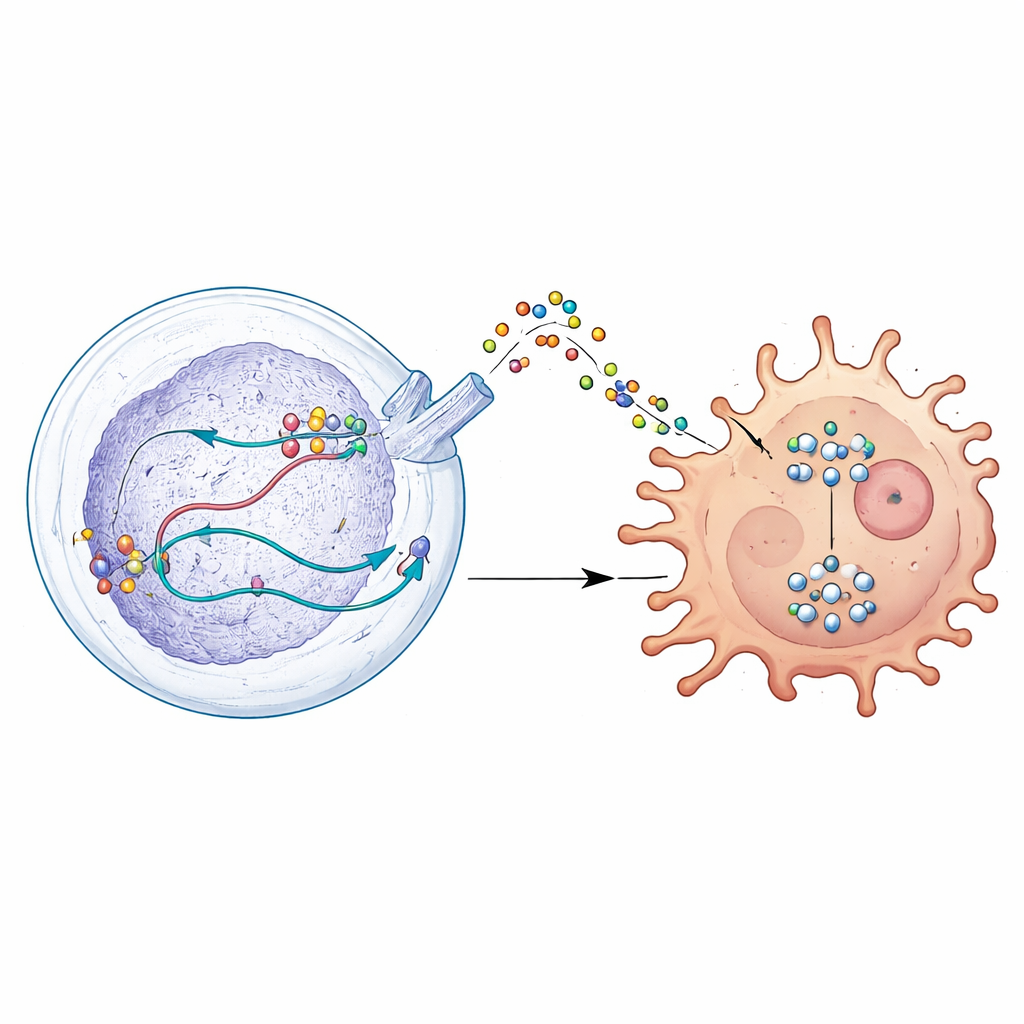
免疫防御を無効化する秘密の信号
さらに掘り下げると、DDX39AはWISP1という遺伝子の処理方法を変えることが分かりました。DDX39AはWISP1を単にオン・オフにするのではなく、そのRNAを形作りメッセージを安定化させることでWISP1タンパク質の産生を高めます。腫瘍細胞はこうして生成したWISP1を周囲に放出し、それが厄介な偽のシグナルとして作用します。腫瘍を攻撃する側にも支援する側にもなり得る近傍のマクロファージは、このシグナルに応答して免疫抑制的で腫瘍を助ける状態へとシフトします。このシフトはAKTとして知られる成長制御経路の活性化を介して駆動されます。DDX39AやWISP1を減らすと、この経路は静まり、腫瘍細胞は攻撃性を失い、マクロファージはより腫瘍と闘うプロフィールへ戻りました。
精神科薬をがん治療へ転用する試み
この経路図を手がかりに、研究者らはDDX39Aの活性を妨げうる化合物を薬剤データベースから探索しました。その中で脳に到達することが知られる長年使用されてきた抗精神病薬フルフェナジンに注目しました。計算モデルと結合試験により、フルフェナジンがDDX39Aに直接結合し得ることが示されました。腫瘍細胞内でこの薬はDDX39AのWISP1 RNAへの結合を弱め、WISP1レベルとAKTシグナルを低下させました。処理を受けた細胞は増殖や浸潤が減り、腫瘍球形成能が低下し、細胞死を起こしやすくなりました。マウスモデルではフルフェナジンは脳腫瘍の成長を遅らせ、腫瘍を支持するマクロファージの数を減らし、生存期間を延長しました。投与量は既に人で他の疾患に用いられている用量に近いものでした。
今後の治療への含意
平たく言えば、本研究は膠芽腫細胞がDDX39Aを利用してWISP1というメッセージを巧妙に調整し、それが細胞自身の持久力を高めると同時に周囲の免疫細胞を護衛に書き換えてしまうことを示しています。この補助因子を遺伝的にあるいはフルフェナジンのような薬で阻害することは、腫瘍細胞自身と免疫抑制的なマクロファージという二方面からがんを弱体化させます。患者への応用に至るにはさらに多くの検証が必要ですが、この成果は馴染みある薬を再利用して、最も手ごわい脳腫瘍の一つに新たな弱点を突く有望な道筋を開きます。
引用: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
キーワード: 膠芽腫, RNAスプライシング, 腫瘍微小環境, マクロファージ分極, 薬剤リポジショニング