Clear Sky Science · ja
PMM2はTRIM28と相互作用してE2F4をリクルートし、KIFC3媒介の腫瘍糖代謝と大腸癌進展を促進する
このがん研究が重要な理由
大腸がんは世界で最も致命的ながんの一つであり、その一因は多くの腫瘍が制御されない増殖のために体のエネルギーシステムを取り込むことを学習している点にあります。本研究は、あまり知られていない酵素PMM2が大腸腫瘍の糖代謝をより攻撃的にし、転移を促進する仕組みを明らかにし、将来の薬剤や診断検査の有望な新しい標的となりうる理由を示します。
糖を貪る腫瘍エンジン
がん細胞はしばしばグルコースの利用方法を書き換え、解糖系と呼ばれる高速だが効率の低い糖の燃焼を好みます。研究者らはまず、大腸腫瘍サンプルと近傍の正常組織の何千もの遺伝子を比較しました。通常は糖鎖をタンパク質に付加する役割を持つ酵素PMM2が、がんで著しく増加している遺伝子の一つとして際立ちました。PMM2を多く持つ腫瘍細胞は増殖が速く、コロニー形成や広がりが増加し、一方でPMM2を消した細胞は増殖が遅く、移動能が低下し、死にやすくなりました。
腫瘍細胞が糖利用を過激化する仕組み
研究チームが大腸がん細胞でPMM2レベルを下げると、細胞のグルコース取り込み、主要なエネルギー通貨であるATP産生、解糖系の廃棄物である乳酸の放出がいずれも減少しました。感度の高い代謝測定は、周囲培地の全体的な酸性化が低下し、酸素消費が上昇したことを示し、細胞が過度に活性化した解糖系からより通常の呼吸へとシフトしたことを示しました。重要な解糖系補助タンパク質であるPKM2やLDHAも減少しました。驚くべきことに、触媒活性を失った「非活性」型PMM2であってもこの糖嗜好的な挙動を促進でき、PMM2のがんにおける役割が本来の化学反応ではなく、細胞内で誰と結合するかに依存していることを示しました。
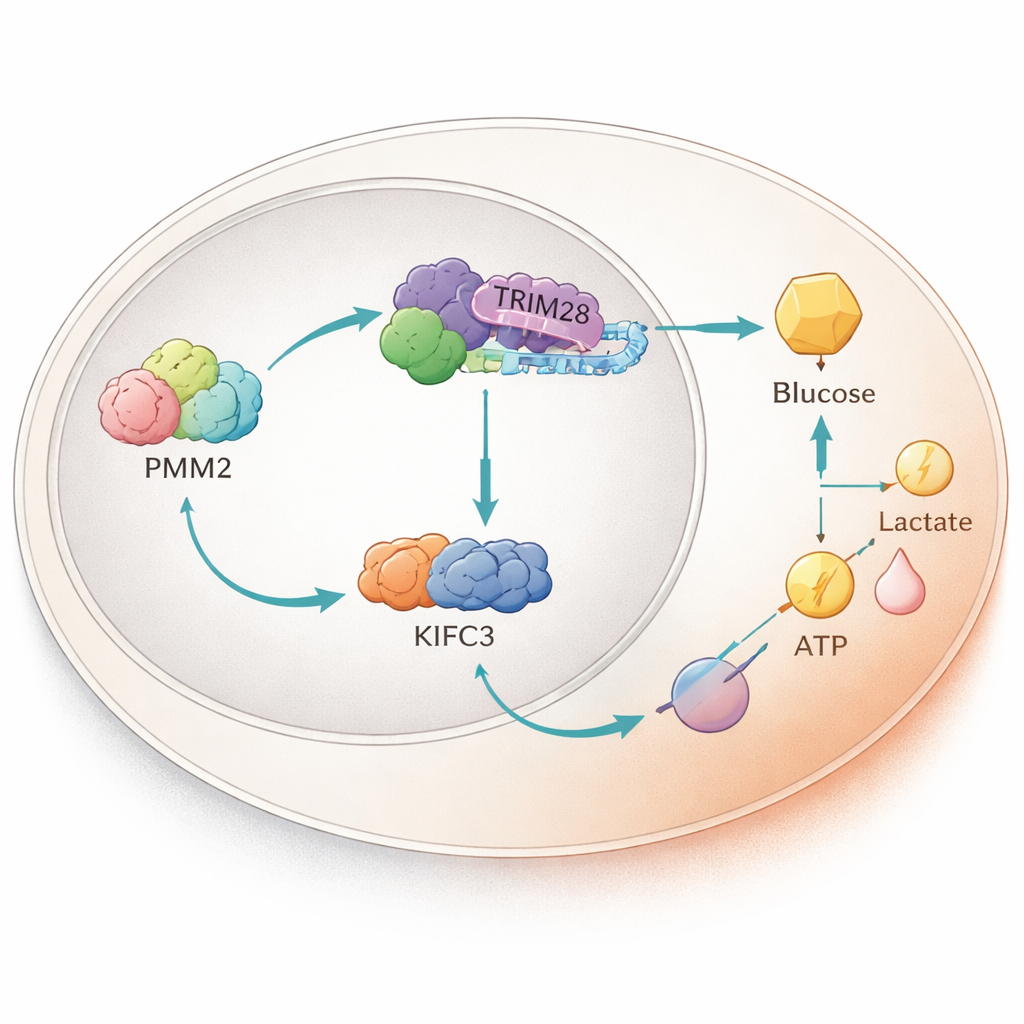
核内でのタンパク質リレー
さらに掘り下げると、PMM2はTRIM28という別のタンパク質に物理的に結合することが分かりました。TRIM28は細胞核に移行して遺伝子活性に影響を与えることができます。PMM2はTRIM28の核内蓄積を助け、TRIM28は転写因子E2F4と協働します。この三者はKIFC3というモータープロテインのDNA制御領域の特定の配列に結合してKIFC3の産生を促進します。TRIM28結合に必要なPMM2領域を欠失させる実験では、PMM2が解糖系や細胞増殖を増強する能力が消失し、PMM2の古典的な酵素機能ではなくこのタンパク質相互作用が腫瘍の有利性を担っていることが強調されました。
重要な代謝スイッチの活性化
細胞内部の足場に沿って貨物を運ぶ役割で知られるKIFC3は、重要な代謝スイッチであることがわかりました。研究者らがKIFC3レベルを低下させると、大腸がん細胞はグルコース摂取、ATPや乳酸の産生が減少し、解糖活性が弱まり、酸素消費が増加しました。重要なのは、KIFC3を沈黙させるとPMM2が引き起こす解糖増強や増殖優位が部分的に打ち消されたことです。ヒト大腸がん細胞を移植したマウスでは、PMM2を多く持つ腫瘍はより大きく成長しましたが、KIFC3をノックダウンするとその効果は鈍化しました。これらの動物から得た腫瘍サンプルではPMM2、KIFC3、解糖マーカーのレベルが高く、体内組織でも一連の連鎖が成り立つことが示されました。
実験モデルから患者サンプルへ
臨床への応用を視野に入れるため、チームは患者由来の大腸がんからオルガノイドと呼ばれる小型の三次元腫瘍を作成しました。PMM2とKIFC3のレベルが高いオルガノイドは、低いものよりも早く成長し、ATPや乳酸を多く産生しました。オルガノイドにPMM2を過剰発現させるとKIFC3と解糖が増加し、PMM2を低下させると逆の効果が見られました。患者腫瘍アレイの解析でも、高いPMM2レベルは進行した病期、リンパ節転移、全生存期間の短縮と関連しており、PMM2は有力なバイオマーカー候補であることが示されました。
将来の治療への意味
簡潔に言えば、本研究は多くの大腸腫瘍がPMM2を核内のタンパク質リレー(TRIM28とE2F4を介して)に組み込み、KIFC3とそれに続く糖代謝機構を活性化していることを示しています。その代謝的な急増ががんの成長と転移を助けます。この経路がPMM2の通常の酵素活性ではなくタンパク質相互作用に依存していることから、治療の新しい道が開けます。具体的には、PMM2とTRIM28の結合を妨げる小分子やペプチド、分解剤、E2F4のDNAアクセスを阻む手法、あるいはKIFC3の活性を抑える手段はいずれも理論的には腫瘍の優先的燃料を枯渇させうる可能性があります。こうした治療法はまだ実用化されていませんが、PMM2–TRIM28–E2F4–KIFC3の連鎖は大腸がんに対するより精密で代謝に焦点を当てた戦略の有望な設計図となります。
引用: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
キーワード: 大腸がん, 腫瘍代謝, 解糖系, 発がん性シグナル, バイオマーカー