Clear Sky Science · ja
乳がんにおけるレチノイド、レチノイン酸受容体およびエピジェネティクスの関連性
乳がんにおけるビタミンAの重要性
多くの人にとってビタミンAは視力に重要な栄養素として知られていますが、体内での活性型であるレチノイン酸は、細胞が増殖するか、分化して安定した形になるか、あるいは損傷時に自ら死を選ぶかを決める働きも担います。本総説は、乳がんにおいてレチノイン酸とその細胞内の“ドッキングステーション”(受容体)がどのように変化するか、有望な実験室レベルの成果がなぜ患者治療につながらなかったか、そしてがん細胞の“ソフトウェア”であるエピジェネティックなコードに関する新たな知見がこの治療戦略をどう蘇らせるかを検討します。
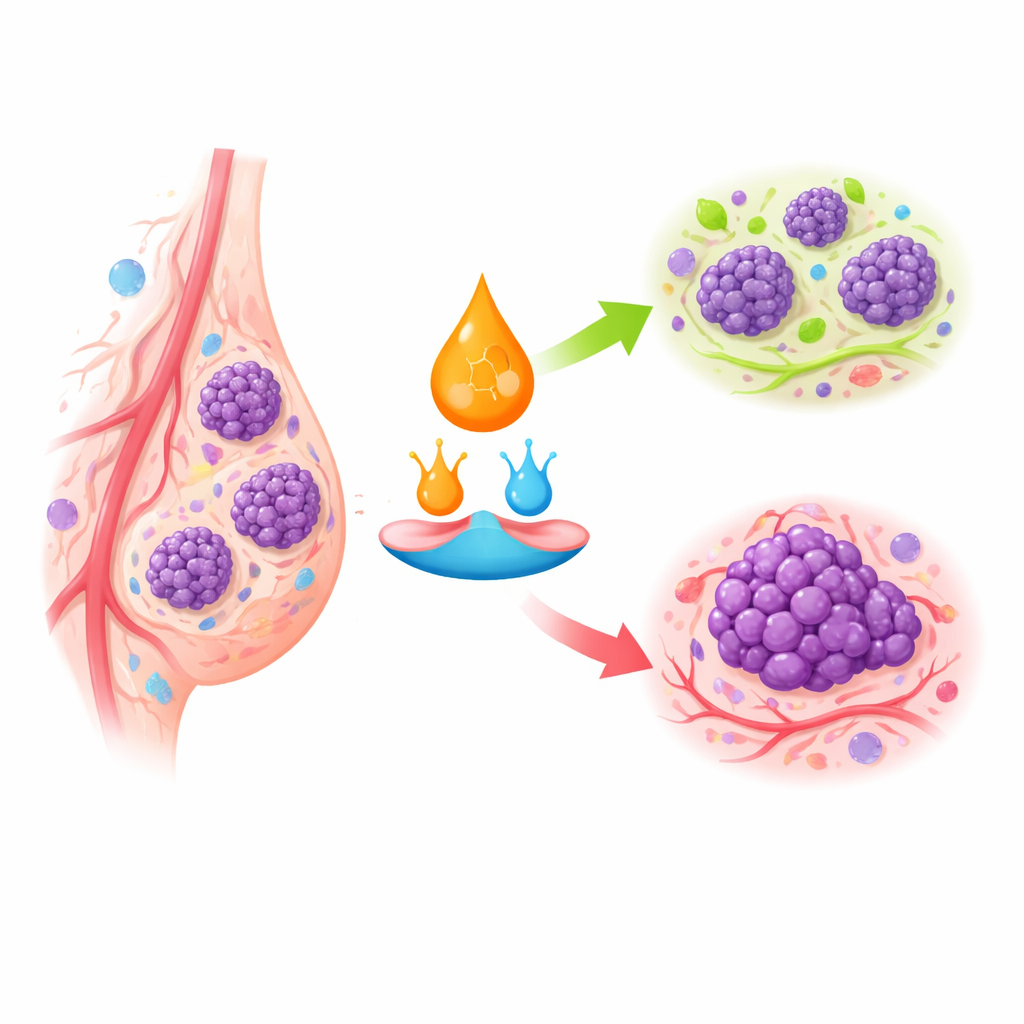
増殖と自滅のための細胞内信号の信号機
レチノイン酸は細胞内の特定の受容体に結合することで作用し、その結果として遺伝子群のスイッチをまとめてオン/オフします。健康な乳房組織では、このシステムが細胞に分裂を止めて成熟した安定した形になるよう促したり、異常が生じた際に細胞死を誘導したりします。乳がん、特により攻撃的なサブタイプでは、主要な受容体が欠失または沈黙していたり、レチノイン酸の細胞内輸送経路が書き換えられています。増殖を抑える受容体に届けられる代わりに、生存や増殖を促す経路に流されることがあり、これが一部の乳腫瘍でレチノイド薬がほとんど効かない理由を説明します。これらの薬が特定の血液がんで非常に有効であるのとは対照的です。
がん細胞のソフトウェアに潜むスイッチ
著者らはエピジェネティクスに注目しています。エピジェネティクスとは、ゲノムの“設定”のように働くDNAやその梱包タンパク質に付く化学的なタグのことです。多くの乳がんでは、これらのタグが重要なレチノイン酸受容体、特にRARβ2と呼ばれるものを基底のDNA配列を変えずに「オフ」に固定してしまいます。DNAへの過剰なメチル化や周辺のタンパク質スプールの締め付けがこの受容体を不活化し、他の酵素はクロマチンの環境を成長や遊走を促す状態へと再構築します。タンパク質を作らないが遺伝子活性に影響する非コードRNAも、細胞死や分化からシグナルを逸らす方向へさらに偏らせます。これらの変化が総合して、がん細胞に治療抵抗性やストレスへの適応性を与えます。
シグナル経路の再配線
重要なことに、これらのエピジェネティックなロックは可逆的です。実験モデルでは、DNAメチル化を除去したりクロマチンを緩めたりする薬剤がRARβ2やレチノイン酸経路の他の構成要素を回復させることが示されています。これらの“プライミング”剤をレチノイン酸自体や標準的な化学療法と組み合わせると、腫瘍をより効果的に縮小し、再発の原動力と考えられる幹様細胞のプールを減らします。細胞内でのレチノイン酸のシャトル方法も重要で、あるキャリアタンパクはそれを増殖抑制受容体へ導き、別のキャリアは増殖促進経路へ届けます。これらのキャリアのバランスを調整することで、レチノイン酸が“肥料”のように働くか“ブレーキ”のように働くかを反転させることができます。
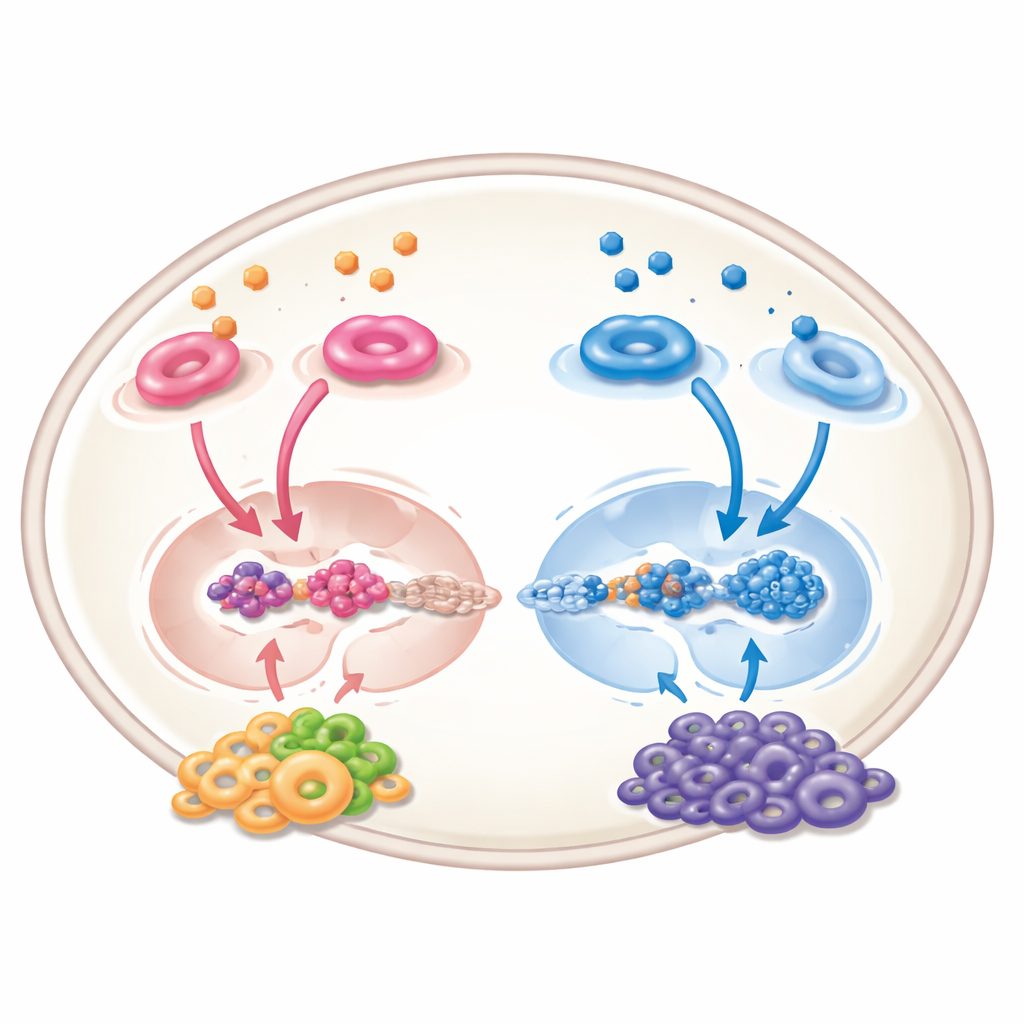
腫瘍を超えて:周辺環境の影響
レチノイン酸はがん細胞だけで作用するわけではなく、血管、免疫細胞、支持細胞といった腫瘍を取り巻く“近隣”環境も再構築します。実験系では、新生血管の成長を抑え、免疫細胞をより活性化した腫瘍攻撃型へ促し、通常は体の防御を鈍らせる抑制的な細胞を制限することが示されています。しかし、話は必ずしも一方的に良いわけではありません。腫瘍を囲む特定の間質細胞では、レチノイン酸シグナルの活性化が化学的コミュニケーションを強めて悪性細胞を引き寄せ、がんの増殖を助長することがあります。これらの相反する効果は、将来の治療が適切な細胞型を適切な方法で標的にするよう慎重に調整されなければならないことを意味します。
より賢い臨床試験設計へ
乳がんに対するレチノイド薬の初期の臨床試験は大部分が失敗しましたが、それらは今日のサブタイプ、バイオマーカー、複雑な薬理学に関する理解が深まる前に行われました。著者らは、新たな試験ではレチノイド感受性の分子学的特徴、たとえば受容体発現の保持や特定のDNAメチル化パターンを示す患者を選択し、エピジェネティックな障壁を解除する薬剤、成長経路を標的にする薬剤、あるいは免疫応答を高める薬剤とレチノイドを組み合わせるべきだと主張しています。体内で薬物濃度を安定させる改良された製剤や、腫瘍とその周辺組織の綿密なモニタリングも重要です。これらの障壁が克服されれば、レチノイン酸ベースの治療は選択されたタイプの乳がんに対する精密治療の一手段として再び位置を占める可能性があります。
引用: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
キーワード: レチノイン酸, 乳がん, エピジェネティクス, 分化療法, 腫瘍微小環境