Clear Sky Science · ja
YEATS2はDNA修復を促進し、クロマチンアクセス性を高めて脱着依存性細胞死(アノイキス)耐性を誘導し前立腺がんの転移を促進する
なぜ「離れない」がん細胞が重要なのか
がんが原発巣から離れて遠隔臓器に広がると、治療は格段に難しくなります。前立腺がんも例外ではなく、リンパ節や骨に新たな腫瘍を形成すると生存率は大きく低下します。転移の過程では、腫瘍細胞がまず宿主組織から剥がれて血管やリンパ管に入る必要があります。こうした遊走細胞の多くは死にますが、ごく一部はこの剥離によって誘導される細胞死(アノイキス)に抵抗する能力を獲得します。本研究は、YEATS2というタンパク質がDNA損傷の修復能力を強化することで、前立腺がん細胞がその危険な旅を生き抜く手助けをしている仕組みを解き明かします。
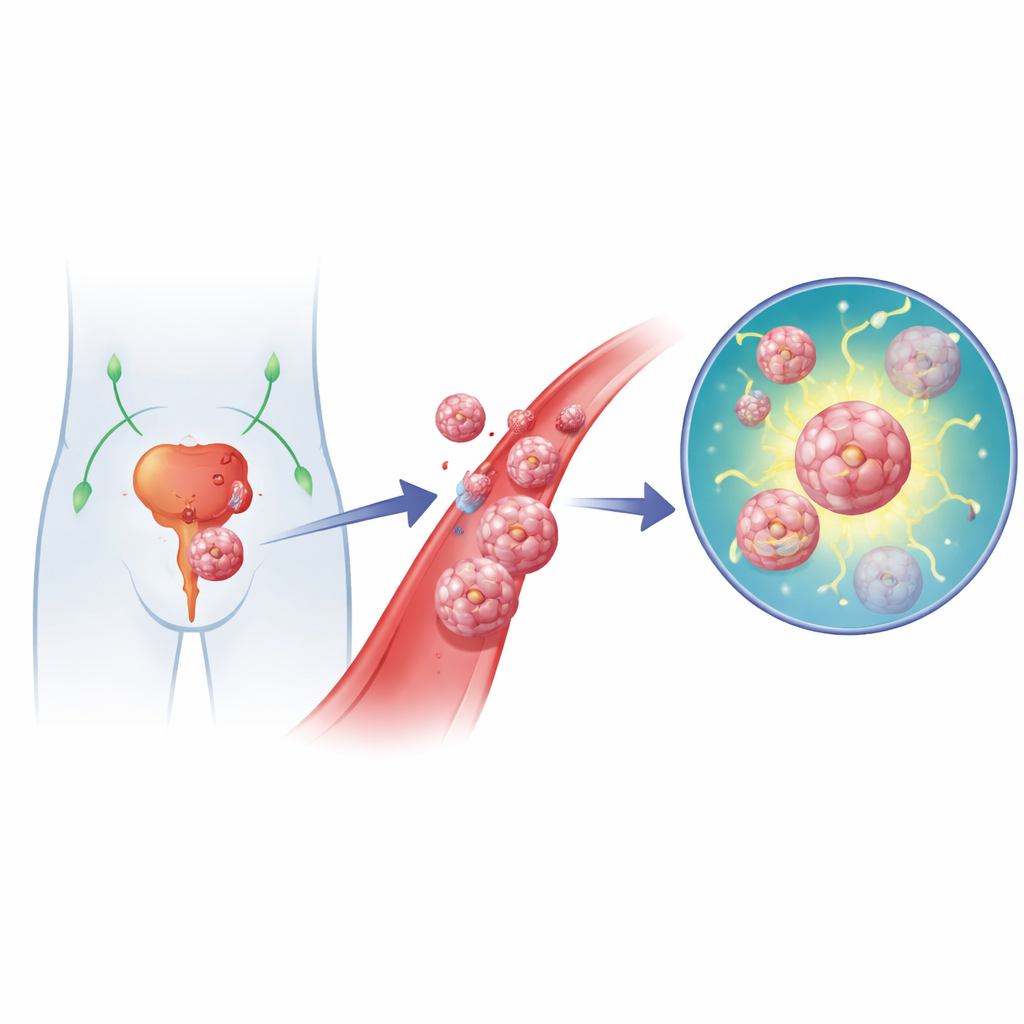
移動する細胞たち
研究者らはまず、転移した前立腺腫瘍が原発腫瘍と何が異なるかを問いかけました。公開されているがんデータベースの遺伝子データと、非付着状態での生存を選択させた前立腺がん細胞に関する自らの実験結果を比較しました。患者サンプルと培養細胞の両方で、転移性およびアノイキス耐性細胞において一貫して変化している少数の遺伝子群が際立ちました。その中でYEATS2は強く発現上昇しており、発現が高い患者は生存期間が短く、病勢進行が早いことと強く結びついていました。
容疑者を検証する
YEATS2の役割を調べるため、チームは前立腺がん細胞をマウスの足底に注入してリンパ節への広がりを再現するモデルを構築し、原発腫瘍と近傍の膝窩リンパ節の両方を採取しました。リンパ節転移から採取した細胞は、原発腫瘍由来の細胞に比べて懸濁状態での生存、運動性、浸潤能が優れていました。これらの転移細胞ではYEATS2の発現も高くなっていました。培養試験でYEATS2を人工的に増やすと、剥離後の細胞が死ににくくなり、移動・浸潤能が高まりました。逆にYEATS2をノックダウンするとこれらの性質は失われ、マウスでのリンパ節転移は大幅に減少しました。
生存のトリックとしてのDNA修復
周囲の組織から剥がれると、がん細胞にはストレスがかかり、部分的にはDNAを損傷する有害分子が増加します。DNA二本鎖切断のマーカーを用いた解析で、懸濁状態にある細胞はDNA損傷をより多く蓄積し、特に原発腫瘍由来の細胞でその傾向が顕著であることが示されました。YEATS2を過剰発現させるとこの損傷は軽減し、YEATS2を沈黙させると損傷が増えて懸濁状態での生存が低下しました。大規模患者データ解析では、DNA損傷応答や修復に関わる遺伝子群がYEATS2の活性と強く関連していました。中でも修復遺伝子RAD50が重要なパートナーとして浮上しました:RAD50は転移性およびアノイキス耐性細胞で高発現し、YEATS2の増加に伴って上昇し、YEATS2欠失細胞に再導入すると生存を回復させました。
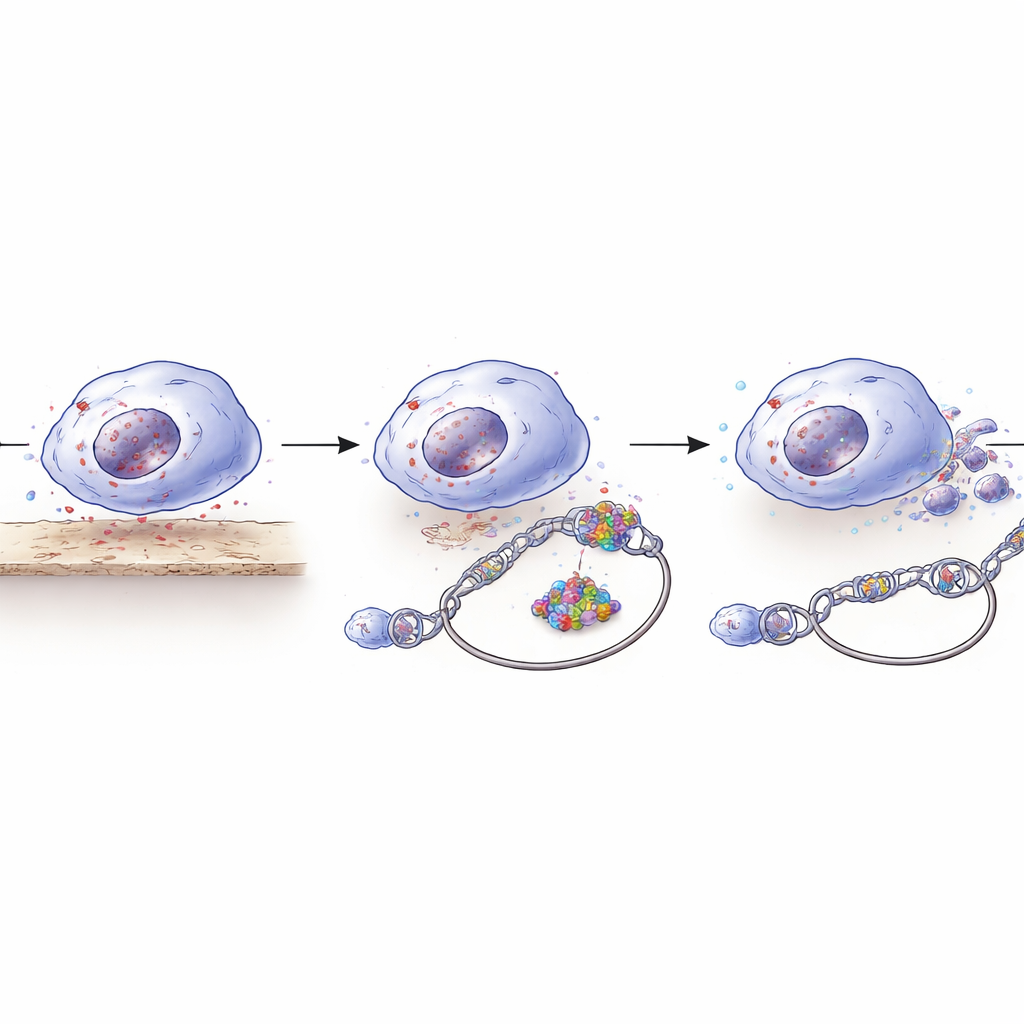
DNAの栞(しおり)を開く
YEATS2はどのようにRAD50を増やすのでしょうか。YEATS2はDNAのパッケージングを変化させるタンパク質複合体の一部であり、特定の遺伝子を読みやすくしたり読みにくくしたりします。研究チームは「開いた」領域と「閉じた」領域をマッピングする手法を用い、YEATS2がRAD50のプロモーター領域のアクセス性を高めることを見いだしました。この開かれたDNA領域で、YEATS2はヒストンタンパク質上の化学的標識(H3K27アセチル化)を認識し、そのYEATSドメインを介して近傍にさらなるアセチル化マークを呼び込む助けをしました。こうした変化は栞を開いて段落に蛍光マーカーを付けるような働きをし、転写因子NR2C2がより効率的に結合してRAD50の発現を促進できるようにしました。YEATS2とNR2C2は協働して、剥離した細胞が最も必要とする時期に修復能力を高める生存回路を形成しました。
逃走ルートを阻む
RAD50は危険なDNA二本鎖切断を修復する中核装置であるMRN複合体の一員であるため、研究者らはこの機構を乱せば転移を鈍らせられるかを探りました。彼らはMRN複合体を阻害する小分子Mirinを用い、またRAD50のパートナーであるMRE11の発現を低下させる手法を試しました。どちらの戦略もDNA損傷を増大させ、RAD50が豊富であっても前立腺がん細胞の肺やリンパ節へのコロニー形成能力を低下させました。これらの所見は、転移性前立腺がんが剥離と移動を生き延びるために強化されたDNA修復に大きく依存していることを示唆します。
患者にとっての意義
日常語で言えば、本研究は前立腺がんの一部の細胞が旅の最も危険な段階――原発巣から離れている間――にDNAをより効果的に修復する術を身につけることで死を免れていることを示しています。YEATS2は遺伝情報の教科書の該当ページを開く分子的なファシリテーターとして働き、RAD50やその修復パートナーが大量に産生されるようにします。こうした強化された修復によって、異常細胞は血流やリンパ系を渡っても死ぬことなく、新たな腫瘍を播種する可能性を高めます。したがって、YEATS2–NR2C2–RAD50経路やそれが支えるMRN修復複合体を標的にすることは、前立腺がんの転移を抑える新たな手段を提供し、進行した病態の男性の転帰改善につながる可能性があります。
引用: Li, H., Song, Y., Cong, Y. et al. YEATS2 promotes DNA repair and induces anoikis resistance by enhancing chromatin accessibility to drive prostate cancer metastasis. Oncogene 45, 971–988 (2026). https://doi.org/10.1038/s41388-026-03696-x
キーワード: 前立腺がんの転移, DNA修復, アノイキス耐性, クロマチンのアクセス性, RAD50