Clear Sky Science · ja
腫瘍細胞と健全なクラスターのマルチスケール高スループット濃縮のための段階的慣性マイクロフルイディクス:悪性度診断の強化へ
なぜ体液中のがん細胞を分離することが重要なのか
がんが広がる際、腫瘍細胞はしばしば臓器を覆う液体に脱落します。肺がん患者では、肺の周囲に溜まる液体、つまり胸水がその代表例です。この液体の中には稀な単一の腫瘍細胞や緊密に結合した細胞の塊(クラスター)が含まれます。こうしたクラスターは、攻撃的な病態や予後不良と強く関連するため特に危険だと考えられています。しかし現行の実験室法では、大量の患者由来液から単一細胞とクラスターの両方をやさしくかつ効率的に回収することは難しいのが現状です。本研究は、胸水からこれらの細胞を迅速かつ丁寧に選別できる新たなチップベース技術を提示し、より信頼できるがん診断と腫瘍転移メカニズムに関する洞察の向上への道を開きます。
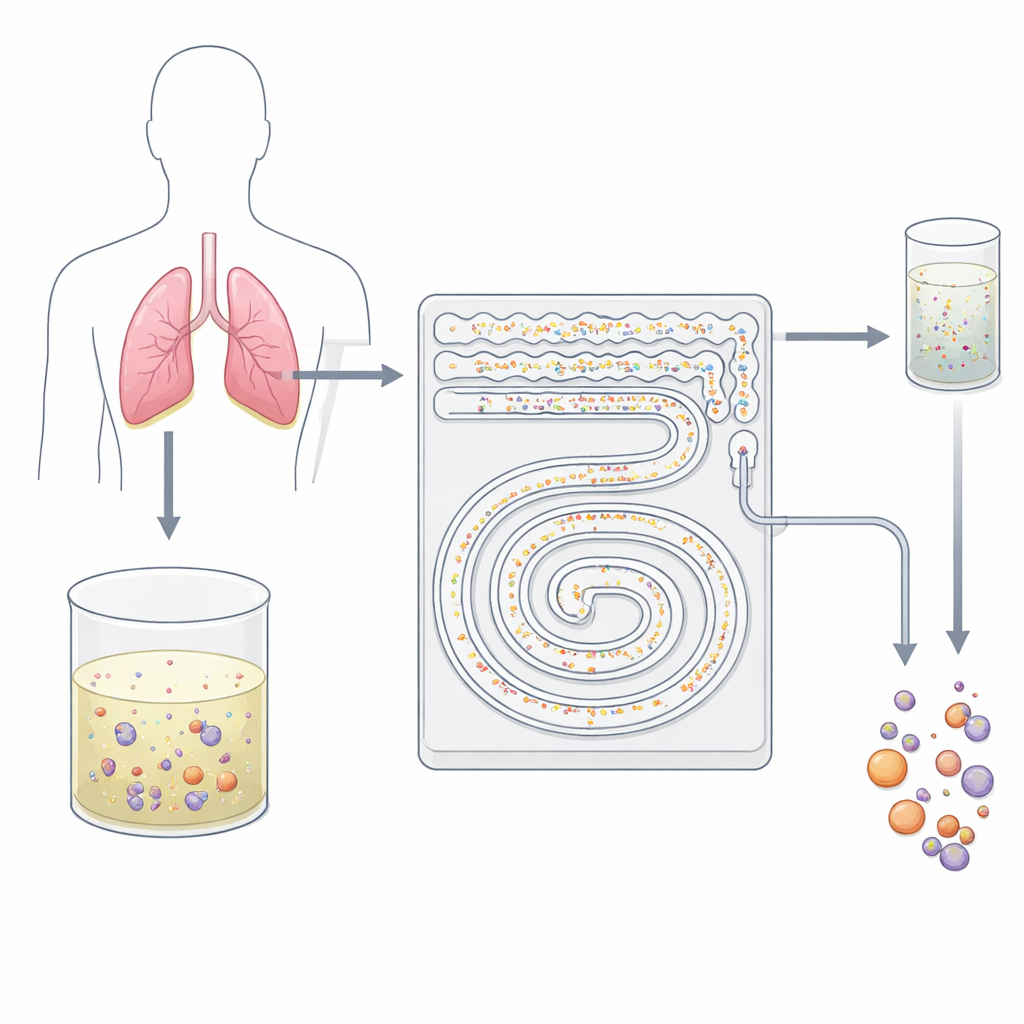
チップ上のやさしい細胞ストレーナー
研究者らは小指大のプラスチックデバイスを設計し、微小チャネルを彫り込んで賢い二段階のフィルターのように機能させました。粘着性の抗体や粗いろ過を使う代わりに、このチップは高速流体中での細胞の振る舞いを利用します。曲がったマイクロチャネルを流れる液体では、見えない力が粒子の大きさに応じて異なる流線へと押し分けます。研究チームはこの効果(一般に慣性マイクロフルイディクスとして知られる)を活用し、接触や標識を行わずに小さな背景の血球と大きな腫瘍細胞やそのクラスターを分離します。全てが連続した閉じた流れの中で起こるため、デバイスは数十ミリリットルの液体を数分で処理できます—スライドベースの伝統的な細胞診では容易には達成できない速度です。
第一段階:雑多な細胞の除去
装置の第一段階では、余分な液体を除去して細胞を再懸濁した胸水が並列の蛇行チャネル群に流されます。ここでは曲がった流れによる渦が小さな白血球をチャネル壁側へ押しやり、より大きな腫瘍細胞やクラスターは流れの中心付近に留まります。小さな細胞は廃棄出口へ導かれ、背景成分が劇的に希釈されます。この高スループット段階は約8ミリリットル毎分で動作でき、典型的な50ミリリットルの臨床サンプルは詰まりなく約6分半で処理できます。第一段階から出てくるのは、潜在的に悪性の細胞が濃縮された、よりクリーンな混合物です。ここからより精密な分離に進みます。
第二段階:単一細胞とクラスターの分離
部分的に濃縮されたサンプルは、狭部と広部が繰り返される斜めのらせんチャネルに入ります。この段階では、異なる大きさの物体に対して複数の流体力が異なった平衡を作り、内側または外側の壁近くの別個のレーンへと導きます。より小さな単一の腫瘍様細胞はある側方位置に整列し、かさばるクラスターは内側の壁近くの別の位置へ移動します。適切な位置に出口を配置することで、チップはこれらの流れを物理的に分割します:一つの出口は主に単一腫瘍細胞を回収し、別の出口は形を保ったクラスターを回収し、残りの小さな細胞は別の出口で除去されます。重要なのは、クラスターが一塊のまま維持されることで、従来のろ過法でしばしば見られる損傷や分解を避けられる点です。
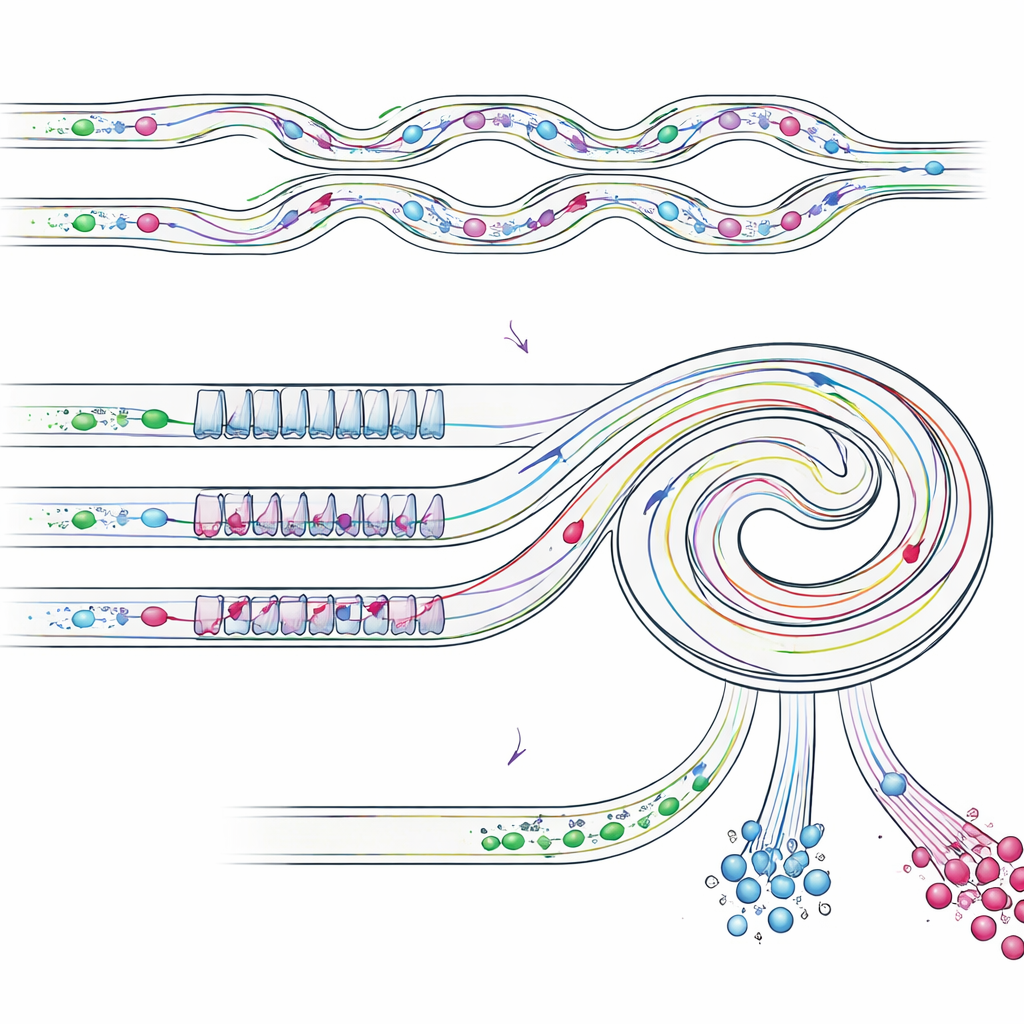
装置の性能検証
設計の有効性を確かめるため、まず既知サイズのプラスチックビーズを用いて血球、単一腫瘍細胞、クラスターを模倣しました。段階的チップは「単一細胞」ビーズの87%以上、「クラスター」ビーズの約92%を回収し、より小さな「血球」ビーズの大部分を除去することを示しました。次に白血球と混合した実際の肺がん細胞(A549細胞)で試験を行いました。これらのテストでは、装置は全体で約82%のがん細胞を回収し、濃縮された分画で約76%の純度、クラスターに対してはほぼ80%の純度を得ました。最後に、3名の肺がん患者から得た実際の胸水サンプルを処理しました。腫瘍細胞やクラスターが全細胞の1%未満を占めるような出発液から、チップは単一の悪性細胞が全細胞の約68%、クラスターが専用の出口流で約35%を占める分画を生成しました。
患者にとっての意義
流体の流れとチャネル形状のみを用いることで、このデバイスは化学的標識や複雑な装置を使わずに、大量の患者由来液から単一腫瘍細胞と形を保ったクラスターの両方を迅速かつやさしく回収できます。濃縮された細胞は免疫蛍光染色や顕微鏡観察などの標準的な検査に適しており、既存の病院のワークフローにスムーズに組み込めます。本研究は少数の患者を対象としたものであり、診断や予後への影響を証明するにはより大規模な試験が必要ですが、ラベル不要の高速「細胞濃縮装置」という強力な概念を示しています。長期的には、このようなツールが悪性度評価を鋭敏にし、個別化治療の選択を導き、がんの転移過程への理解を深める可能性があります。
引用: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
キーワード: リキッドバイオプシー, マイクロフルイディック細胞ソーティング, 腫瘍細胞クラスター, 胸水, がん診断