Clear Sky Science · ja
PEG化CuドープWS2ハイブリッドナノシートを用いた標的型マルチモーダルがん治療
なぜより賢いがん治療が重要なのか
多くの乳がん患者は依然として、周囲の健康な組織を傷つけながら腫瘍を完全には抑えられないような過酷な治療に直面しています。本研究は、肉眼では見えないほど小さな人工ナノシートという新しい材料を紹介します。これらは体内を巡り、乳がんに選択的に到達し、複数の作用を協調して同時に働かせるように設計されています。熱、化学反応、そして従来の抗がん剤を一つの標的化されたパッケージに組み合わせることで、治療の効果を高めつつ、全身への負担を軽減することを目指しています。 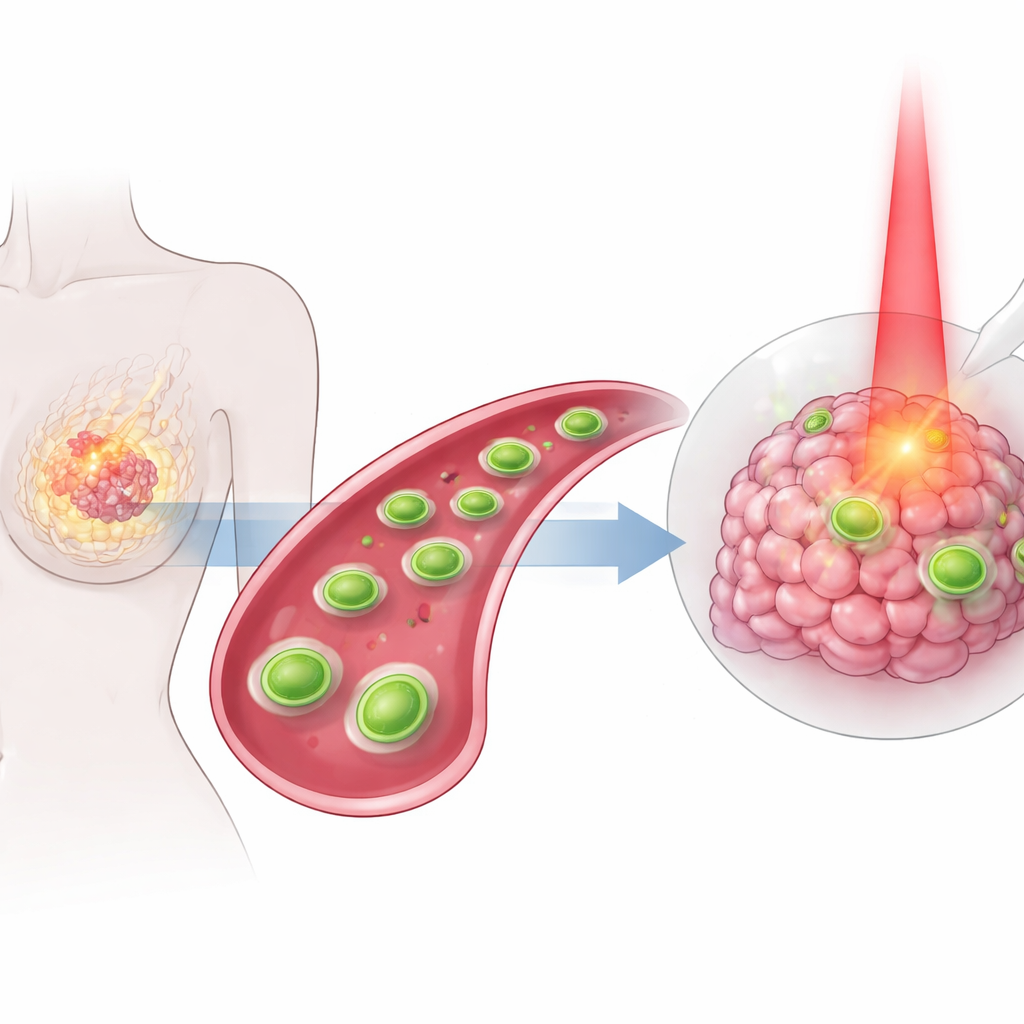
薬剤を運搬・放出するために設計された極小シート
このアプローチの核心は、タングステンと硫黄からなる超薄型の材料で、ナノサイズのシート状をしています。これらのシートは近赤外光を自然に吸収して熱に変換します。研究チームはまずこれらのシートを作製し、続いて他の有用成分を担持できるように表面を慎重に粗造化しました。銅原子はシート上に高分散で固定され、体液中でよく混ざり凝集を避けるための柔らかく柔軟な被覆(分子レインコートに似たもの)が追加されました。最後に、腫瘍細胞が好んで取り込む葉酸をホーミング装置として結合し、一般的な化学療法薬ドキソルビシンを表面に搭載しました。最終的に得られるのは、血流中を循環し腫瘍細胞を認識して大量の治療薬を運搬できる、層状の小さなプラットフォームです。
光、化学、薬剤が連携して働く仕組み
これらの粒子が腫瘍に到達すると、いくつかの作用が同時に起こります。腫瘍領域に穏やかな赤色レーザーを照射すると、タングステン–硫黄シートが効率よく加熱され、局所温度が上昇してがん細胞にストレスと損傷を与えますが、全身を過度に加熱することはありません。同時に、シート上の銅原子は腫瘍内で通常より高濃度に存在する過酸化水素と反応します。この反応により過酸化水素が非常に反応性の高い短寿命の酸化剤に変わり、細胞内の構成要素を内側から損傷します。腫瘍は正常組織よりやや酸性に傾く傾向があり、この酸性環境下とレーザーによる加熱のもとで、シートとドキソルビシンの結合が緩み、薬剤が必要な場所でより多く放出されます。これら三つの効果—熱、化学的攻撃、局所的化学療法—は互いに補強し合うよう設計されています。 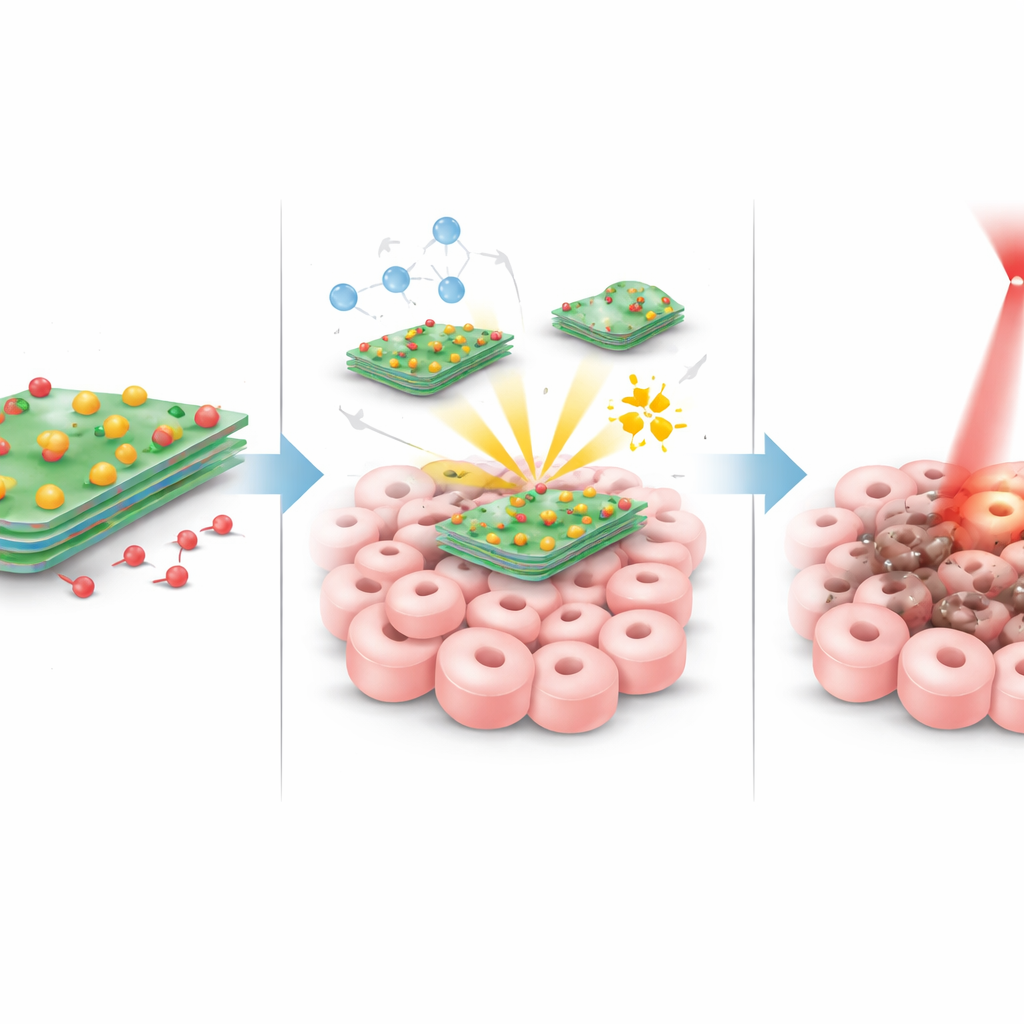
細胞実験と腫瘍移植マウスでの証拠
培養皿内では、被覆したシート単独では正常細胞に対する毒性は低く、基本的な安全性が示唆されました。しかし、ドキソルビシンを搭載し、過酸化水素存在下でレーザー照射を行うと、単独の治療よりもはるかに強い乳がん細胞死が誘導されました。研究者らはまた、これらの粒子が腫瘍細胞内で反応性酸化種の急増を引き起こすことを示し、銅を介した化学反応が活性であることを確認しました。乳がんを移植したマウスでは、葉酸被覆粒子が非標的粒子よりも腫瘍組織に強く、かつ長く蓄積しました。マウスに完全な組合せ治療(標的化粒子+赤色光照射)を施したところ、腫瘍は劇的に縮小し、生存期間は延び、体重や臓器の健康状態は概ね正常に保たれ、従来の薬物治療に比べて副作用が限定的であることが示されました。
将来のがん治療にとっての意義
総合すると、これらの設計されたシートは多機能ツールのように振る舞い、腫瘍を探索して加熱し、反応性化学により内部から毒性を与え、かつ実績のある薬剤をより精密に届けることで、体の大部分を温存することができます。研究はまだ動物実験段階にあり、長期的な安全性、分解性、ヒト使用に適した製造方法など重要な課題が残っています。それでも、この設計は腫瘍の環境に合わせていくつかの穏やかな治療を一つのスマートなパッケージに統合することで、総合的に強い効果を生み出せることを示しています。今後の研究で安全性と有効性が確認されれば、この種の多機能ナノプラットフォームは乳がん治療をより標的化し、効率的で、患者にとって負担の少ないものにする可能性があります。
引用: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
キーワード: 乳がん治療, ナノ医療, 光熱療法, 標的化薬物送達, 化学動力学療法