Clear Sky Science · ja
微小ピペット抵抗モデリングに基づくロボット細胞輸送システム
顕微鏡なしで小さな細胞を移動する
現代生物学では、驚くほど単純な作業に依存することが多い。それはガラス管で単一の細胞を吸い取り、別の場所に置くという行為だ。これは不妊治療、胚凍結、細胞治療、基礎研究に不可欠である。しかし現在、この作業はほとんど常に大型の顕微鏡と、動作を逐一監視する高度に訓練された操作者を必要とする。本論文は、顕微視なしで液滴間を単一細胞で移動させられる新しいロボットシステムを説明しており、密閉された完全自動の「細胞ファクトリー」を実現して、より速く、より安価に、壊れやすい細胞へのダメージを減らしながら動作させる道を開く。
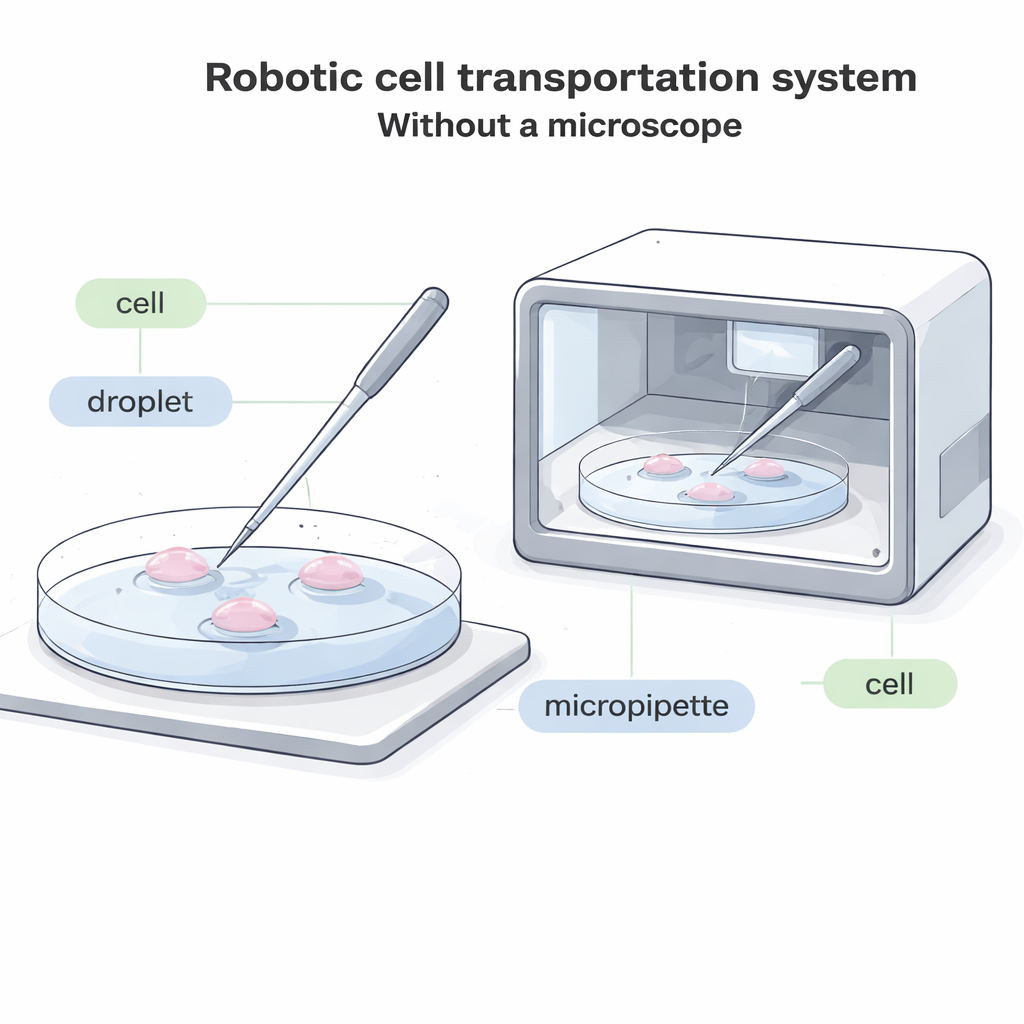
なぜ細胞移動は刷新が必要か
現在の研究室では、操作者が顕微鏡をのぞき、細いガラス管(マイクロピペット)を用いて皿底に着地させ、やさしく一つの細胞を吸引し、それを新しい液滴に移して押し出す。このプロセスは遅く、視覚的な負担が大きく、自動化が難しい。将来の多くのシステム――胚や他の細胞を箱の中で培養するようなコンパクトで密閉された装置など――では、従来型の顕微鏡を収めるスペースが十分にない。また、細胞が発光色素で標識されている場合、光で色素が消耗したり損傷したりするため、強い顕微観察を最小限にすることが重要である。既存の“ブラインド”システムは、画像に依存しないものの、異常に大きな細胞にしか使えず、一般的な細胞種の多くには良い自動化ソリューションが存在しない。
内蔵のストッパーを持つ特別なストロー
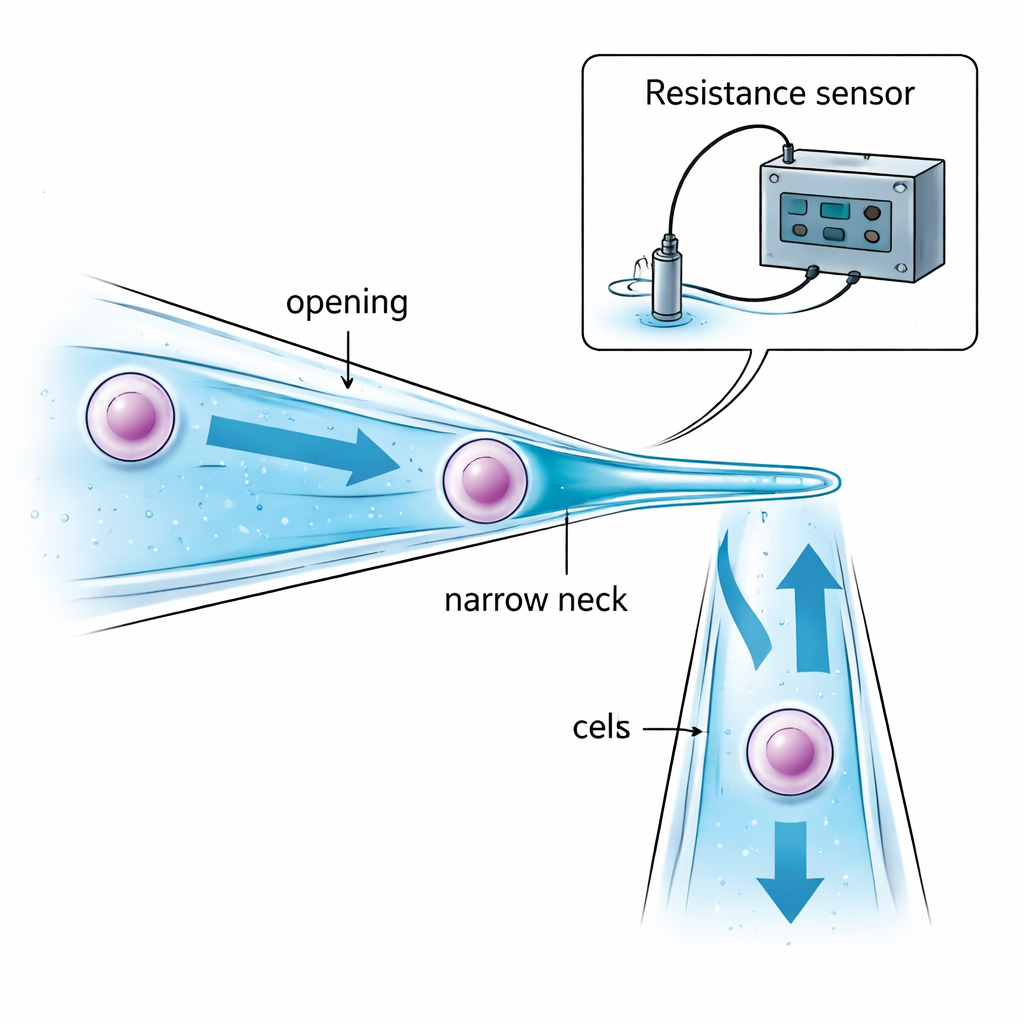
著者らはマイクロピペット自体を再設計してこの問題に取り組む。全長が均一な直管の代わりに、細い首を持つマイクロピペットを作成した。その開口部は標的細胞よりわずかに大きく、細胞が内部に引き込まれる。内部の深い位置で管はゆるやかに狭まり「ネック」を形成し、ネックの径は細胞より小さい。吸引がこの絞りに細胞を引き寄せると、細胞はチューブの内部で停止して保持される――液滴間で先端にぶら下がり、油や空気にさらされる代わりに。入口サイズ、ネック幅、両者の距離を慎重に選ぶことで、細胞を過度に圧迫せず確実に捕捉でき、さらに一滴から持ち込む液量を最小限に抑えて汚染を減らせる。
見る代わりに電気信号を聞く
顕微鏡がない状態でも、ロボットは次の三つを知る必要がある:ガラス先端が皿底に十分近づいたとき、細胞がネックで確実に捕捉されたとき、そして新しい液滴に完全に放出されたとき。チームはこれを、マイクロピペットの内外の液体に生じるごく小さな電気抵抗の変化を監視することで解決した。斜めに近づくピペットが皿底に近づくにつれ、両者間の液体ギャップが縮まり、電気抵抗が予測可能な形で上昇し、接触直前の安全な着地を知らせる。細胞が狭いネックで通路を塞ぐと、液体を通る電気経路が絞られて抵抗が急上昇し、細胞が押し出されると抵抗は急激に低下する。これらの「ギャップ」「吸引」「注入」抵抗の数学モデルにより、コンピュータはこれらの信号をリアルタイムで解釈し、視覚フィードバックなしに吸引や加圧を停止すべき時を判断できる。
ロボットの実地試験
この手法が実際に機能するかを確かめるため、研究者らは運動制御、圧力制御、抵抗検出、ホストコンピュータを統合した完全なロボット装置を構築した。彼らは直径約10マイクロメートルの小型がん細胞(HeLa細胞)と、直径約150マイクロメートルのより大きなブタ卵細胞で試験した。システムは幅広いピペットサイズで、着地、捕捉、放出を抵抗信号のみで確実に検出できた。直接比較では、ロボットはHeLa細胞を90%の成功率で移動させ、既存の画像ベース自動法より良好であり、ブタ卵は95%の成功率で輸送し、従来の顕微鏡法より高い成果を示した。細胞あたりの操作時間は人手による方法と同等か短く、主な理由は狭いネックにより細胞位置決めのための吸引の微調整を繰り返す必要がなくなるためである。
細胞の生存を守りつつスケールアップする
生物学実験室のどんなロボット補助も、扱う細胞を傷つけないことが必須である。新しいシステムで輸送した後、HeLa細胞とブタ卵細胞は1日培養され、生存細胞のみが発光する色素で染色された。新手法の生存率は、従来の顕微鏡ガイド移送や未処理の対照細胞と同等かほぼ一致し、ネックでのやさしい機械的な圧迫はしきい値を正しく設定すれば細胞生存率を著しく低下させないことを示している。展望として、同じ抵抗ベースのセンシングと圧力制御をコンパクトなマイクロ流体チップに組み込むことが提案されている。これにより多数のチャネルを並列に動作させ、高スループットで密閉された細胞処理システムを実現し、不妊医療、細胞治療、自動化が難しい長期培養装置に適した運用が可能になる。
今後の細胞作業にとっての意味
非専門家向けの主要なメッセージは、単一細胞の移動がもはや顕微鏡越しに人が見続けることに依存する必要はない、という点だ。ガラス管の形状を注意深く設計し、周囲の液体を通る電気の流れを「聞く」ことで、ロボットは着地、把持、放出を感じ取ることができる――暗所や狭い空間でも。これにより、壊れやすいサンプルを保護し、臨床ワークフローを単純化し、ラボ品質の細胞操作を自動化された工場のような運用に近づける密閉型の自律的細胞培養システムを設計しやすくなる。
引用: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
キーワード: 細胞操作, マイクロピペット, ロボット工学, マイクロ流体, 自動化