Clear Sky Science · ja
マイクロ生理学的システムにおける細胞の空間配置を制御するための戦略
研究室で小さな組織をつくる
私たちの臓器が高い機能を発揮するのは、細胞がランダムに散らばっているのではなく、空間的に精密に配列されているからです。本稿は、科学者たちが「オルガンオンチップ」やその他の小型の試験管内組織でその精緻な秩序を再現する方法を学んでいる過程を探ります。異なる細胞の位置や相互作用を導くことで、研究者は心臓、脳、腸、血管、さらにはヒト—微生物の生態系に至るまで、より現実に即したモデルを構築できます。こうした高度なシステムは、安全な薬剤試験、動物実験の削減、疾患研究や個別化治療の開発に役立つ道具を提供することが期待されます。
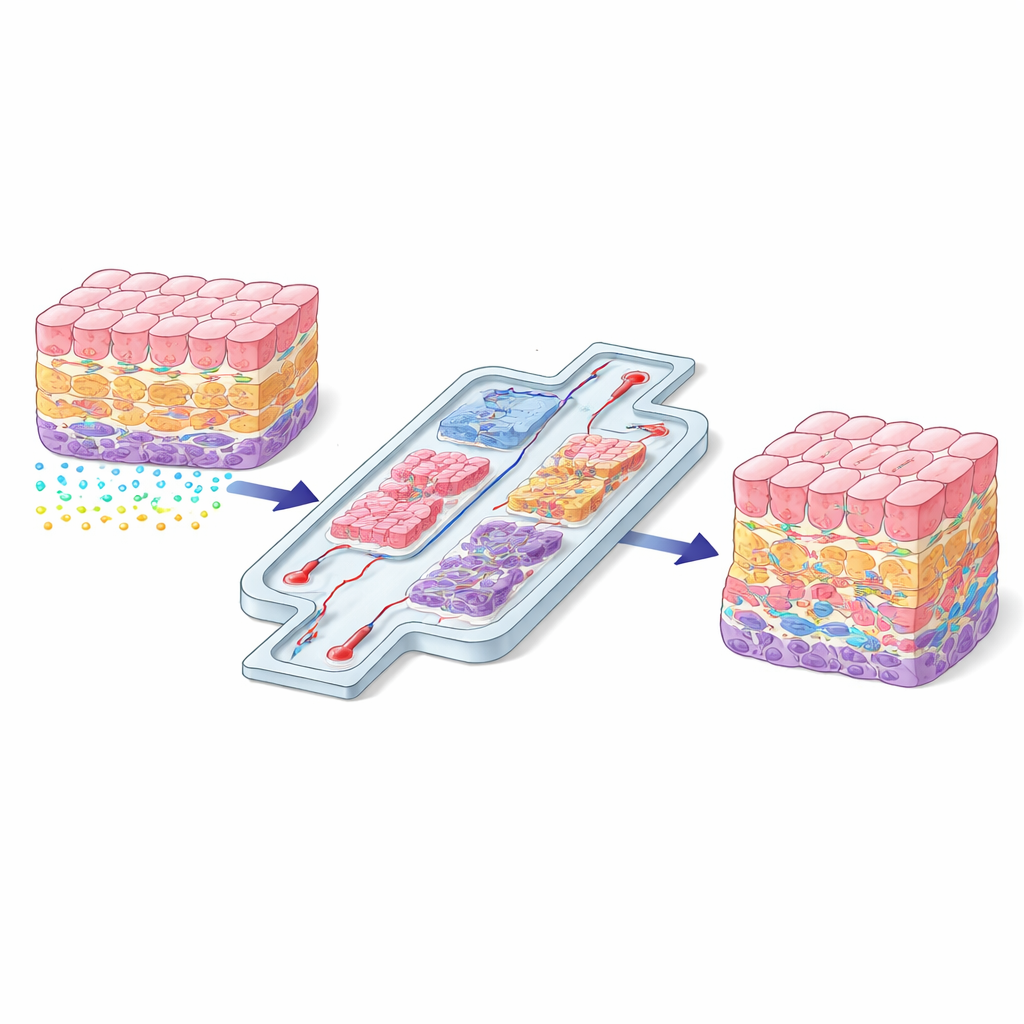
なぜ細胞の位置が重要か
体内では、すべての細胞が特定の「近隣環境」に住んでおり、そこには支持構造、化学シグナル、物理的な力が混在しています。血管の近くにいる肝細胞は、臓器の奥深くに埋もれた細胞とはまったく異なる手がかりを受けます。これらの位置差は、細胞の増殖、分化、傷害や薬剤への反応を決定づけます。平らなプラスチック培養皿で細胞を育てると、その空間的な“会話”はほとんど失われ、細胞は不自然な振る舞いを示すことが多いのです。本稿は、現実的な空間配置を再現することはオプションではなく、試験管内組織が実際の臓器を模倣するための基本要件であると論じています。
細胞を配列する二つの主要アプローチ
著者らは現在の戦略を大きく二つの系統に分類しています:直接的制御と間接的制御。直接的手法は、細胞や区画を物理的に必要な場所に正確に配置します。例としては、細胞や軟らかいゲルを層状に配置する3Dバイオプリンティング、組織を連結チャンバーやチャネルに区切るマイクロ流体チップ、光・音・磁気・電場を用いて細胞を所望の位置に誘導する物理的なトラッピング法があります。これらは、血液脳関門や層状の血管壁、腸から肝臓への流路の再現など、精密な幾何学が重要な場合に特に有効です。
細胞に周囲を読み解かせる
間接的手法はむしろ環境を再形成し、細胞自身にその場を整えさせます。ここでは、研究者が細胞が感知する“風景”を調整します:周囲ゲルの組成、表面の硬さやテクスチャー、増殖因子や薬物の溶解性濃度勾配などです。配置された支持分子は特定の細胞種を特定領域に定着させることができます。細胞が再構築するときに柔らかくなったりシグナルを放出したりするスマートハイドロゲルは、血管ネットワークや腸のクリプトや絨毛のような自己組織化構造を促します。マイクロ流体デバイスは安定した化学勾配を作り出し、幹細胞がチャネルに沿って異なる同一性を獲得したり、がん細胞と免疫細胞が異なるゾーンへ移動して病気の広がりを明らかにしたりします。
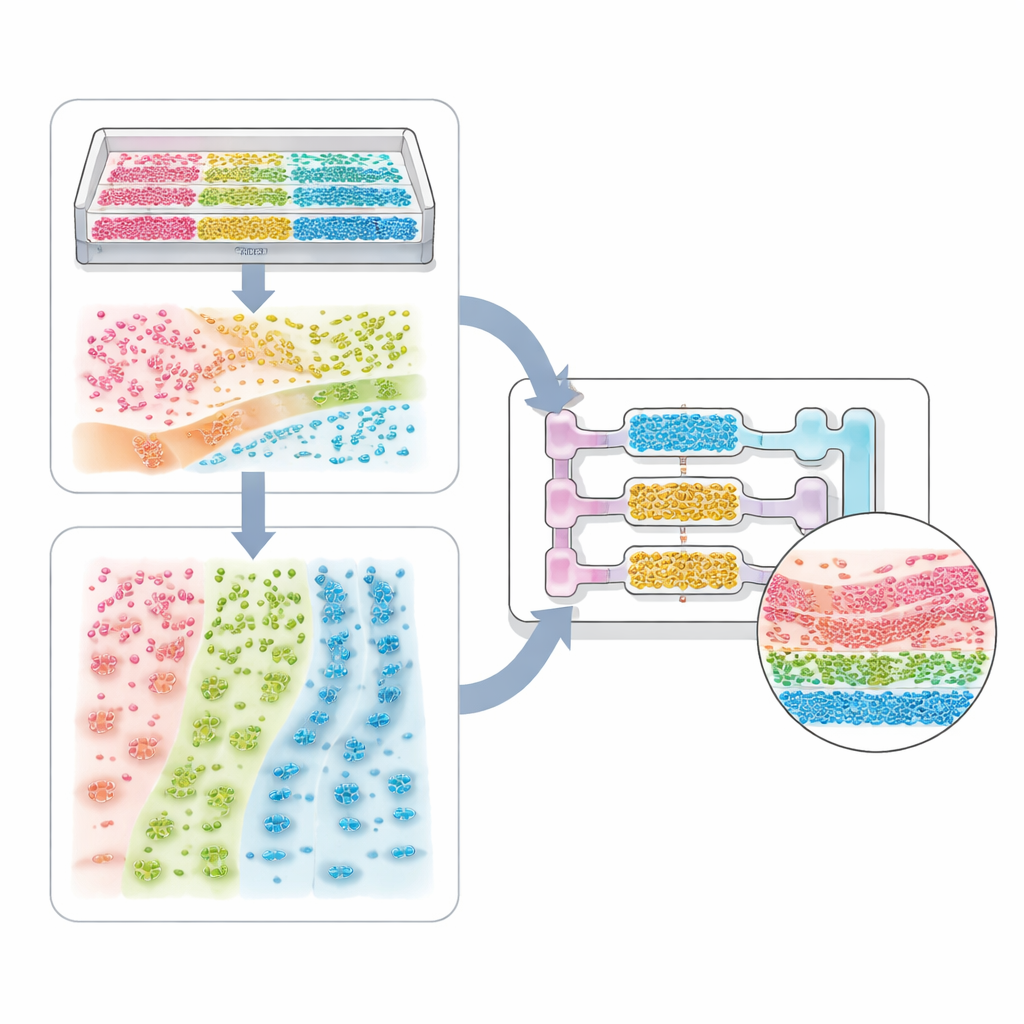
単一細胞系から全身モデルへ
レビューは応用のスペクトルを辿ります。最も単純な例は単一細胞種のシステムで、パターン化された溝や剛性勾配が心筋細胞を同調して拍動させたり、神経細胞の繊維を整列させたりします。より複雑な組織モデルでは、腫瘍細胞、支持細胞、血管細胞など複数の細胞種を混ぜて内部にコアとシェルを持つ球状体やオルガノイドを形成します。マイクロチャネルチップやバイオプリンティングは境界や流れを付与し、肺の空気嚢、腎臓の濾過構造、肝臓のゾーン、薬物の吸収・代謝・排除を追跡する多臓器回路の再現を可能にします。同じ考え方は宿主—微生物系にも適用され、腸壁に沿った細菌の空間配置や粘液層を挟んだ分布が、保護的か病原的かを左右します。
配置が本物であることを検証する
これらのシステムがより複雑になるにつれ、細胞が適所に配置され、意図したとおりに機能しているかを確認する信頼できる手段が必要です。本稿は、生きた細胞の動きや変化を時間経過で観察できるイメージング法、各位置でどの遺伝子・タンパク質・代謝物が現れているかをマッピングする高度な染色やシーケンシング技術を強調します。チップに埋め込まれたセンサーは酸素、栄養素、酸性度、機械的力を追跡し、局所条件と細胞応答を結びつけます。これらのツールを組み合わせることで、設計が視覚的に説得力があるだけでなく、機能的にも実際の組織に忠実であることを検証できます。
この研究の行き先
著者らは、最も強力なシステムは直接的手法と間接的手法を融合させるだろうと結論づけています:チップやバイオプリンターで全体のレイアウトを定め、その上に調整可能なゲル、テクスチャー、勾配を重ねて組織が成熟し時間とともにリモデリングできるようにする、というアプローチです。また、製造のスケールアップ、ラボ間のばらつきの低減、複雑なヒト組織モデルに関わる倫理的問題など、実際的な障害にも言及しています。それでも伝えたいメッセージは明確です:空間的組織化を習得することが、マイクロ生理学的システムを人間の臓器の信頼できる代替物に変え、発生の研究、治療法の試験、個別化医療の道を開く鍵であるという点です。
引用: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
キーワード: オルガンオンチップ, 細胞の空間配置, 3Dバイオプリンティング, マイクロ流体組織モデル, マイクロ生理学的システム