Clear Sky Science · ja
攻撃性の高いB細胞リンパ腫におけるMCL-1阻害とCAR-T療法の合成致死性
がん治療にとって重要な理由
攻撃性の高いB細胞リンパ腫は増殖の速い血液がんで、治療後に再発することが多くあります。患者自身の免疫細胞を再プログラムしてがんを攻撃させる強力な新手法であるCAR-T細胞療法でさえ、時間の経過とともに約半数の患者で効果が失われます。本研究は、その弱点を強みに変える方法を探ります:リンパ腫細胞が依存する重要な生存タンパク質を標的とする薬剤を用いて腫瘍を殺すと同時に、残存する細胞をCAR-T細胞が撃破しやすい状態にする、という考えです。
しつこいリンパ腫細胞の問題
攻撃性の高いB細胞リンパ腫はしばしばMYCという遺伝子の過剰な活性によって駆動され、細胞分裂を加速すると同時に免疫から逃れるのを助けます。標準治療やCAR-T療法でも、薬剤に耐える小さな細胞集団が残り、後に再発を引き起こすことがあります。これらの“パーシスター”や耐性細胞は、キラーT細胞の働きを抑える免疫抑制的な細胞で混み合った腫瘍の近隣に生き延びます。著者らは、リンパ腫細胞が自己破壊を回避するために依存するタンパク質であるMCL-1を阻害することで、このシステムの隠れた弱点を露呈できるかを問いかけました。
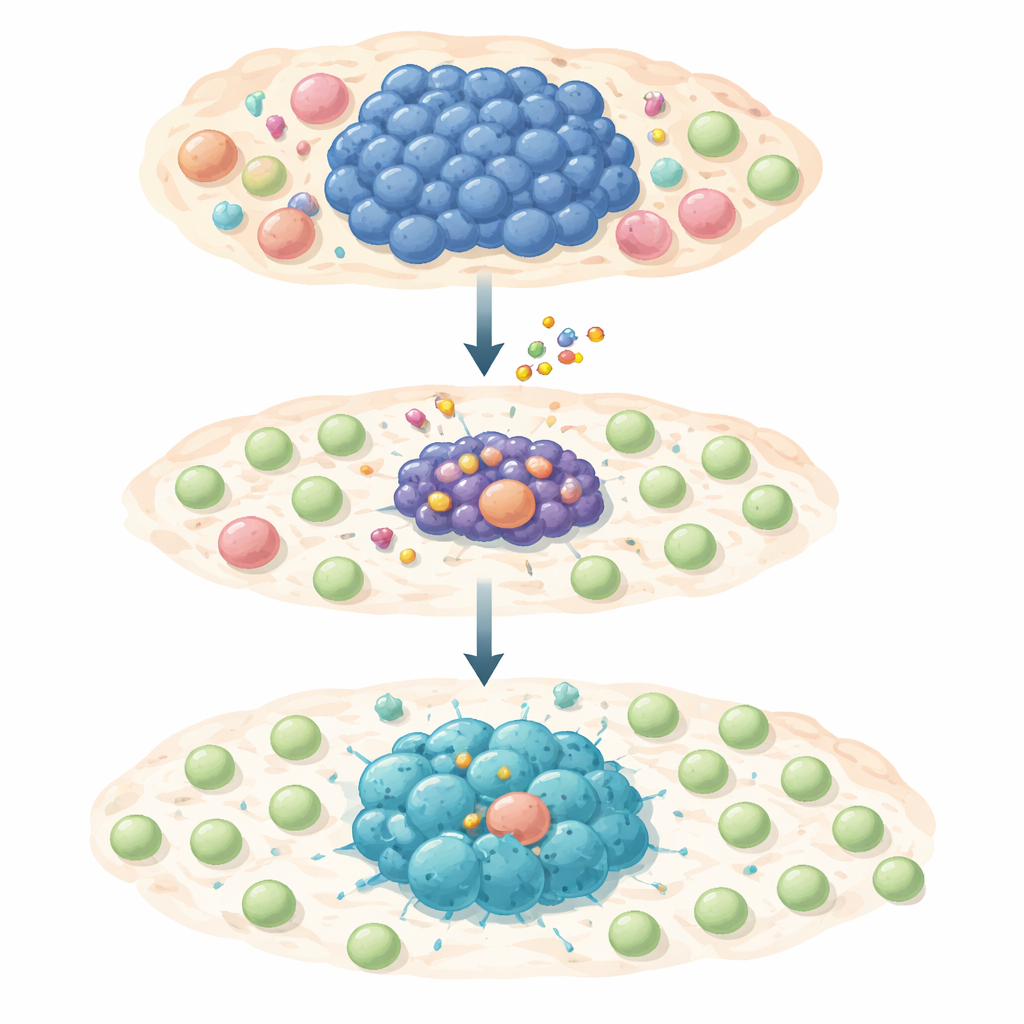
腫瘍の生存と隠れ場所を同時に攻める二段構え
研究チームは、選択的なMCL-1阻害薬S63845をMYC依存のヒトリンパ腫細胞株パネルで検証しました。これらのがん細胞の多くは薬剤に高度に感受性で、MCL-1を阻害されるとプログラム細胞死を起こしました。ただしごく一部は短期または長期曝露に耐え、薬剤耐性または耐性化した集団として生き残りました。生存細胞を詳しく調べると、MYC活性は低下する一方で、別の分子であるSTAT1とそれに連なるインターフェロン警報経路がオンになっていました。この変化は、炎症シグナルやケモカインを駆動する遺伝子を活性化し、T細胞を腫瘍領域に呼び寄せる“フレア”を生むことになりました。
免疫の近隣を再活性化する
この現象を生体で確認するために、著者らはMYC駆動性リンパ腫を有するマウスに低用量のMCL-1阻害剤を投与しました。薬剤は正常B細胞を残しつつ腫瘍負荷を縮小しましたが、その効果は単なる腫瘍縮小にとどまりませんでした。処置を受けた腫瘍ではCD4およびCD8 T細胞が増加し、疲弊したT細胞や制御性T細胞、抑制的な骨髄系細胞が減少しており、より免疫に寛容な環境が形成されていました。腫瘍と周辺細胞の単一細胞RNAシーケンスは、残存するリンパ腫細胞がMYC低下、STAT1上昇、インターフェロンおよび炎症シグナルの強化を示す一方で、周辺組織は抑制的な細胞ではなく活性化したT細胞やナチュラルキラー細胞で再充填されていることを確認しました。
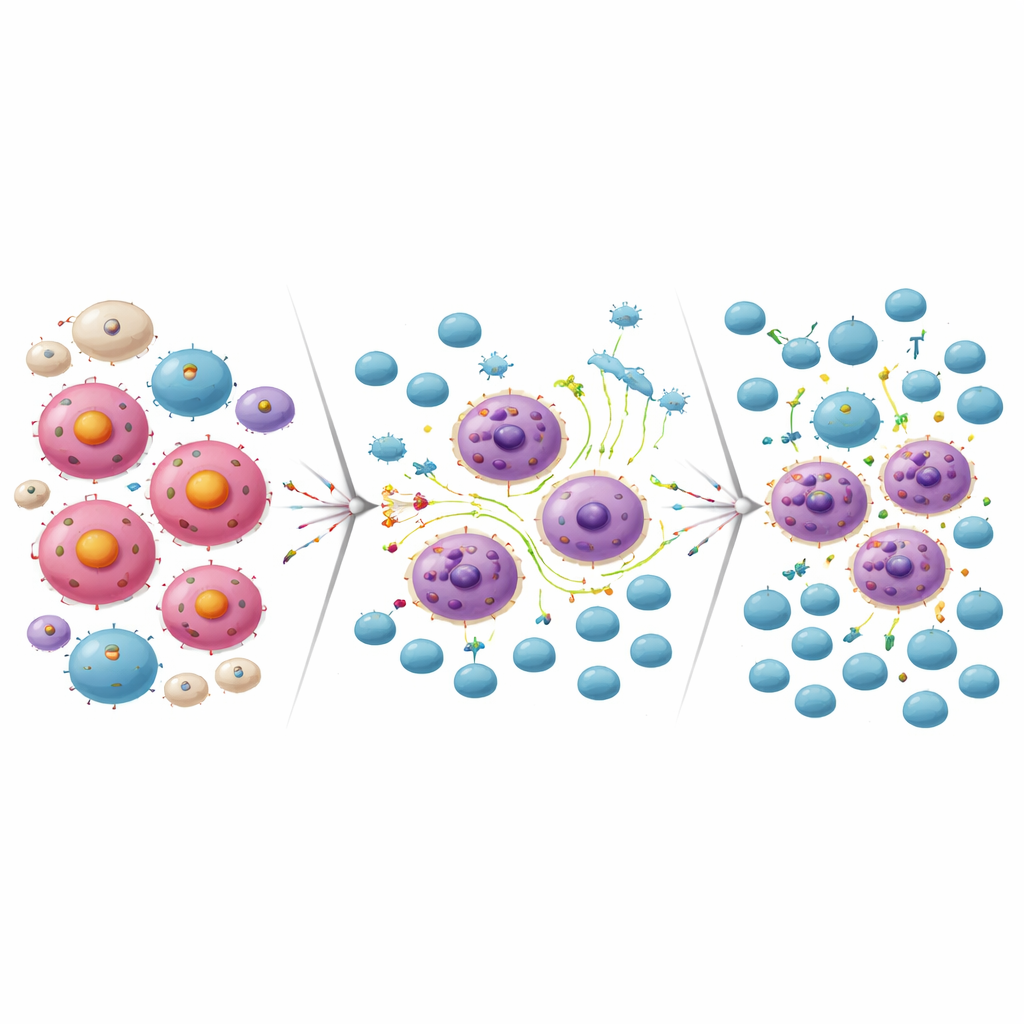
耐性をCAR-T細胞の突破口に変える
MCL-1阻害による同じ炎症性の再プログラミングは、一部のリンパ腫細胞を生き残らせる一方で免疫攻撃に対して脆弱にしました。実験室内では、CD19を標的とするCAR-T細胞がMCL-1阻害薬に耐性化したリンパ腫細胞を効率的に殺しました。逆に、CD19 CAR-T療法に耐性化したリンパ腫細胞はMCL-1阻害剤に対して高い感受性を示しました。研究者らが細胞培養でサブ致死量のMCL-1阻害剤とCAR-T細胞を組み合わせると、両者を単独で用いるよりもはるかに多くのリンパ腫細胞が根絶されました。マウスモデルでも、MCL-1阻害剤を投与した後にCD19 CAR-T細胞を与えると、単独治療に比べてほぼ完全な腫瘍消失と有意な延命が得られました。
治癒の可能性を持つワンツーパンチ
簡潔に言えば、本研究は「ワンツーパンチ」戦略を示しています。まずMCL-1を阻害する薬剤でほとんどのリンパ腫を叩き、残存するがん細胞を炎症化して可視化し、T細胞を引き寄せて保護的な免疫シールドを剥ぎ取ります。次にCD19ターゲットのCAR-T細胞がこの新たに露呈した弱点を突いて残存病変を根絶します。腫瘍の内部の生存配線と保護的な周辺環境の両方を同時に攻撃することで、この併用アプローチは再発を減らし、攻撃性の高いB細胞リンパ腫を長期寛解に近づける可能性があります。
引用: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
キーワード: B細胞リンパ腫, CAR-T療法, MCL-1阻害, 腫瘍微小環境, 薬剤耐性