Clear Sky Science · ja
可溶性ノッチ作動薬はヒトアメロブラストの成熟とエナメル様組織形成を促進し、歯再生への道を開く
なぜ歯のエナメル修復は難しいのか
エナメルは歯を覆うガラスのような白い殻であり、人の体の中で最も硬い組織です。しかし一度失われると自然には再生しません。成人の90%以上が何らかのエナメルの喪失や損傷を抱えていますが、歯はこの保護層を再構築する手段を持っていません。本研究は、ヒトのエナメル産生細胞を実験室で増やし、それらを完全に成熟させ、動物体内でエナメル様の鉱物を形成させる方法を示します。この成果は、将来的に詰め物やクラウンの代わりに生体組織で歯を修復する治療への道を開くものです。
幹細胞からエナメルをつくる
エナメルはアメロブラストと呼ばれる特殊な細胞によって作られますが、歯が歯茎を突き破って萌出するとこれらの細胞は消失します。そのため成人の歯は新しいエナメルを作れません。研究者たちは、成人細胞を胚に似た可塑性のある状態に戻したヒト誘導多能性幹細胞(iPS細胞)を使って「誘導アメロブラスト」を作成しました。以前の研究では、これらの培養細胞はエナメルを作る細胞に似始めるものの完全な成熟に至らず、基底の象牙質を形成するオドントブラストと密接に接している場合にのみ適切に機能しました。ここから生じた重要な疑問は、オドントブラストがアメロブラストの最終成熟に必要な何を提供しているのか、という点でした。
歯細胞間で欠けている対話
この細胞間の対話を解読するために、チームは発生中のヒトおよびマウス歯の単一細胞遺伝子発現マップを解析しました。エナメルが形成される重要な時期に、オドントブラストからアメロブラストへ特異的に働くように見えるシグナル経路を探索しました。際立った経路が見つかりました:ノッチ経路です。ノッチは胚発生で広く使われる直接的な細胞間コミュニケーションシステムです。これらの歯のマップでは、デルタ様リガンド(特にDLL1およびDLL4)が主にオドントブラストに見られ、ノッチ受容体は成熟中のアメロブラストに集中していました。研究者たちが共培養系で薬剤を用いてノッチ活性を遮断すると、アメロブラストは主要なエナメルタンパク質であるエナメリンの産生を著しく減少させました。これは、ノッチシグナルがエナメル形成細胞の成熟に不可欠であるという強い証拠です。 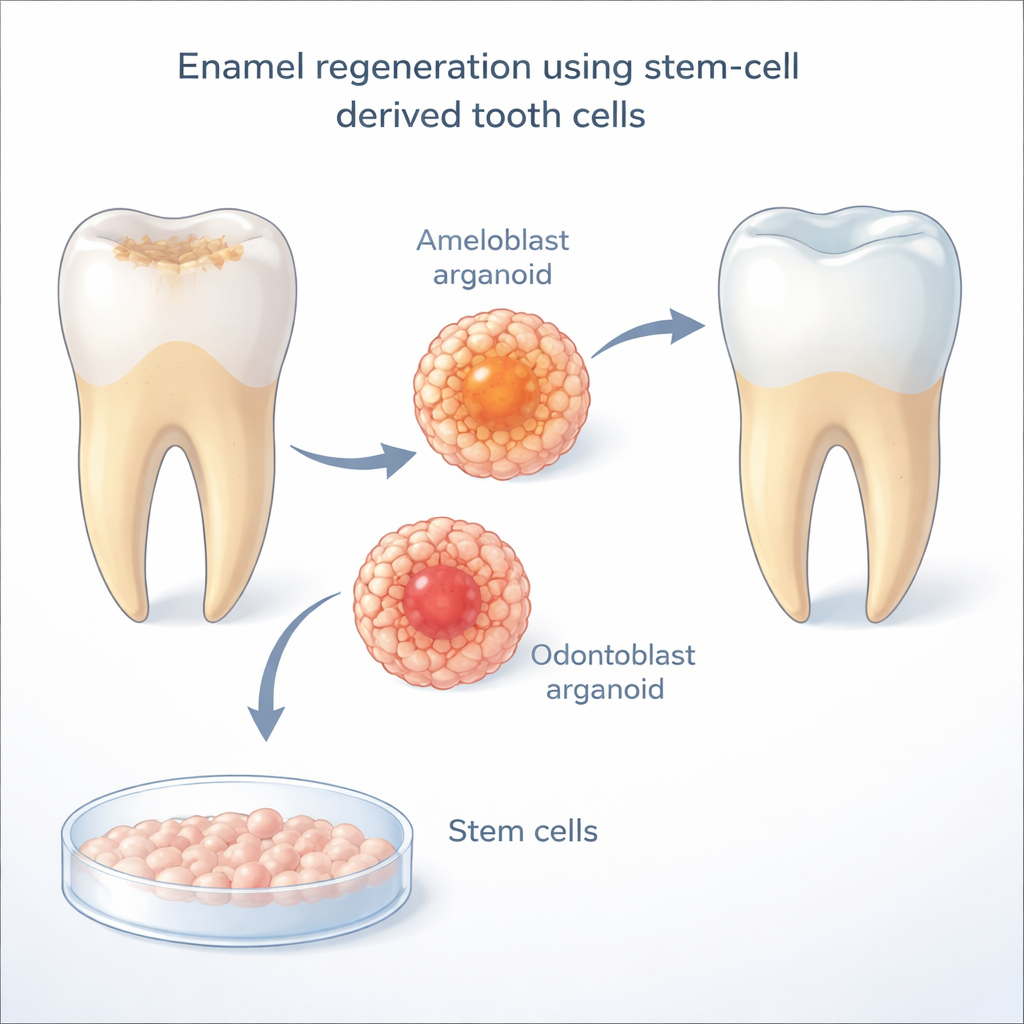
エナメル細胞のためのAI設計タンパク質スイッチ
さらに進めるために、チームは実際のオドントブラストに頼らずにノッチを精密に制御してオンにできる手段を求めました。彼らは計算ツールで設計された人工タンパク質C3‑DLL4を用いました。この可溶性分子はDLL4のシグナル領域を3コピー、剛直な三腕構造に配列し、天然の隣接細胞のようにノッチ受容体をクラスター化して活性化できます。レポーター細胞株では、C3‑DLL4はノッチ依存遺伝子を強くオンにしました。初期のアメロブラストオルガノイド(幹細胞から育てた小さな3次元細胞クラスター)に添加すると、遺伝子発現は大きく変化し、未熟なプロファイルから分泌型および完全に成熟したアメロブラストに一致する状態へと移行しました。AMELX、ENAM、MMP20、ODAM、KLK4、TUFT1、WDR72などの特徴的な遺伝子が活性化されました。逆にノッチ活性を除くと成熟が停滞し、エナメルタンパク質の産生が乱れました。
オルガノイドからエナメル様組織へ
驚くべきことに、ノッチ活性化されたアメロブラストオルガノイドを免疫不全マウスの腎被膜下に移植すると(ヒト組織を試験するためによく使われる栄養が豊富で安全なニッチ)、濃密な鉱物化物質の沈着が始まりました。高解像度のマイクロCTスキャンと古典的な骨染色法は、通常その場所に存在しない石灰化小結節の存在を確認しました。顕微鏡観察では、主要なエナメルタンパク質とWDR72(適切なエナメル鉱化に関連する因子)を発現する組織化され極性をもったヒト細胞層が示されました。この物質は完全な天然エナメルというより「エナメル様」と表現するのが適切ですが、設計したヒトアメロブラストが生体内で硬い鉱物を堆積できることを示しています。 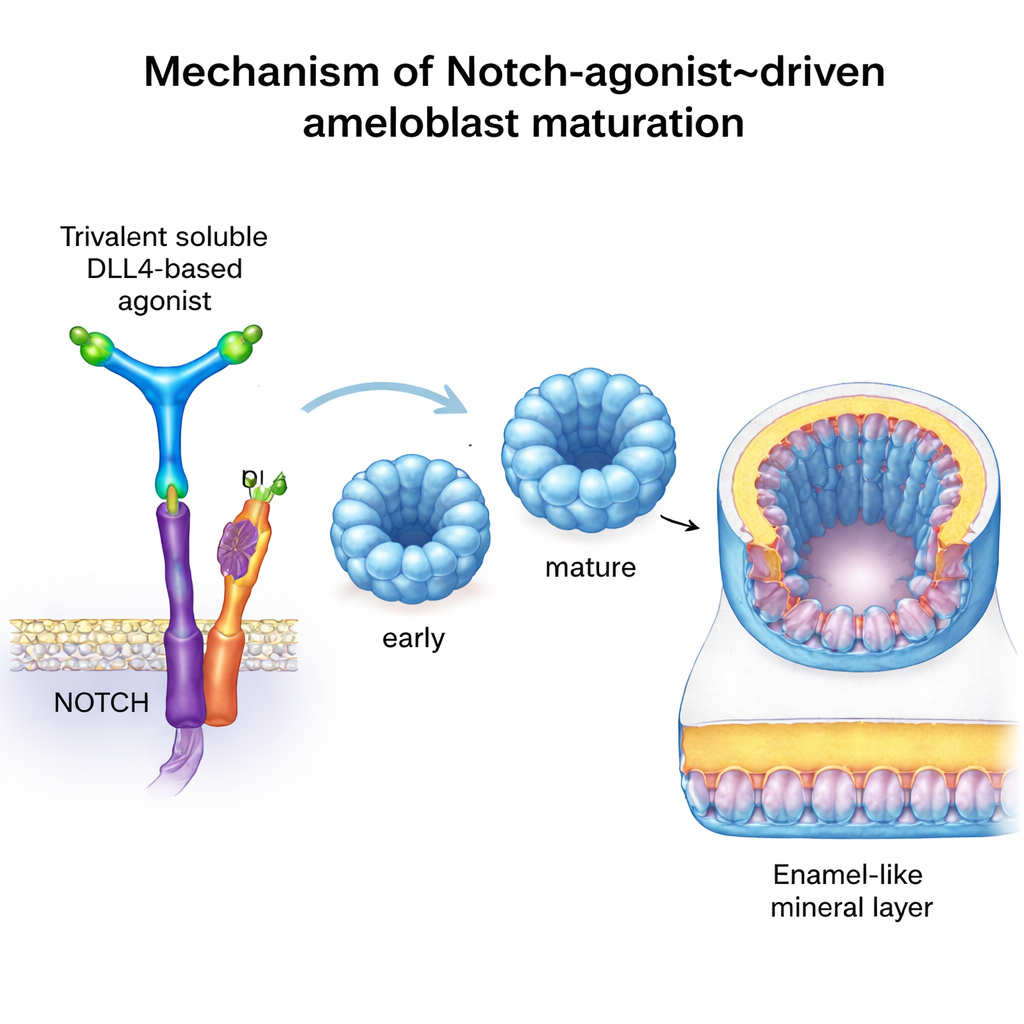
弱いエナメルの遺伝的謎を解く
本研究は、DLX3と呼ばれる遺伝子にまつわる長年の謎にも取り組んでいます。この遺伝子の変異は特定の遺伝性エナメル欠損を引き起こし、虫歯のリスクを高めます。DLX3はアメロブラストとオドントブラストの両方で活性を持つため、どちらの細胞型が主に影響を受けるのか特定が難しい問題でした。オドントブラストを介さないオルガノイド系とCRISPR遺伝子編集を使い、研究者たちはアメロブラスト系統で特異的にDLX3を除去しました。アメロブラスト形成の初期段階は進行しましたが、最終の成熟段階は崩壊しました:エナメリン、AMELX、MMP20、KLK4、TUFT1、WDR72といった主要なエナメルタンパク質がRNAおよびタンパク質レベルの両方で劇的に減少しました。これはDLX3がヒトアメロブラスト内部でエナメル形成プログラムを完了するために直接必要であることを示し、この遺伝子近傍の変異が脆弱で虫歯になりやすい歯と関連する理由を解き明かします。
将来の歯科医療にとっての意義
これらの発見は、幹細胞からエナメル産生オルガノイド、さらにin vivoでのエナメル様組織へ至る段階的なロードマップを示しています。これは調整可能なノッチ「オン・スイッチ」とDLX3遺伝子によって制御されます。臨床的な歯の再生はまだ遠い目標ですが、本研究は遺伝性歯疾患の理解、新規治療のスクリーニング、失われたエナメルを不活性な材料ではなく生きた細胞で再構築する戦略の改良に向けた強力な試験場を提供します。患者にとっての長期的な希望は、将来歯科受診が磨耗や虫歯の歯をより本物に近い生体工学的エナメルで修復することを伴うようになることです。
引用: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
キーワード: エナメル再生, アメロブラストオルガノイド, ノッチシグナル伝達, DLX3, 歯科幹細胞