Clear Sky Science · ja
マイクロRNA処理機構における疾患関連変異の構造的洞察
小さなRNAのハサミが健康と病気をどう形作るか
すべての細胞の中には、遺伝情報が読み取られる前にそれを切り整える隠れた編集システムがあります。このシステムはマイクロRNAと呼ばれる小さなRNA断片に依存しており、何千もの遺伝子の微調整つまみのように働きます。マイクロRNAを作る分子「機械」が正常に働くと、細胞は制御された形で増殖し、分化し、機能します。しかし、これらの機構が変異で損なわれると、遺伝子活動のバランスががんや造血不全、脳の発達障害に傾くことがあります。本稿では、これらの機械の3次元構造を理解することが、何がどのように壊れるのか、そしてそれをどう修復できるかを突き止める手がかりになることを説明します。
細胞の遺伝子“減光”ツールキット
マイクロRNAは約22塩基程度の短いRNAで、自身がタンパク質をコードするわけではありません。代わりに、長いメッセンジャーRNAに結合して、それらを分解へ導いたり翻訳を阻害したりして、遺伝子の働きを完全にオフにするのではなく下げる働きをします。マイクロRNAを作るために、細胞はより長いRNA前駆体を段階的なアセンブリラインに通します。まず核内で酵素DROSHAが一次転写産物を切り、短いヘアピン状の断片にします。これらは細胞質へ移動し、そこで別の酵素DICERがヘアピンの末端をはかり取り、マイクロRNAサイズの二本鎖に切断します。最後に、その二本鎖の一方の鎖がArgonaute 2(AGO2)と呼ばれるタンパク質に搭載され、AGO2はマイクロRNAをガイドとして用いて一致するメッセージを見つけ出してサイレンシングします。 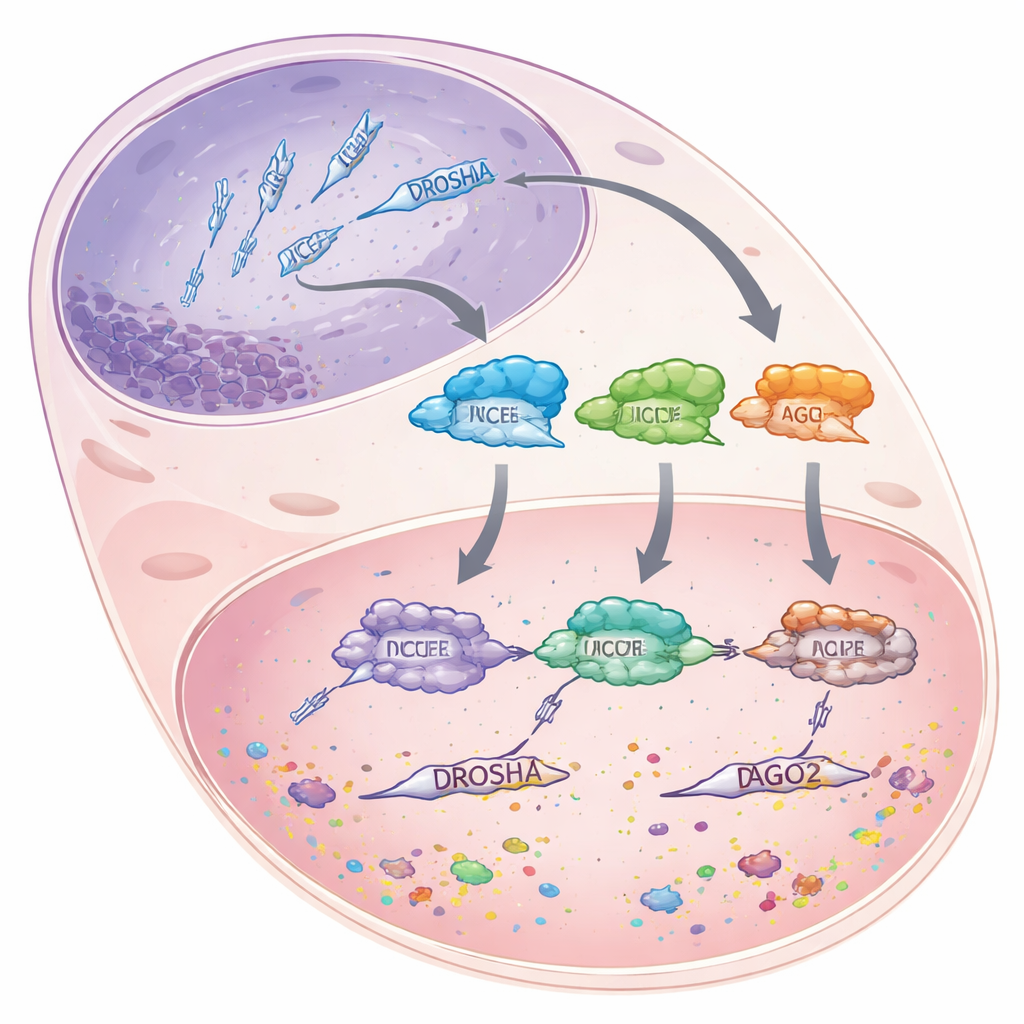
精密な仕事を担う繊細な形状
DROSHA、DICER、AGO2は単純なハサミではなく、それぞれ複数の相互作用するパーツで構成され、これらが振付のように動く必要があります。DROSHAはパートナータンパク質DGCR8と協働して一次マイクロRNAヘアピンの末端を把持し、正確にどこを切るかを判断します。DICERはドメインによって形成される一種の内蔵定規を使い、ヘアピン末端を把持する場所と触媒中心が切断する場所との間に一定の距離を設定します。AGO2は単一のマイクロRNA鎖を包み込み、その“シード”領域を標的認識に最適な形で露出させ、一方で金属イオンと主要なアミノ酸がコア内に整列して塩基対が十分に強いときに標的を切断します。三者に共通して、正に帯電した溝や柔軟なリンカーがRNA鎖を位置決めし、金属結合ポケットや触媒残基が化学的切断を行います。
ハサミが曲がったり鈍ったりしたとき
がん、血液疾患、神経発達症候群の患者を対象とした遺伝学的研究は、これらのマイクロRNA機械に変異が集中していることを明らかにしています。最も有害な変化の多くは触媒中心やRNAを厳密に把持する表面に直接位置します。例えばDROSHAでは、E1147KやD1219Gのような置換が切断部位の中心にあり、必須の金属イオンを保持する能力を損なって一次マイクロRNAを処理できなくします。切断領域を失うトランケーションや支持ヘリックスを不安定化する変化など、他のDROSHA変異は複合体全体を弱め、Wilms腫瘍、骨髄疾患、神経系疾患でマイクロRNAレベルの全般的な低下を引き起こします。DICERでは、繰り返し見られる変異が二つの切断ドメインのうちの一方に集まり、マイクロRNA二本鎖の一方の腕が失われるように産生を歪め、それが増殖促進と抑制のシグナルのバランスを変えます。 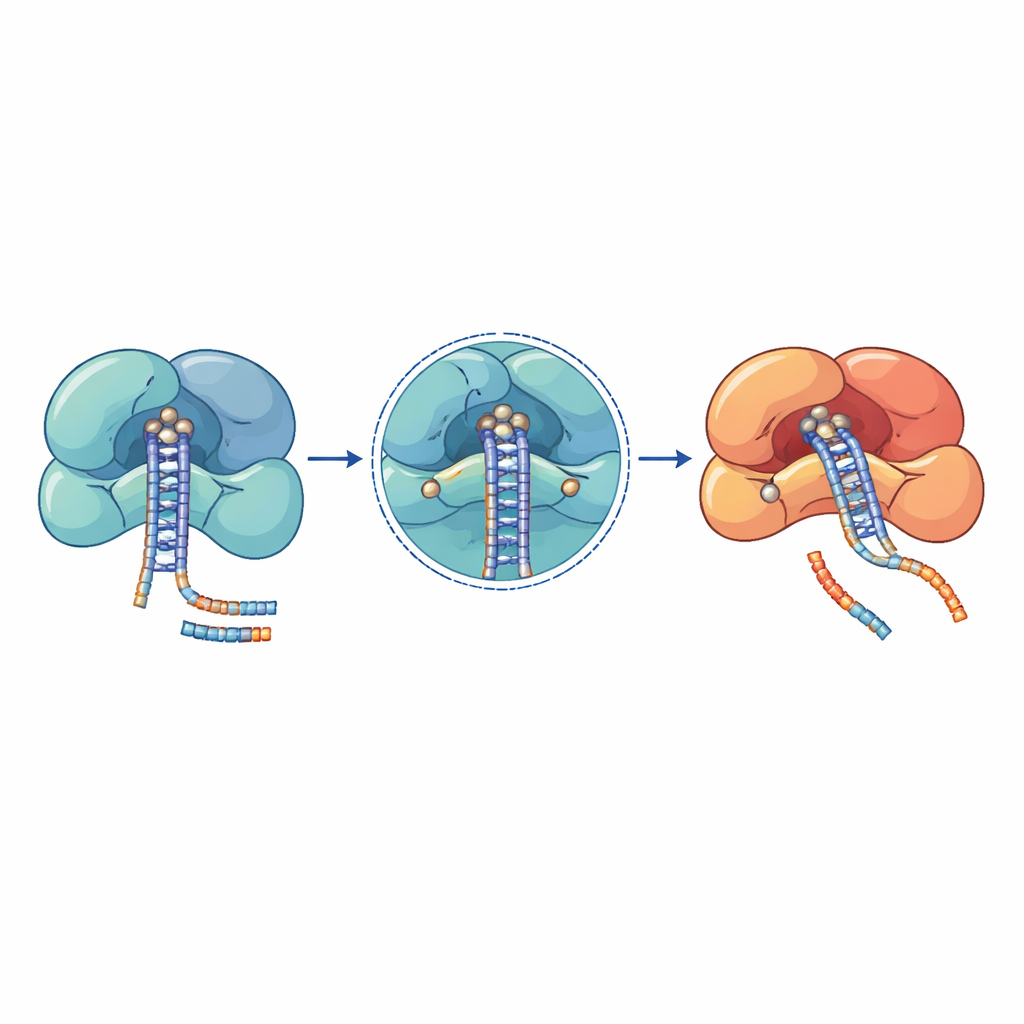
脳をはじめとする部位でのずれたガイド
AGO2変異は異なるが関連した物語を示します。触媒コアへの直接的な打撃は稀で、発生の早期に致命的になりうるためと考えられます。代わりに、疾患と関連する変異は柔軟なリンカー領域やAGO2の形を保つドメイン接合部に現れる傾向があります。神経発達疾患であるLessel–Kreienkamp症候群では、これらのリンカーや周辺表面の変異がPAZ、MID、PIWIといったAGO2の部分のパッキングや動きを微妙にねじります。これによりガイドとなるマイクロRNAがずれたり、標的RNAへの把持が弱くなったりして、脳発達における遺伝子サイレンシングの精度がぼやける可能性があります。マイクロRNA経路のどこで起きても—DROSHA、DICER、AGO2のいずれにせよ—類似した構造変化は波及し、細胞増殖、造血、ニューロン配線に関わる遺伝子ネットワーク全体を変えてしまうことがあります。
構造的手がかりを将来の治療へつなげる
疾患変異をこれらタンパク質の高分解能3次元地図上に重ねることにより、各変化がどのようにトラブルを引き起こすかを分類できます—切れ味を鈍らせるのか、パートナータンパク質との重要な接触を緩めるのか、主要なヘリックスをずらして整列を崩すのか、といった具合です。こうした構造的洞察は標的化された介入への道を開きます:弱まった界面を安定化する低分子、部分的に機能する酵素を正しい基質へ誘導する設計RNA、あるいは変異タンパク質をより活性な形に押しやるアロステリック化合物などです。一般の読者への要点は、細胞のRNAハサミにおける小さな構造的変化が健康に大きな影響を与えうる一方で、次世代の変異対応型治療を設計するための精密な取り手も提供するということです。
引用: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
キーワード: マイクロRNA, RNA干渉, DROSHA DICER AGO2, がん遺伝学, 神経発達障害