Clear Sky Science · ja
スネイル(Snail)タンパク質の安定性を調節する機構:ユビキチン–プロテアソーム系とシャペロン介在性オートファジー
がんの転移が脆弱なタンパク質にかかっている理由
がんが真に生命を脅かすのは、腫瘍の元の場所から細胞が離れて遠隔の臓器へ移動するときです。この広がり、すなわち転移は、細胞同士の結びつきを緩め移動性を高める強力な“マスタースイッチ”タンパク質であるスネイルに部分的に依存します。本稿では、細胞が通常どのようにしてスネイルを短命に保ち、二つの主要な廃棄システムを介して速やかに分解しているかを説明します。このバランスを理解することで、転移を遅らせたり防いだりする新たな手法が見えてきます。
密に詰まった細胞からさまよう侵入者へ
健常な組織では、上皮細胞は規則正しい層を形成し、隣接する細胞と強く結合してその場にとどまります。腫瘍細胞が脱出するには、しばしば上皮–間葉転換(EMT)と呼ばれる形質変換を経て、細胞間接着を失い移動・浸潤能力を獲得します。スネイルはこの変換の主要な駆動因子であり、核内に存在すると細胞間接着を維持する遺伝子を抑え、移動や浸潤を促す遺伝子を活性化します。スネイルの高発現は攻撃的ながんや患者予後不良と関連するため、細胞は通常の状態でスネイルを稀で短命に保つ仕組みを進化させてきました。
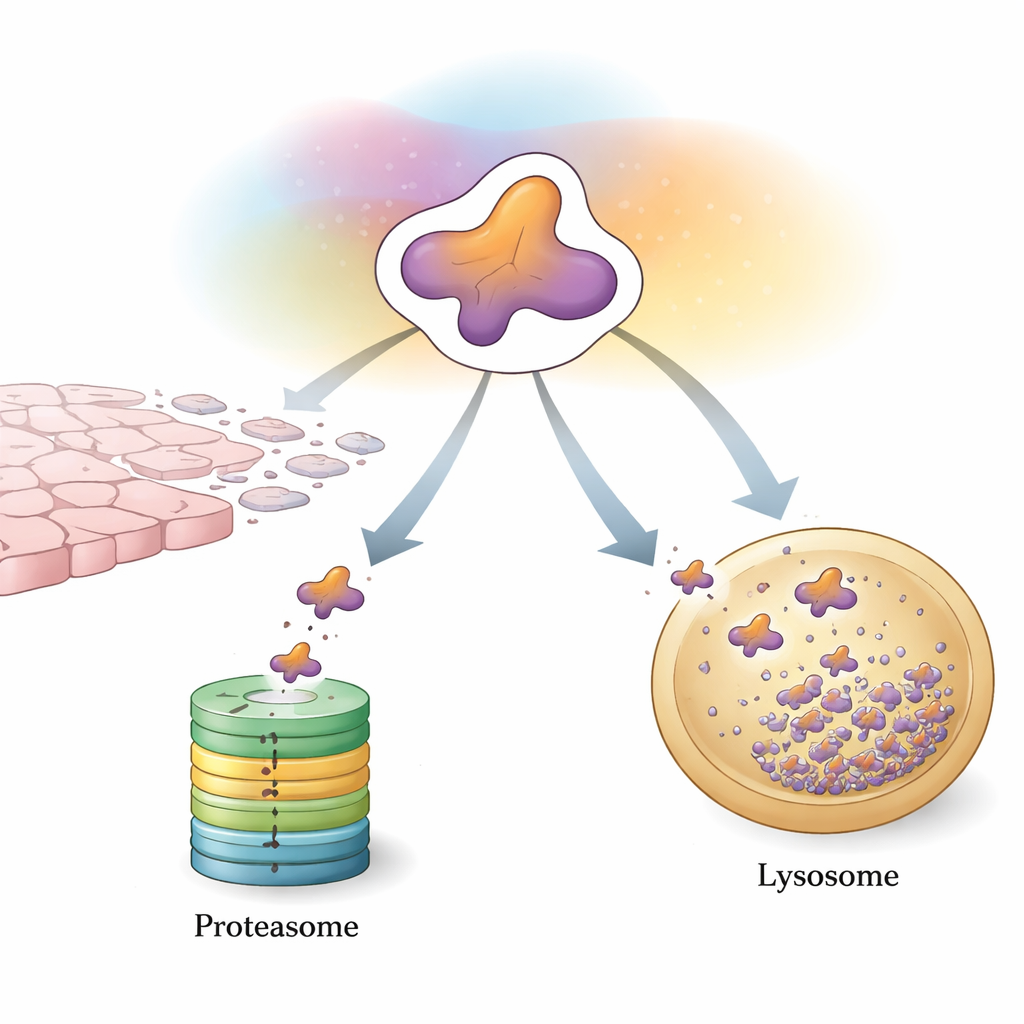
細胞の第一の制御線:タグ付けして粉砕する
細胞がスネイルを制御する主な方法の一つは、ユビキチン–プロテアソーム系です。不要なタンパク質をタグ付けして粉砕する機構です。特殊な酵素群がスネイルにユビキチンという小さな“旗”を付けます。一定のパターンで十分な数の旗が付くと、スネイルはプロテアソームへ誘導され、樽状の複合体がそれを断片化します。多くの補助タンパク質がこの過程を微調整します。ある酵素は分解を促進する鎖を付けてスネイルを速やかに粉砕器へ送ることで腫瘍の増殖や拡散を抑えます。一方で別の酵素はスネイルを安定化させたり遺伝子発現を間接的に高めたりして、EMTや転移の方向へバランスを傾けます。リン酸化やアセチル化といった化学的修飾は追加のスイッチのように働き、どの補助因子がスネイルに結合できるか、また分解されるか保存されるかを制御します。
ブレーキを解除する酵素:スネイルを救うもの
スネイルにタグを付けて終わりというわけではありません。脱ユビキチン化酵素と呼ばれる別の酵素群は、ユビキチンの旗を剥がしてスネイルをプロテアソームから救い出すことができます。これらの多くはがんで活性化されたり亢進したりしており、スネイルが分解を逃れて核内に持続することを可能にします。これらの作用は細胞の文脈に強く依存します:ある状況では直接的にスネイルを安定化させ、別の状況ではスネイルの細胞内局在や相互作用に影響を与えます。増殖因子やストレス応答などのがん関連シグナルはこのネットワークに入力し、スネイルが迅速に除去されるかEMTプログラムを駆動することが許されるかを決定します。
第二の安全網:細胞のリサイクルセンターへの選択的搬送
プロテアソームに加えて、細胞はオートファジーに依存し、タンパク質を酸性コンパートメントであるリソソームへ運んで分解します。本レビューは、シャペロン介在性オートファジー(CMA)として知られる高度に選択的な経路を、スネイル制御の第二の主要経路として強調します。CMAはスネイル内の短い配列を認識し、エスコートタンパク質の助けを借りて細胞質のスネイルをリソソームへ送り込み分解します。侵襲性の低い乳がん細胞ではこの系がスネイルを主に核の外にとどめ、リソソームによる除去を受けやすくします。より侵襲的なトリプルネガティブ乳がんでは、スネイルは核内に蓄積しCMAを回避する傾向があり、EMTと転移を引き起こす能力を強化します。
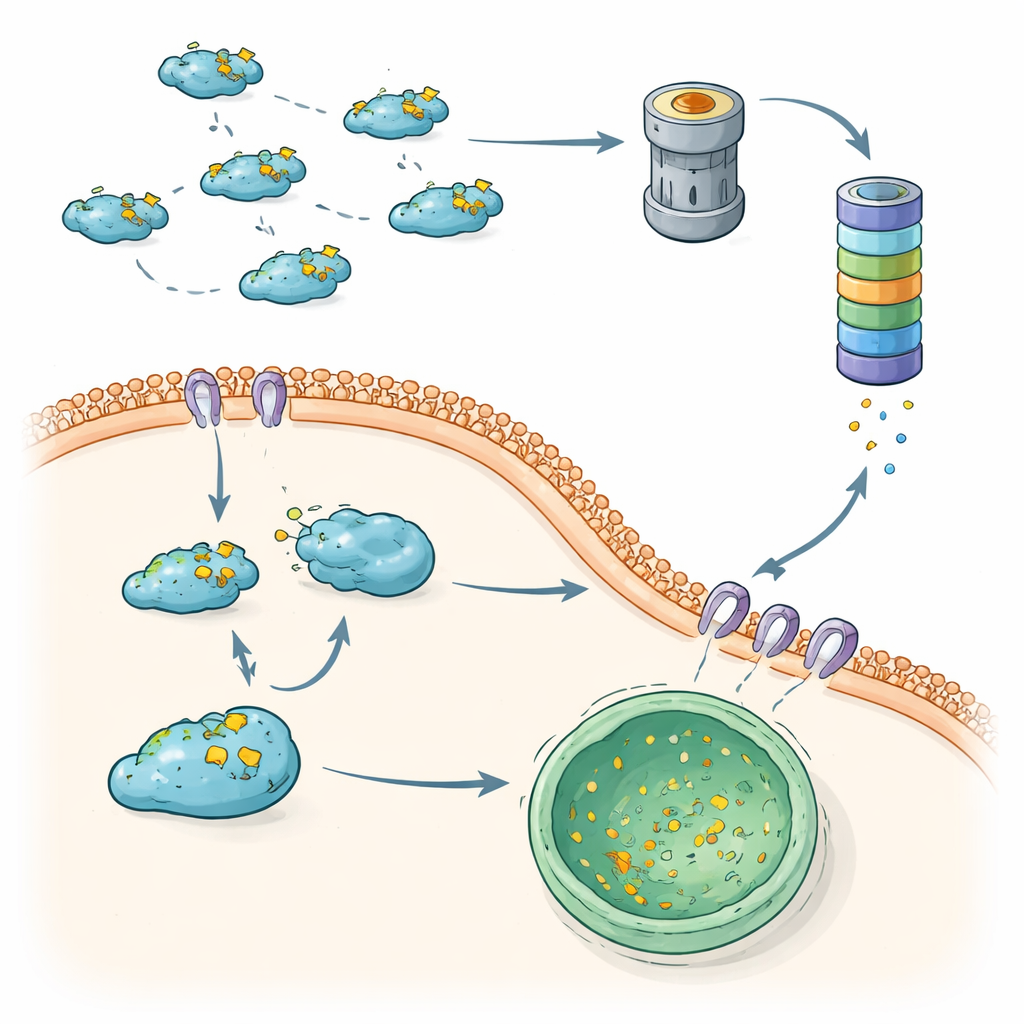
品質管理が失敗すると転移が進む
総じて、これらの知見は細胞がスネイルを抑制するために二つの補完的な「品質管理」軸、すなわちユビキチン–プロテアソーム経路とCMAに基づくリソソーム分解を用いていることを示します。両者が適切に機能しているとき、スネイルは速やかにターンオーバーされ、EMTが制限され腫瘍細胞の拡散を防ぎます。一方、タグ付け酵素、脱ユビキチン化酵素、またはCMA構成要素の変化でいずれかの軸が弱まると、スネイルはより安定化して核内に蓄積し、浸潤性の行動を強力に促進します。これら相互に関連する分解経路を地図化することで、スネイルの分解を回復・促進したり、スネイルをCMAやプロテアソームによる分解へ再誘導したりする薬剤が、これらの必須なタンパク質リサイクル系を完全に停止することなく転移のブレーキを再適用するための新たな治療可能性を提示します。
引用: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
キーワード: がんの転移, 上皮–間葉転換, スネイルタンパク質, タンパク質分解, オートファジー