Clear Sky Science · ja
酸化還元に敏感なタンパク質HMGB1:細胞内および細胞外での役割
形を変えるタンパク質が健康に重要な理由
ほぼすべての細胞の中に存在する小さなタンパク質HMGB1は、多機能ツールのように振る舞います。平常時には静かにDNAの整理を助けますが、細胞がストレスを受けたり損傷したりすると、HMGB1は核を出て周囲の組織に放出され、免疫系に対するアラーム信号として働くことがあります。本総説は、酸化によって引き起こされる微細な化学的変化がHMGB1をまったく異なる生物学的「性格」に変える仕組み—組織を保護するもの、炎症を促進するもの、慢性疾患に寄与するもの—を解説します。この分子の「ムードリング」を理解することで、免疫系を完全に止めることなく過剰な炎症を抑える新たな手法が開ける可能性があります。
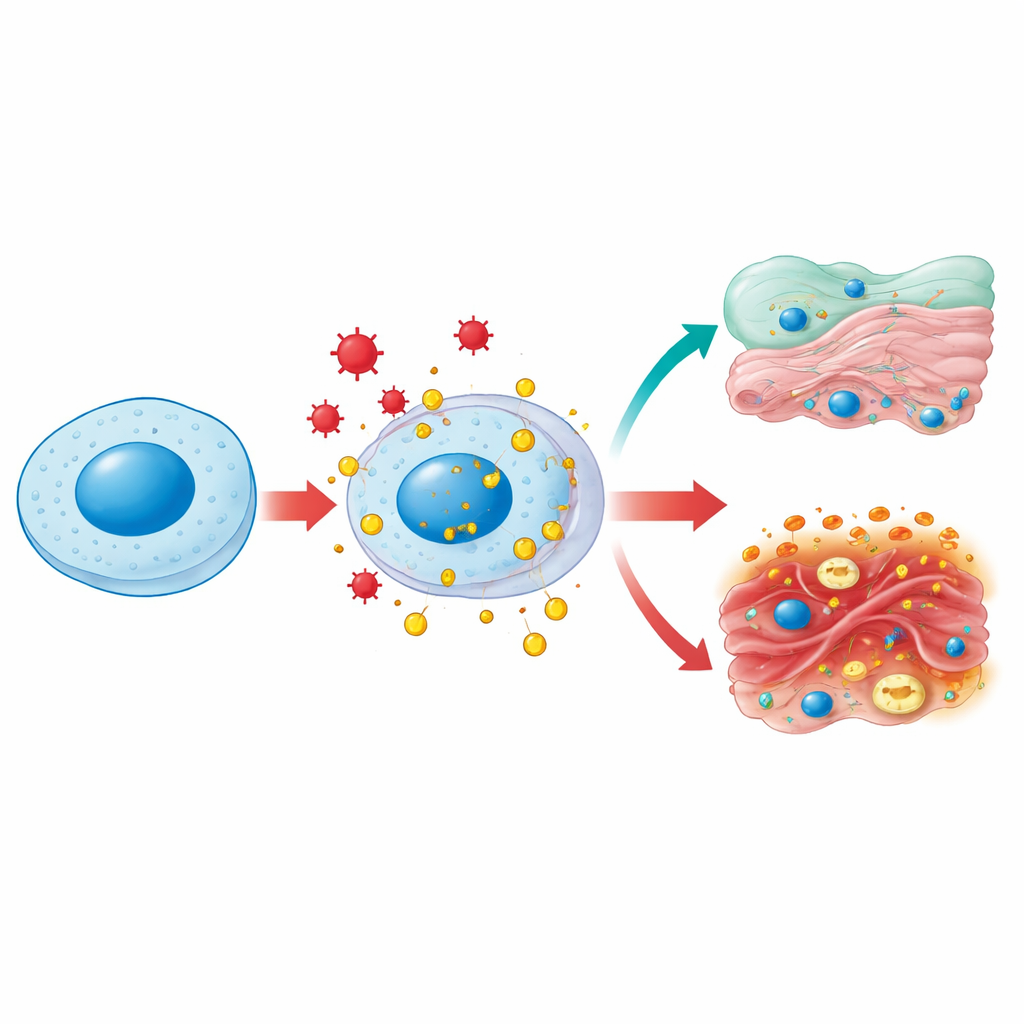
一つのタンパク質、さまざまな居場所
HMGB1は通常、細胞核に存在してDNAを曲げたり緩めたりして遺伝子の複製や修復を助けます。感染、高血糖、毒性損傷などのストレス下では化学修飾を受け、細胞質へ、さらに細胞外へと移動します。細胞質では、オートファジーというクリーニング過程を促進したり、ミトコンドリアの過度な断片化を防いだりしてミトコンドリアの健全性維持に寄与します。細胞外へ放出されるとHMGB1は古典的な“危険信号”となり、免疫細胞は組織損傷の印としてこれを認識して現場に急行します。したがって同じ分子が、いる場所と化学的にどのように調節されているかに応じて、細胞内ではハウスキーピング的な役割を、細胞外ではアラーム的な役割を果たします。
酸化が振る舞いを書き換える仕組み
本総説の中心は、酸化—活性酸素種(ROS)による反応—がHMGB1をどのように再形成するかです。このタンパク質には、スイッチの役割を果たす3つの硫黄含有部位があります。完全に還元された状態では、HMGB1は細胞生存や修復細胞の呼び寄せを支持する傾向があります。軽度の酸化はこれらのうち二つの部位を同一分子内で結びつけて“ジスルフィド”型を作り、これは特にトール様受容体やRAGEなどの細胞表面受容体に結合しやすくなります。この型は炎症性メッセンジャーの産生を強力に刺激します。より強い酸化ストレスは分子をさらに過酸化の状態へ押し進め、DNAや受容体に効果的に結合できない“焼き尽くされた”形にし、免疫学的に沈黙した状態となって炎症の解消期や免疫反応を誘発しない細胞死プログラムに関連します。
細胞死シグナルから病気の推進役へ
HMGB1は多様な細胞死の経路と深く結びついています。壊死、ネクロプトーシス、フェロトーシス、パイロトーシスといった劇的な細胞死の過程では、HMGB1は漏出するか能動的に細胞外へ輸送され、その赤化還元(レドックス)サインは周囲の酸化状態を反映します。壊死の初期には還元型である傾向があり、長期のストレスはより酸化された状態へと押し上げます。細胞外に出ると、還元型HMGB1は一部のがん細胞で保護的なオートファジーを促進し化学療法からの生存を助けることがある一方、ジスルフィド豊富な型や二量体化した形式は炎症カスケードや補体系の活性化を増幅し組織損傷を悪化させます。HMGB1はまた、細菌由来の脂質と協働してネクロプトーシスを誘導したり、脳梗塞後に支持細胞で鉄依存性の細胞死を促進したりして、特定の死の経路を逆に促進することもあります。このようにHMGB1は、組織における生死のバランスを示すだけでなく調節しています。
炎症、自己免疫、がんとの関連
その挙動が酸化に非常に敏感であるため、HMGB1の異なる変異体は疾患ごとに異なるパターンで現れます。ジスルフィド豊富なHMGB1は慢性炎症と強く関連しており、関節リウマチの炎症関節、線維化した肝臓、肺障害、手術後の虚血再灌流障害、敗血症などで見られ、血中レベルは重症度や死亡リスクと相関します。対照的に還元型HMGB1は心臓線維芽細胞やCXCL12に導かれる単球の移動など、細胞移動や組織再構築に関連することが多いです。過酸化された免疫的に静かなHMGB1は、死体を免疫攻撃を誘発せずに処理したい状況—例えばアポトーシスの後期—で豊富に見られます。腫瘍ではジスルフィド型が抑制的で増殖を許容する免疫環境を支持し、HMGB1を阻害すると腫瘍が縮小しチェックポイント免疫療法の効果が高まる場合があります。
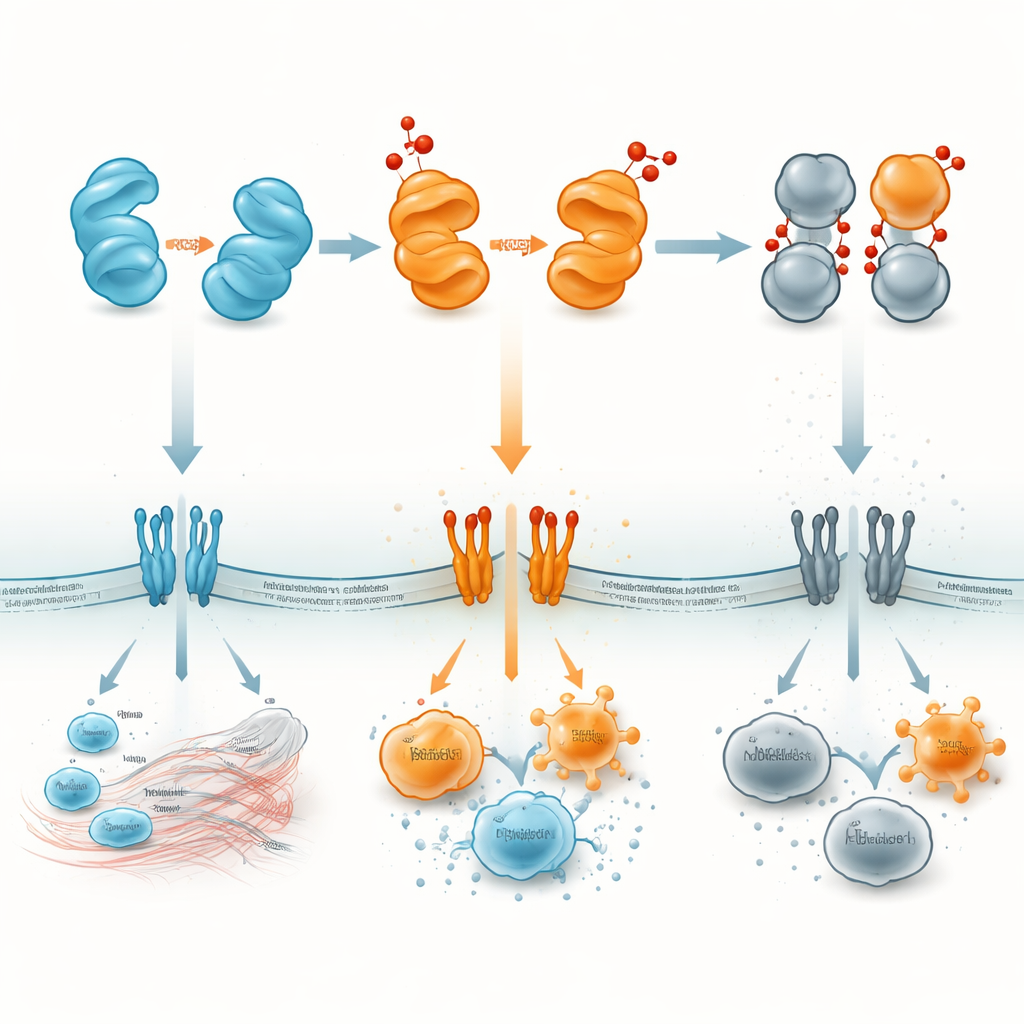
分子アラームを治療標的に変える
非専門家から見れば、HMGB1は化学状態によって音量とメッセージが変わる小さなタンパク質のアラームのように考えられます。還元型HMGB1は修復クルーを呼び込み、ジスルフィド型や二量体は有害な炎症を煽る強いアラームを鳴らし、完全に酸化された形はほぼ沈黙して炎症の終息を助けます。どのバージョンがいつどこに現れるか—核内、細胞質、血中、特定の臓器内—をマッピングすることで、研究者らは有害な形を阻害したり有益な形を安定化したりする薬剤を設計できると期待しています。このような戦略は、HMGB1そのものだけでなく、このタンパク質が免疫系に語りかける方法を制御する酸化という“ディマー(調光)スイッチ”を標的にすることで、敗血症、自己免疫、脳卒中、肺障害、がんなどを治療する道を開くかもしれません。
引用: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
キーワード: HMGB1, 炎症, 酸化ストレス, 細胞死, 自己免疫疾患