Clear Sky Science · ja
T細胞受容体を介した機械的伝達:コンセンサス、議論点と将来の展望
免疫細胞はどのように周囲を感じるか
免疫系は化学信号を検知するだけでなく、物理的な力も感知します。本総説では、ウイルスやがんを探索する白血球であるT細胞が、表面の受容体にかかる微小な押し引きを用いて攻撃するかどうかを判断する可能性を検討します。この分子スケールの「触覚」の理解は、ワクチンやがん免疫療法、自己免疫疾患に対する考え方を一変させる可能性があります。
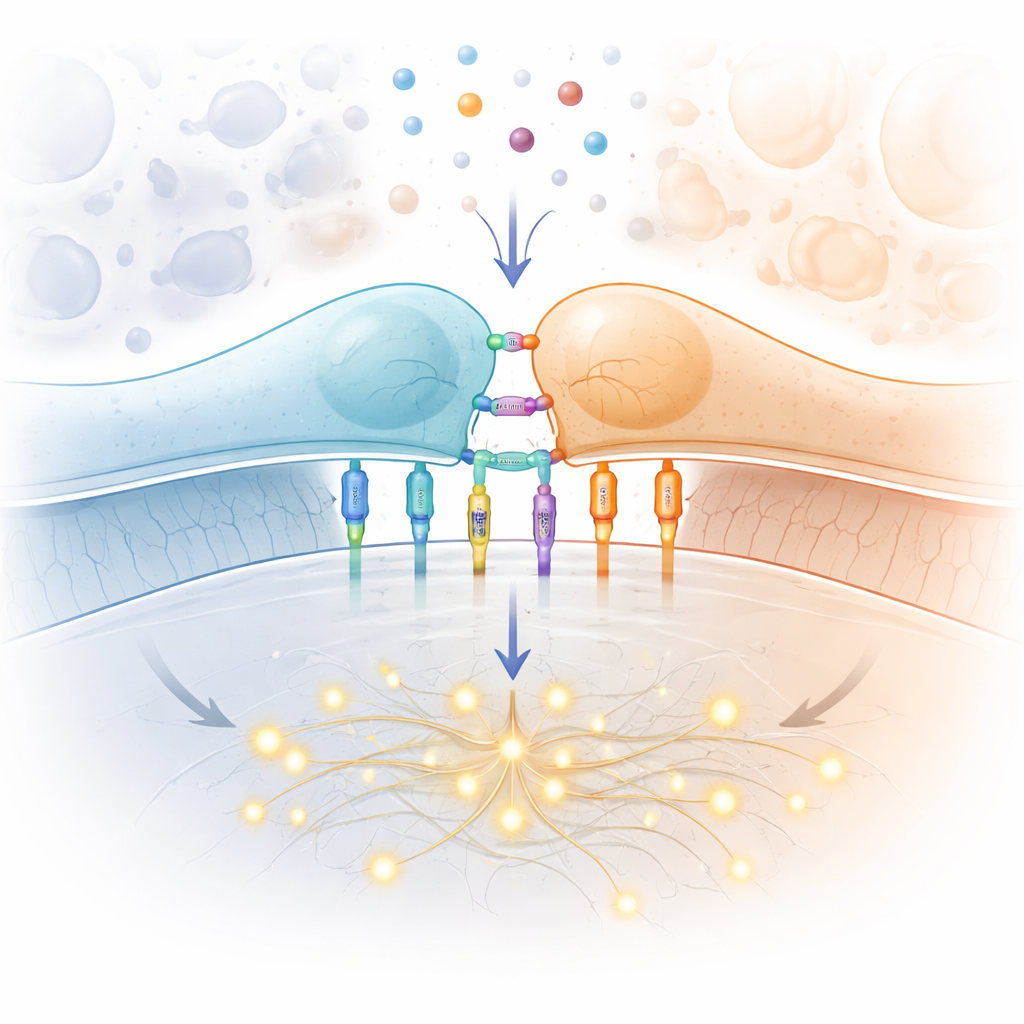
T細胞受容体の特別な役割
物語の中心にあるのはT細胞受容体で、他の細胞が提示するタンパク質断片を検査するT細胞表面の分子機械です。適切な断片が見つかると、T細胞は活性化して増殖し、感染やがん化した標的を排除します。この受容体には厳しい要求が課されます:極めて少数の外来断片に反応し、無数の無害な自己断片を無視し、パトロール中のT細胞として速やかに働き、さらに個々人の何百万もの受容体バリアントに対応すること。細胞内のシグナル伝達経路――タンパク質キナーゼ、足場タンパク、転写因子を含む古典的な配線――はよく解明されていますが、謎なのは最初の一歩です:細胞表面で断片に結合するという単純な行為が、どのようにして受容体を静止状態から活性状態へ反転させるのか。
最初の火花に関する対立する考え方
研究者はT細胞受容体が初めてオンになる仕組みについていくつかのモデルを提案してきました。一つの見方では、受容体が小さなクラスターに集まることで局所濃度が上がり、シグナル反応が効率的に進行することでシグナルが始まるとされます。別の考えは形状変化を重視します:結合により受容体複合体の部分がねじれたり緩んだりして、細胞内に埋もれていた領域が解放され、酵素が修飾できるようになるというものです。三番目のモデルは細胞間接触での混雑を強調します。ここでは短い受容体–リガンド対が狭い領域に詰まり、通常シグナルをオフにするかさばった酵素を物理的に排除し、活性化のバランスを傾けます。各モデルは実験に裏付けられ、パズルの一部を説明しますが、いずれも単独では受容体の極端な感度や非常に類似したタンパク質断片を識別する能力を完全には説明できません。
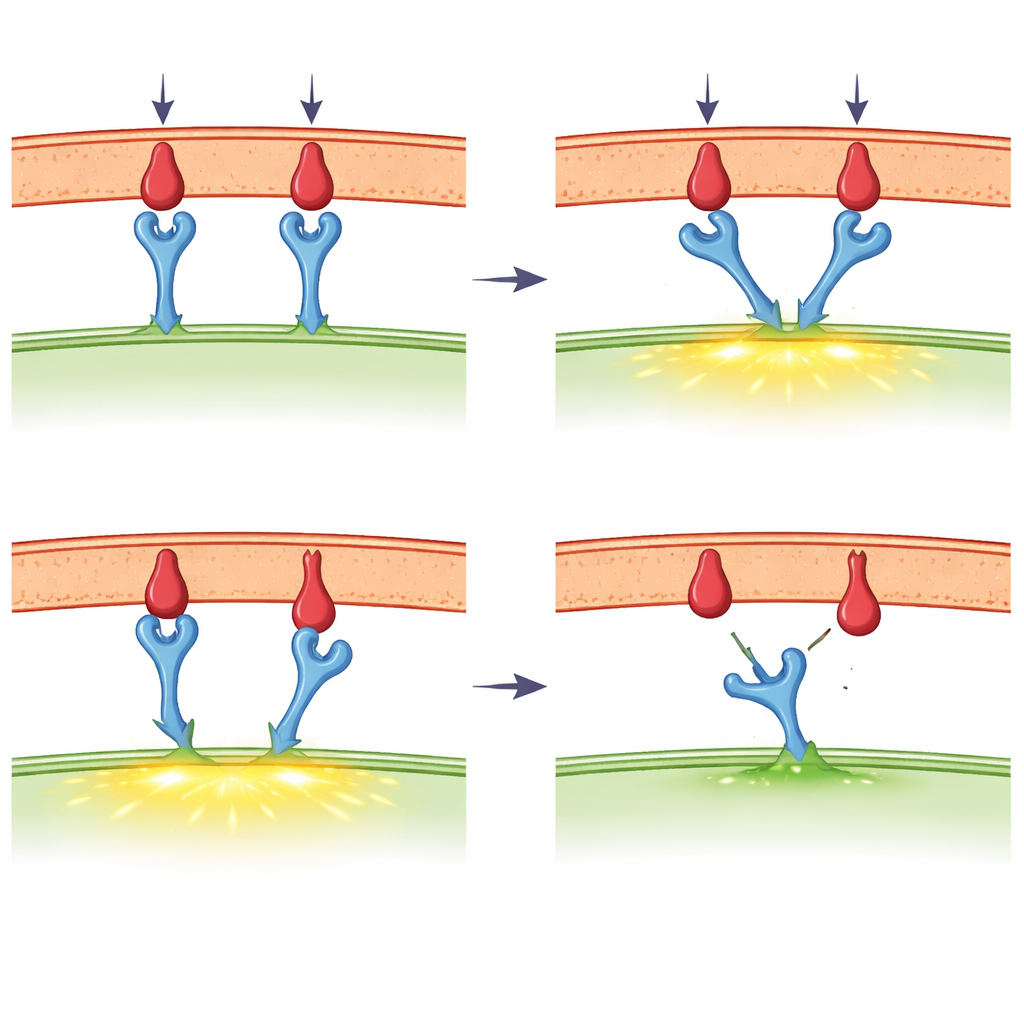
触覚と力が登場したとき
本総説の重要な焦点は、T細胞受容体が力に応答する機械センサーとして振る舞うという新興の考え方です。超感度装置を用いて、研究者は単一の受容体–リガンド結合にリンゴの重さの一兆分の一ほどの力を加えて引っ張ることができます。強力な外来断片に対しては、穏やかな引っ張りが結合寿命を逆に延ばすことがあり、これは「キャッチ」と呼ばれる挙動です。弱い断片や自己断片は代わりに「スリップ」挙動を示し、引っ張るとより早く外れます。T細胞自身はアクチンフィラメントとモータープロテインからなる内部骨格を通じてこのような力を生み出し、特に免疫シナプスと呼ばれる密接な接触領域で顕著です。新しい分子張力プローブは、キャッチ挙動が現れる範囲の力がT細胞活性化の初期に実際に存在することを示していますが、実験手法の違いにより報告される値が異なり、活発な議論を引き起こしています。
時間をかけて自己と非自己を判別する
本稿はまた、T細胞がノイズの多い短時間の接触イベントを信頼できる決定に変える方法を再検討します。長年の考え方である動的プルーフリーディング(kinetic proofreading)は、シグナルが時間を要する一連の段階を経て進行し、十分に長く受容体が関与し続けた断片だけが復帰不能点に到達できると示唆します。著者らは、機械的効果がこの時間フィルターを鋭くする方法を論じます:引っ張る力は生産的な結合の寿命を延ばし、生産性の低い結合の寿命を短くして、強い刺激と弱い刺激の差を拡大します。また、T細胞が単一の長い接触に依存するのではなく、多くの短い接触を統合する可能性や、シグナル伝達ネットワーク内のフィードバックが最近の遭遇の分子「記憶」を保存する方法についても検討します。これらの改良により、複雑な組織環境でT細胞が速さと正確さを両立する理由が説明されます。
免疫受容体に共通する原理
T細胞受容体は特に多くの要求を背負っていますが、その設計原理の多くは他の免疫受容体にも見られます。B細胞受容体や自然免疫細胞上の抗体受容体は類似のシグナルモチーフを共有し、混雑、クラスター化、細胞骨格の力が重要となる近接接触領域で働くことが多いです。力に対するキャッチ様の応答は複数のそのような受容体–リガンド対でも報告されています。これは、機械的手がかりを感知することが、標的がしっかり固定され正しく提示され応答に値するかを確かめるために免疫系が用いる一般的な戦略であることを示唆します。
健康と治療への意義
一般読者への結論は、T細胞が単に異物分子の存在を嗅ぎ分けるだけでなく、それらを引っ張ったときの触感を試しているということです。化学、物理学、細胞生物学を組み合わせることで、本総説は免疫受容体が結合と力のわずかな違いを細胞の生死を左右する決定に変換していると論じます。これらの機械生物学的規則を深く理解することは、より優れたT細胞療法、より精密なワクチン、および受容体が何に結合するかだけでなく、どのように機械的に関与するかを変えることで免疫応答を調整する新しい治療法の設計に役立つ可能性があります。
引用: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
キーワード: T細胞受容体, 機械的伝達, キャッチボンド, 免疫シナプス, 動的プルーフリーディング