Clear Sky Science · ja
大腸腺癌におけるネドデュレーションと細胞周期制御をつなぐ架け橋としてのUBE2M
なぜこの研究が大腸がんに重要なのか
大腸がんは世界的に最も一般的で致命的ながんの一つであり、その主因のひとつは腫瘍細胞が絶え間なく分裂する能力を獲得することにあります。本研究は、大腸がん細胞が細胞分裂の重要なチェックポイントを高速で通過するのを助ける、これまで見落とされていた制御スイッチを明らかにしました。このスイッチの分子レベルでの働きを解明し、既存の抗真菌薬がこれを阻害できることを示すことで、腫瘍増殖を遅らせる、あるいは止める可能性のある新たな手法を示唆しています。
腫瘍細胞内に潜む制御の階層
細胞は無作為に分裂するわけではなく、DNAの複製や細胞分裂が安全に行えるかを確認するチェックポイントを含む秩序立った周期を進みます。がん細胞はしばしばこれらのチェックポイントを書き換えます。著者らはネドデュレーションと呼ばれる翻訳後修飾、すなわちタンパク質に微妙な化学的タグを付ける過程に着目しました。以前の研究は多くのがんでネドデュレーションが活性化していることを示唆していましたが、大腸がん細胞の細胞周期とどう結びつくかは不明でした。ヒト腫瘍からの大規模な単一細胞データセットと、1,800人以上の患者からのバルク遺伝子発現データを用いることで、ネドデュレーション活性が特にG2/M期――細胞が分裂する直前の最終ゲートに位置する段階――にある悪性腸細胞で高いことが判明しました。
分子“橋”タンパク質に注目
ネドデュレーションと細胞分裂をつなぐ分子を特定するために、研究者らはネットワーク解析の手法で何千もの遺伝子をふるいにかけました。際立っていたのはUBE2Mというタンパク質で、これは小さなNEDD8タグを他のタンパク質に付ける補酵素です。データ上でUBE2Mはネドデュレーションや細胞周期経路と強く結びついていただけでなく、大腸腫瘍で周辺の正常組織よりもはるかに高発現でした。腫瘍中のUBE2Mが多い患者は生存率が低い傾向にあり、単なる“同乗者”ではなく駆動因子である可能性が示唆されました。実際にがん細胞株やマウス腫瘍モデルでUBE2Mを減らすと腫瘍増殖が遅くなり、細胞分裂が減り、アポトーシスが増加しました。逆にUBE2Mを過剰発現させると増殖と細胞周期の進行が促進されました。
成長促進タンパク質を守るリレー
さらに掘り下げると、UBE2Mがどのように細胞分裂を助けるかが明らかになりました。UBE2Mは単独で働くのではなく、USP39とPABPC1という二つのタンパク質を含むリレーを引き起こします。通常、PABPC1はユビキチン鎖により分解標的とされ、細胞のタンパク質リサイクル機構へ送られます。研究チームは、UBE2MがUSP39をNEDD8で修飾することを示しました。この修飾はUSP39のPABPC1からユビキチン鎖を切り離す能力を高め、PABPC1が分解されるのを防ぎ、その安定性を増します。PABPC1が増えると、特定のmRNAの翻訳が効率化され、その中にはG2/Mチェックポイントのアクセルとなるサイクリン、CCNB1のmRNAも含まれます。本質的に、UBE2MはPABPC1を安定化させ、これがCCNB1の産生を後押しして細胞を分裂へと駆り立てます。
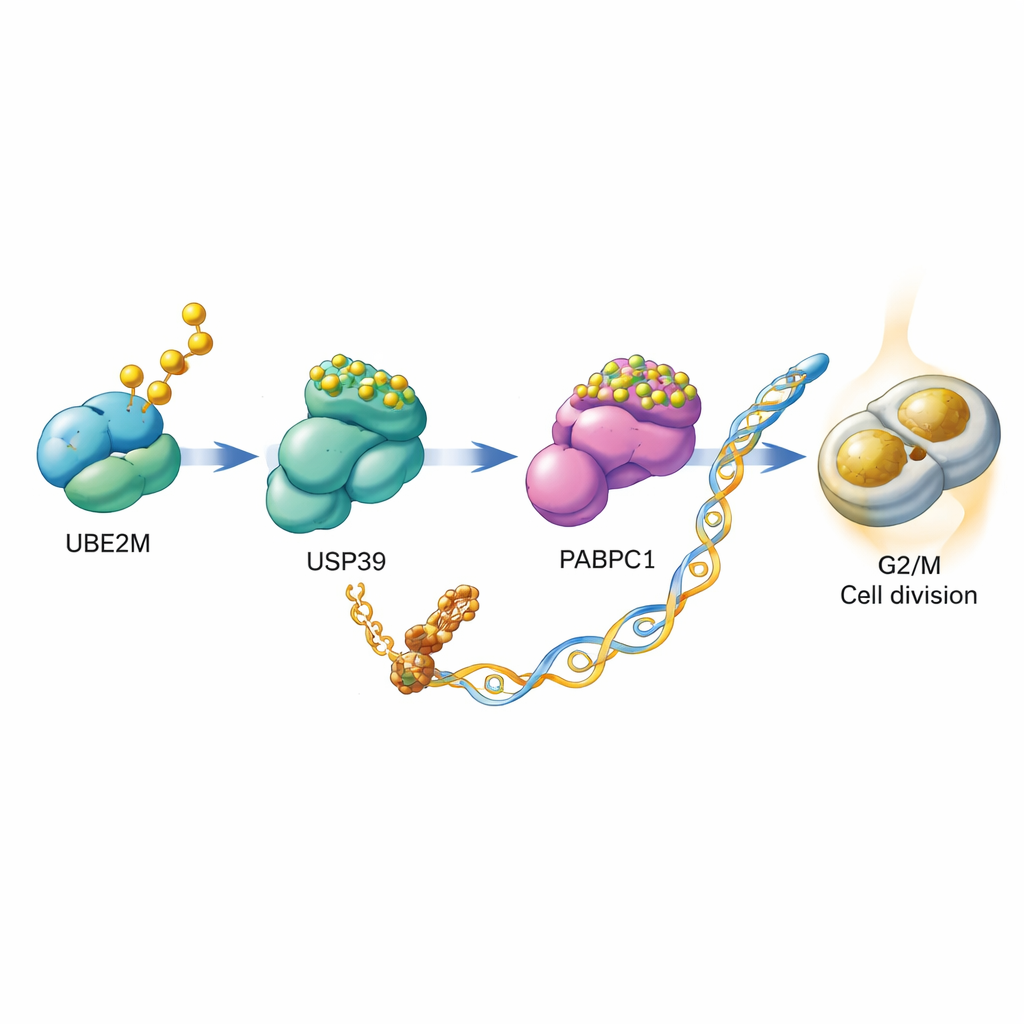
分子機構から薬剤の可能性へ
このUBE2M–USP39–PABPC1–CCNB1という連鎖の発見は、大腸がん細胞の新たな脆弱性を示唆しました。著者らは既に抗真菌治療に使われ、最近ではUBE2Mのネドデュレーション活性を阻害する因子として同定されたミカファンギンに注目しました。培養した大腸がん細胞では、ミカファンギンがUSP39のネドデュレーションを弱め、PABPC1の分解を増やし、CCNB1タンパク質レベルを低下させました。その結果、細胞分裂は遅延し、より多くの細胞がG2/Mチェックポイントで足止めされ、アポトーシスが増加しました。大腸がん細胞を移植したマウスでは、毎日のミカファンギン投与により未治療群と比べて腫瘍が有意に縮小し、UBE2M自体を除去することなく効果が得られました。
長期的に患者にとって何を意味するか
本研究は、単一の酵素UBE2Mが微妙なタンパク質修飾システムを腫瘍細胞の分裂決定につなげる仕組みを明確に描き出しています。UBE2MはUSP39を介して翻訳因子PABPC1を安定化させ、間接的に強力な細胞周期ドライバーであるCCNB1の量を増やして腫瘍増殖を促します。さらなる研究と臨床試験が必要ですが、このリレーを阻害すること、たとえばミカファンギンのような既存薬を再利用することは、大腸がんの進行を遅らせ、患者の転帰を改善する新たな標的戦略となる可能性を示しています。
引用: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
キーワード: 大腸がん, 細胞周期, ネドデュレーション, UBE2M, 標的療法