Clear Sky Science · it
Rilevazione ultrasensibile di biomarcatori dell’Alzheimer con biosensori fotonici a nanopilastri
Perché un semplice esame del sangue per la perdita di memoria è importante
Con l’emergere di nuovi farmaci in grado di rallentare la malattia di Alzheimer, i medici hanno urgente bisogno di test semplici che indichino chi è a rischio molto prima che i sintomi diventino evidenti. Oggi, confermare l’Alzheimer di solito richiede costose scansioni cerebrali o punture lombari che pochi pazienti ricevono nella pratica clinica di routine. Questo studio descrive un minuscolo sensore a base di luce in grado di individuare molecole chiave legate all’Alzheimer in una goccia di sangue a livelli clinicamente rilevanti, aprendo potenzialmente la strada a test rapidi e a basso costo da usare in ambulatori di uso comune o anche vicino al letto del paziente.
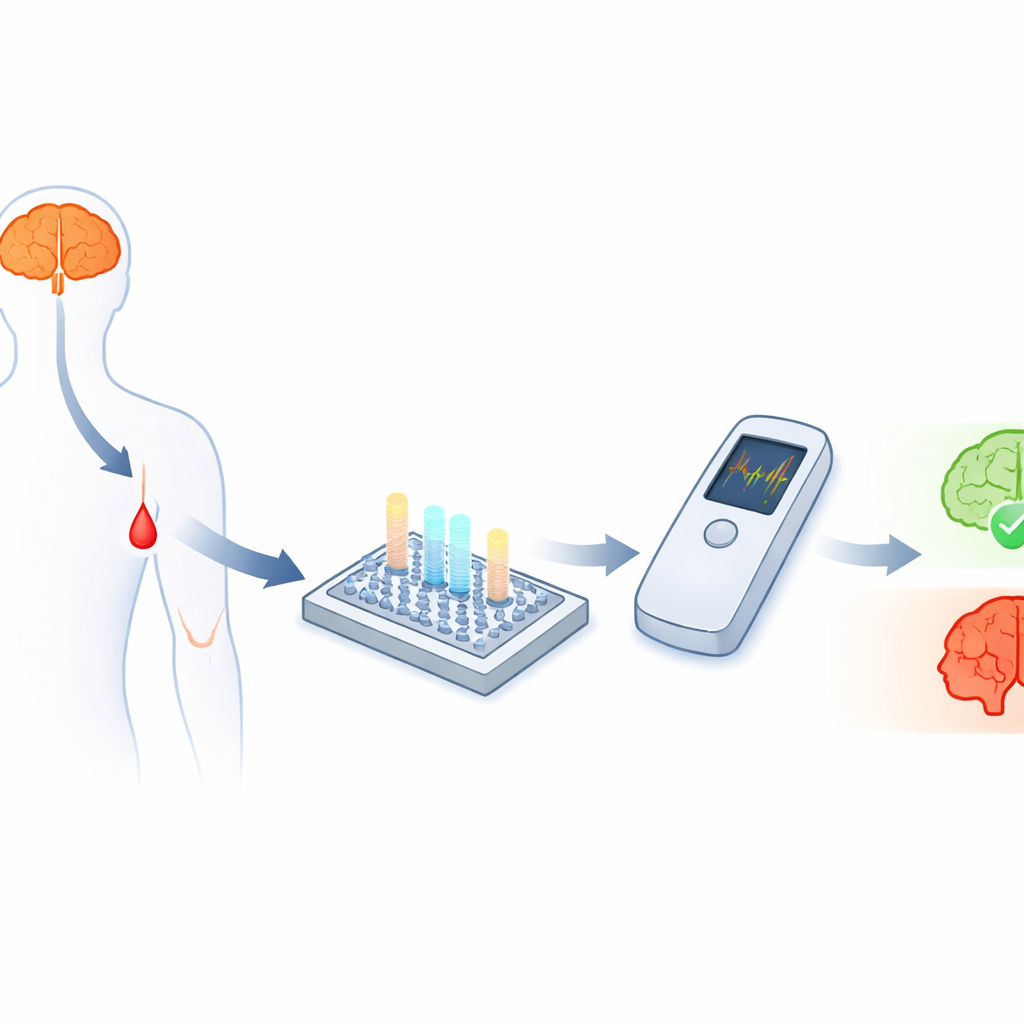
Cercare indizi nel sangue
La malattia di Alzheimer è strettamente collegata a piccoli frammenti proteici chiamati beta‑amiloide, in particolare due forme note come Aβ40 e Aβ42. Le loro quantità, e in particolare il rapporto tra di esse, forniscono indizi importanti sulla presenza della malattia e sul suo andamento. La sfida è che questi frammenti sono minuscoli e circolano nel sangue a livelli estremamente bassi — trilionesimi di grammo per millilitro — rendendoli molto difficili da quantificare con precisione al di fuori di laboratori specializzati. Sebbene i sensori elettrochimici possano in linea di principio rilevare concentrazioni così basse, trasformarli in test robusti e accessibili per il punto di cura, in grado di monitorare contemporaneamente diversi biomarcatori, si è rivelato problematico.
Guidare la luce attraverso minuscoli pilastri
Il team ha affrontato questa sfida usando la nanofotonica — strutture che controllano la luce su una scala più piccola della sua lunghezza d’onda. Hanno costruito un chip coperto da una griglia regolare di coppie di sottilissimi pilastri di silicio su vetro. Quando la luce colpisce questa superficie patternizzata, viene intrappolata in una speciale modalità di risonanza estremamente sensibile ai cambiamenti vicino alle sommità dei pilastri, in modo analogo a come il timbro di un diapason cambia se vi si aggiunge del materiale. Regolando con cura la distanza tra i pilastri di ogni coppia, i ricercatori hanno bilanciato tre proprietà cruciali contemporaneamente: quanto è definita la risonanza ottica, quanto cambia in risposta all’ambiente circostante e quanto grande è il segnale prodotto. Questo design da “punto ottimale” rende il chip particolarmente adatto a rilevare quantità minime di materiale.
Rendere visibili molecole invisibili
Anche con questo design ottimizzato, i marcatori dell’Alzheimer da soli disturberebbero a malapena la luce. Per amplificare l’effetto, i ricercatori hanno usato una strategia a sandwich con nanoparticelle d’oro. Per prima cosa hanno rivestito la superficie del sensore con strati di chimica adesiva che orientano correttamente anticorpi specializzati in modo che i loro siti di legame puntino verso il liquido. Questi anticorpi catturano Aβ40 o Aβ42 dal campione. Successivamente, nanoparticelle d’oro, ognuna decorata con un secondo anticorpo che riconosce l’altro estremo dello stesso frammento amiloide, vengono fatte scorrere sul chip. Ogni volta che è presente un frammento amiloide, esso crea un ponte tra la superficie e una particella d’oro, “segnalandone” efficacemente la presenza. Poiché l’oro altera fortemente l’ambiente ottico locale, ogni frammento catturato produce uno spostamento della risonanza del sensore molto più grande rispetto al peptide da solo, aumentando la sensibilità di circa uno o due ordini di grandezza pur mantenendo un segnale ottico pulito.
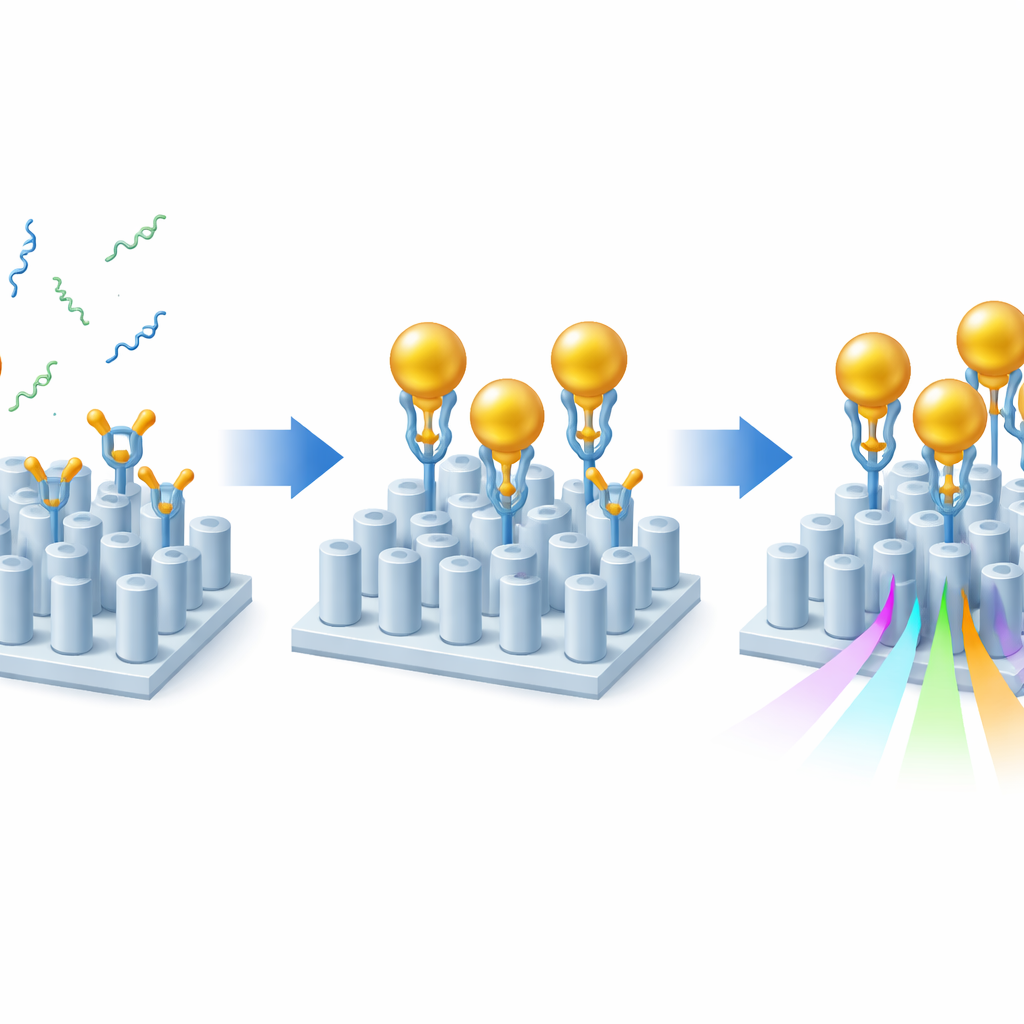
Testare campioni realistici
Per dimostrare che l’approccio funziona oltre ai semplici tamponi di laboratorio, il team ha testato il sensore con siero umano. Hanno diluito il siero per renderlo compatibile con la gestione microfluidica, mantenendo però livelli di amiloide rappresentativi di quelli riscontrati nei pazienti. È importante che siano riusciti a rilevare sia Aβ40 sia Aβ42 a 0,2 picogrammi per millilitro in questo siero diluito — equivalente al livello clinicamente rilevante di 20 picogrammi per millilitro nel sangue intero. Segnando diversi anticorpi di cattura in regioni separate sullo stesso chip, hanno misurato simultaneamente entrambe le forme di amiloide all’interno di un unico canale minuscolo, un passo chiave verso la valutazione del loro rapporto a partire da un singolo piccolo campione. I segnali distinguevano chiaramente i campioni arricchiti con amiloide da quelli contenenti solo i livelli di fondo naturalmente presenti anche in persone sane.
Cosa potrebbe significare per l’assistenza futura
Nel complesso, questi progressi mostrano che un sensore compatto a base di luce, potenziato da nanoparticelle d’oro, può raggiungere le sensibilità necessarie per test ematici significativi per l’Alzheimer, gestendo al contempo più di un biomarcatore. Sebbene siano necessari ulteriori lavori per trasformarlo in un dispositivo commerciale robusto e per aggiungere altri marcatori come le forme della proteina tau, la tecnologia di base è costruita con materiali scalabili e può essere abbinata a ottiche semplici e portatili. Se sviluppata completamente, potrebbe permettere ai clinici di monitorare la salute cerebrale usando solo un piccolo campione di sangue, rendendo molto più agevole rilevare precocemente l’Alzheimer e monitorare nel tempo l’efficacia dei trattamenti.
Citazione: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Parole chiave: Test del sangue per l’Alzheimer, biosensore nanofotonico, beta amiloide, nanoparticelle d’oro, diagnosi precoce