Clear Sky Science · it
L’origine della struttura quaternaria della fibrillazione dell’emoglobina falciforme: uno studio di dinamica molecolare
Perché questa storia del sangue è importante
L’anemia falciforme nasce da una minuscola modifica in una proteina del sangue, eppure può rimodellare i globuli rossi, ostruire i vasi e causare dolore cronico. Questo studio esamina in dettaglio, con strumenti della fisica, come quel singolo cambiamento fa sì che l’emoglobina si impili in fibre rigide all’interno della cellula. Utilizzando avanzate simulazioni al computer, gli autori collegano dettagli atomici a problemi a livello cellulare, offrendo nuovi indizi su come futuri farmaci potrebbero impedire all’emoglobina di bloccare la circolazione.
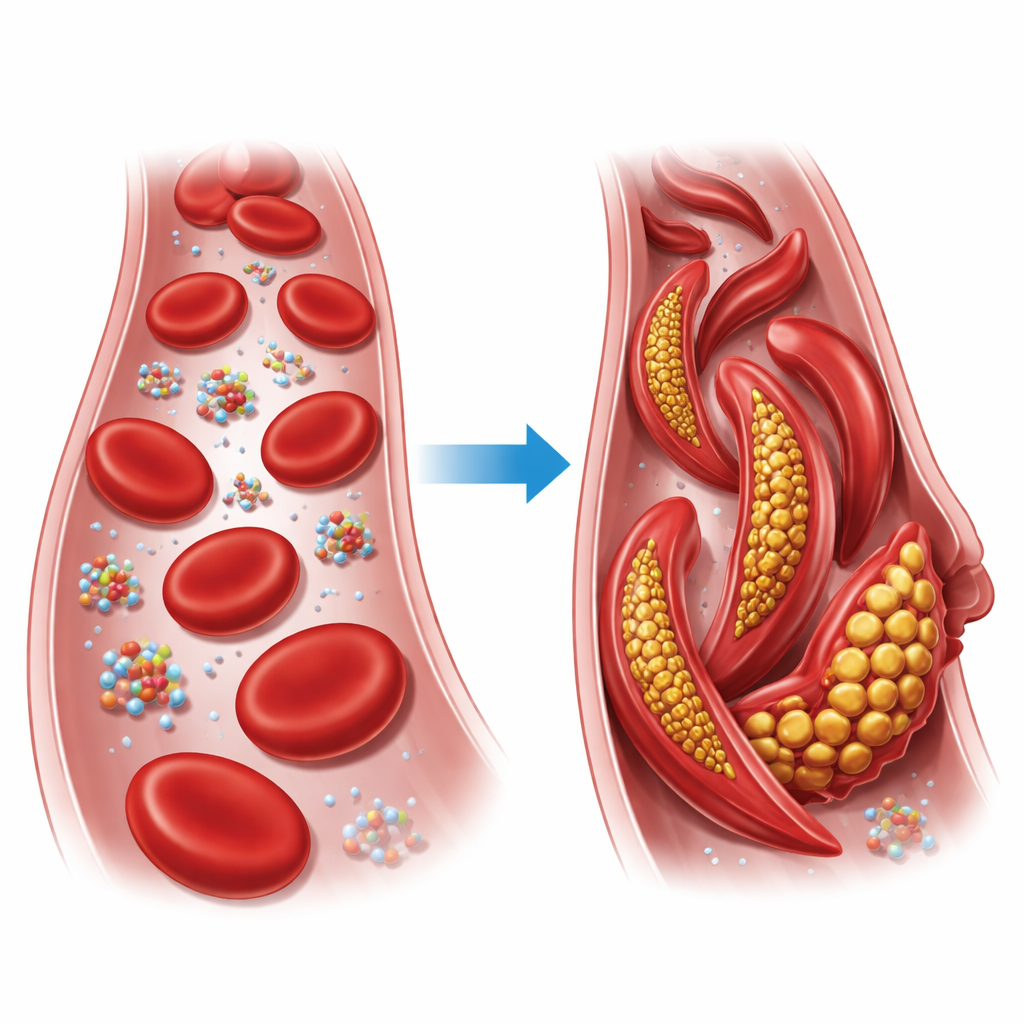
Una piccola sostituzione con grandi conseguenze
L’emoglobina è la proteina che trasporta l’ossigeno e riempie i nostri globuli rossi. Ogni unità di emoglobina è composta da quattro catene che possono disporsi in due principali forme globali, note come stato rilassato (R) e stato contratto (T). Nell’anemia falciforme, un solo mattoncino in una di queste catene viene scambiato: un glutammato carico è sostituito da una valina apolare nella posizione sei della catena beta. In condizioni di basso ossigeno, questa versione alterata, chiamata emoglobina falciforme, si associa in lunghe fibre che deformano i globuli rossi normalmente rotondi in forme rigide a falce, che possono ostruire piccoli vasi e privare i tessuti di ossigeno.
Seguire il mutare della forma dell’emoglobina
Gli autori si concentrano su come le unità intere di emoglobina ruotano e si impilano insieme in una fibra. Tracciano questo cambiamento di forma su larga scala con un singolo angolo che misura come due metà della proteina si torcono l’una rispetto all’altra. Usando simulazioni di dinamica molecolare — esperimenti virtuali che calcolano come gli atomi si muovono nel tempo in acqua e sale — spostano delicatamente questo angolo su un ampio intervallo e calcolano quanto costa energeticamente ogni conformazione. Scoprono che sia l’emoglobina normale sia quella falciforme possono esplorare molte di queste forme a temperatura corporea. L’emoglobina falciforme mostra un angolo leggermente favorito, ma queste preferenze conformazionali da sole non bastano a spiegare perché solo la forma falciforme formi fibre stabili.
Perché le fibre falciformi si attaccano e quelle normali si disfano
Per arrivare al nocciolo della formazione delle fibre, lo studio misura quanto fortemente le unità di emoglobina vicine si attraggono lungo e attraverso la fibra. Il gruppo calcola l’energia cohesiva — la forza netta che tiene insieme le unità — per molte diverse forme complessive. Per l’emoglobina falciforme, questa energia cohesiva rimane negativa (cioè attrattiva) su tutto l’intervallo di forme testate, quindi le fibre restano stabili e non si disfano facilmente. Per l’emoglobina normale, invece, alcune conformazioni mostrano energia cohesiva positiva, rendendo le fibre a quegli angoli instabili e soggette a rottura spontanea. Una differenza chiave è il modo in cui i gruppi laterali della valina mutata si infilano nelle proteine vicine: nell’emoglobina falciforme queste zone apolari formano contatti robusti sia lateralmente sia lungo l’asse della fibra, promuovendo direttamente la crescita delle fibre.
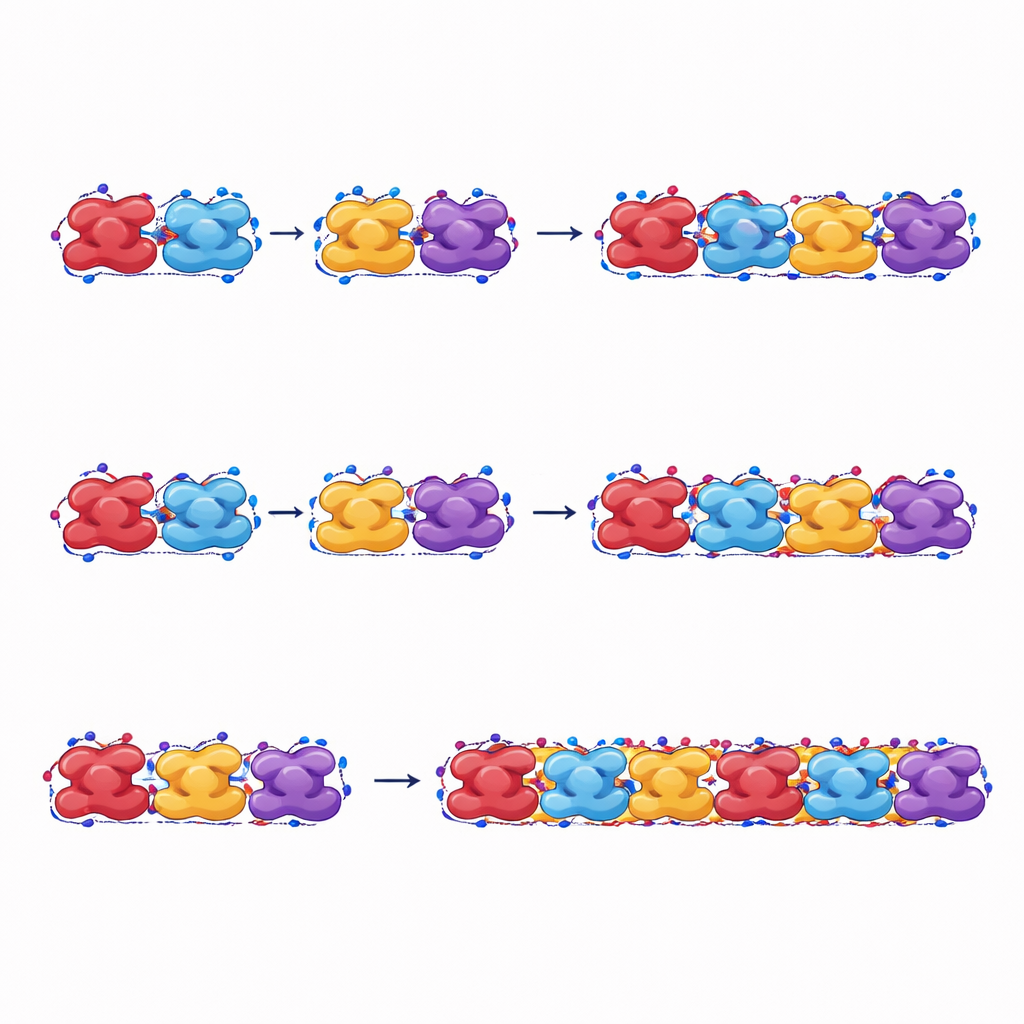
Come queste fibre sopportano carico e si rompono
Gli autori allungano anche le loro fibre simulate per imitare lo stress meccanico. Quando vengono tirate lungo la loro lunghezza, le fibre di emoglobina falciforme sopportano forze e deformazioni maggiori e dissipano più energia prima di rompersi rispetto a quelle formate da emoglobina normale. Anche la forma rilassata delle fibre falciformi, che non è quella in cui le fibre compaiono per prima, può comunque mantenere la catena attraverso cambiamenti di forma plastici, contribuendo a mantenere integra la fibra una volta formata. Le fibre di emoglobina normale, al contrario, si separano più facilmente tra unità adiacenti e assorbono meno energia prima della rottura, confermando che sono meno stabili sotto stress.
Indizi per futuri trattamenti e nuovi materiali
Nel complesso, le simulazioni mostrano che una singola sostituzione di un amminoacido rimodella il modo in cui le unità di emoglobina si incontrano, torcendo l’assemblaggio complessivo in angoli che favoriscono una forte attrazione, specialmente nello stato contratto. Questa combinazione di geometria e aderenza permette all’emoglobina falciforme di formare fibre lunghe e rigide che resistono sia al movimento termico sia alla trazione meccanica, deformando infine i globuli rossi e bloccando il flusso sanguigno. Indicando caratteristiche specifiche dell’organizzazione proteica complessiva che controllano la stabilità delle fibre, il lavoro suggerisce che farmaci antisickling efficaci potrebbero agire spingendo l’emoglobina verso conformazioni in cui le fibre diventano energeticamente sfavorite e meccanicamente fragili — trasformando un ingorgo molecolare letale in un flusso sanguigno libero.»
Citazione: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Parole chiave: anemia falciforme, fibre di emoglobina, aggregazione proteica, dynamica molecolare, disturbi del sangue