Clear Sky Science · it
La dinamina ottimizza le interazioni proteina-membrana per la fissione
Come le cellule staccano ordinatamente le proprie membrane
Ogni secondo, le tue cellule sono impegnate a staccare minuscole bolle di membrana per trasportare carico, rimodellare compartimenti interni e combattere i virus. Questo gesto apparentemente semplice di tagliare un sottile tubo di membrana in due pezzi si rivela sorprendentemente difficile dal punto di vista fisico. Questo articolo pone una domanda ingannevolmente elementare: come fa una proteina chiamata dinamina a rendere la fissione della membrana sia possibile sia affidabile, e quali caratteristiche della proteina sono davvero essenziali per il compito?
I pizzicatori cellulari al lavoro
La dinamina è una macchina molecolare che forma un collare attorno a sottili tubi di membrana e si stringe come un cappio per favorirne la rottura. Eventi di fissione di questo tipo sono alla base di processi come l’endocitosi, in cui le cellule internalizzano materiale, così come della divisione di strutture interne quali i mitocondri. Se lasciato a sé, un tubo di membrana resiste fortemente alla rottura, perché deve prima essere compresso fino a uno spessore quasi pari alla membrana stessa e attraversare uno stato intermedio instabile. Questa barriera energetica è molto più alta dell’energia di agitazione casuale disponibile all’interno di una cellula, perciò proteine specializzate per la fissione come la dinamina sono essenziali.
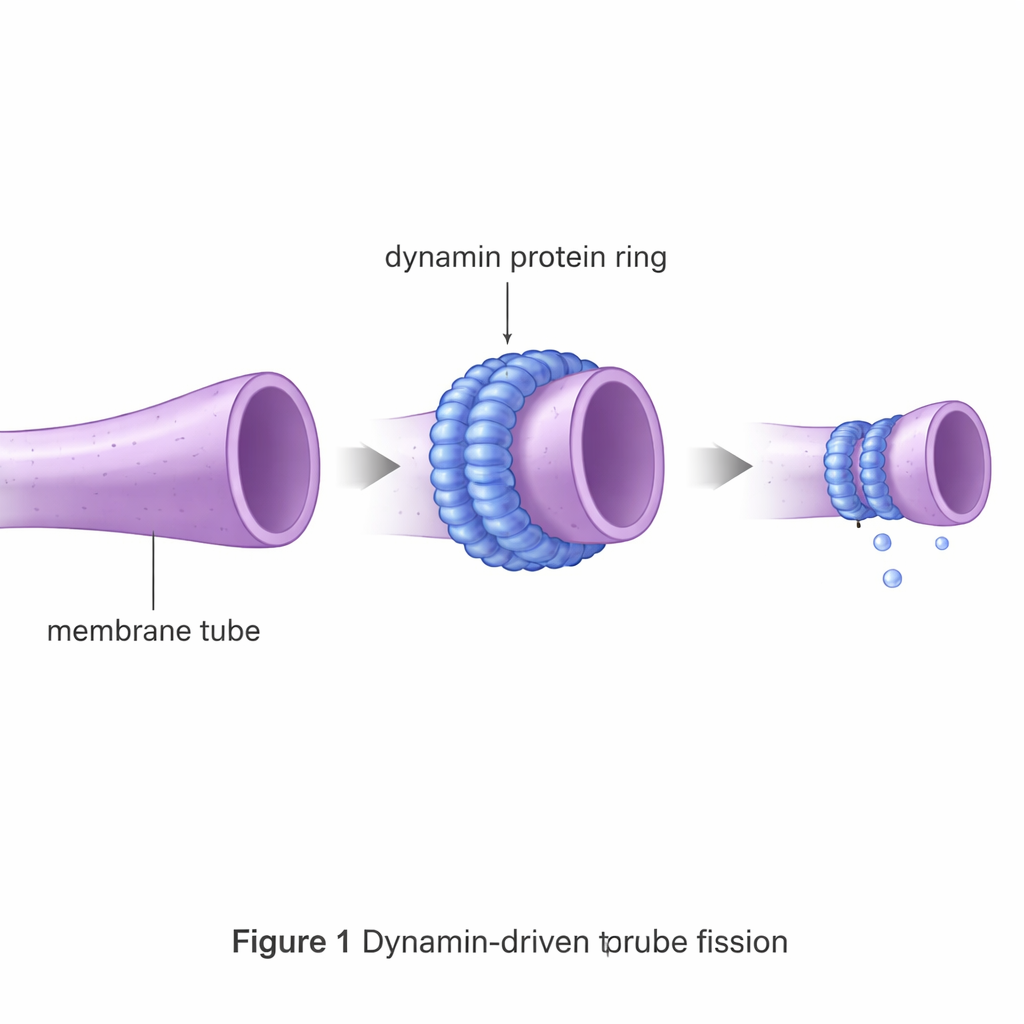
Usare membrane virtuali per testare progetti proteici
Osservare direttamente l’istante critico in cui un tubo si spezza è estremamente difficile negli esperimenti: l’imaging rapido manca di dettagli molecolari e i metodi ad alta risoluzione bloccano il sistema nel tempo. Per colmare questo divario, gli autori utilizzano un potente strumento teorico chiamato teoria del campo auto-coerente. Invece di tracciare ogni atomo, descrivono i lipidi e il solvente come catene flessibili che percepiscono campi variabili in modo regolare. Le proteine sono introdotte non come strutture atomiche complete ma come potenziali esterni a forma di toro che o escludono semplicemente lo spazio, si attaccano alla superficie della membrana o si inseriscono nel foglietto esterno. Con questo quadro possono calcolare sia le forme risultanti della membrana sia il costo di energia libera completo per passare da un tubo intatto allo stato intermedio di fissione.
Quali tipi di presa aiutano un tubo a rompersi?
Il gruppo varia in modo sistematico come una proteina simile alla dinamina interagisce con la membrana. Alcune proteine modello solo sovraffollano la superficie, agendo come un manicotto rigido; altre aderiscono in modo lieve o forte ai gruppi testa esterni; altre ancora imitano il dominio PH della dinamina reale inserendo parti idrofobiche nel foglietto esterno e “apponendo” i gruppi testa ai lati. Per ciascun caso esaminano tre grandezze correlate: quanto forte aderisce la proteina a un tubo non costretto, quanta curvatura e costrizione induce quando è legata, e quanto rimane alta la barriera energetica perché il tubo passi in uno stato di emifissione in cui gli strati interni si sono fusi. Riscontrano che una semplice compressione abbassa la barriera ma non abbastanza da spiegare una fissione efficiente, e che una forte adesione superficiale può in realtà ostacolare la rottura perché la membrana deve prima staccarsi dalla proteina per completare il collasso.
Perché un’inserzione superficiale è meglio della sola compressione
Il progetto più efficace è quello in cui la proteina si inserisce parzialmente tra i gruppi testa dei lipidi e tira le loro code verso l’alto, creando una piega locale a forma di chevron nella membrana. Questo “splay” sposta il punto più stretto del tubo leggermente al lato dell’anello proteico invece che direttamente sotto di esso. Di conseguenza, la membrana può completare il collasso critico nello stato di emifissione senza staccarsi dalla proteina, e la barriera energetica complessiva diminuisce di oltre un ordine di grandezza rispetto a un tubo nudo. Quando gli autori lasciano che i parametri della proteina si aggiustino automaticamente per minimizzare questa barriera, la soluzione ottimale corrisponde strettamente alla dimensione e all’azione del dominio PH della dinamina: una patch idrofobica di larghezza moderata che si inserisce superficialmente, non una superficie ampia e eccessivamente adesiva che spoglierebbe i lipidi dalla soluzione.
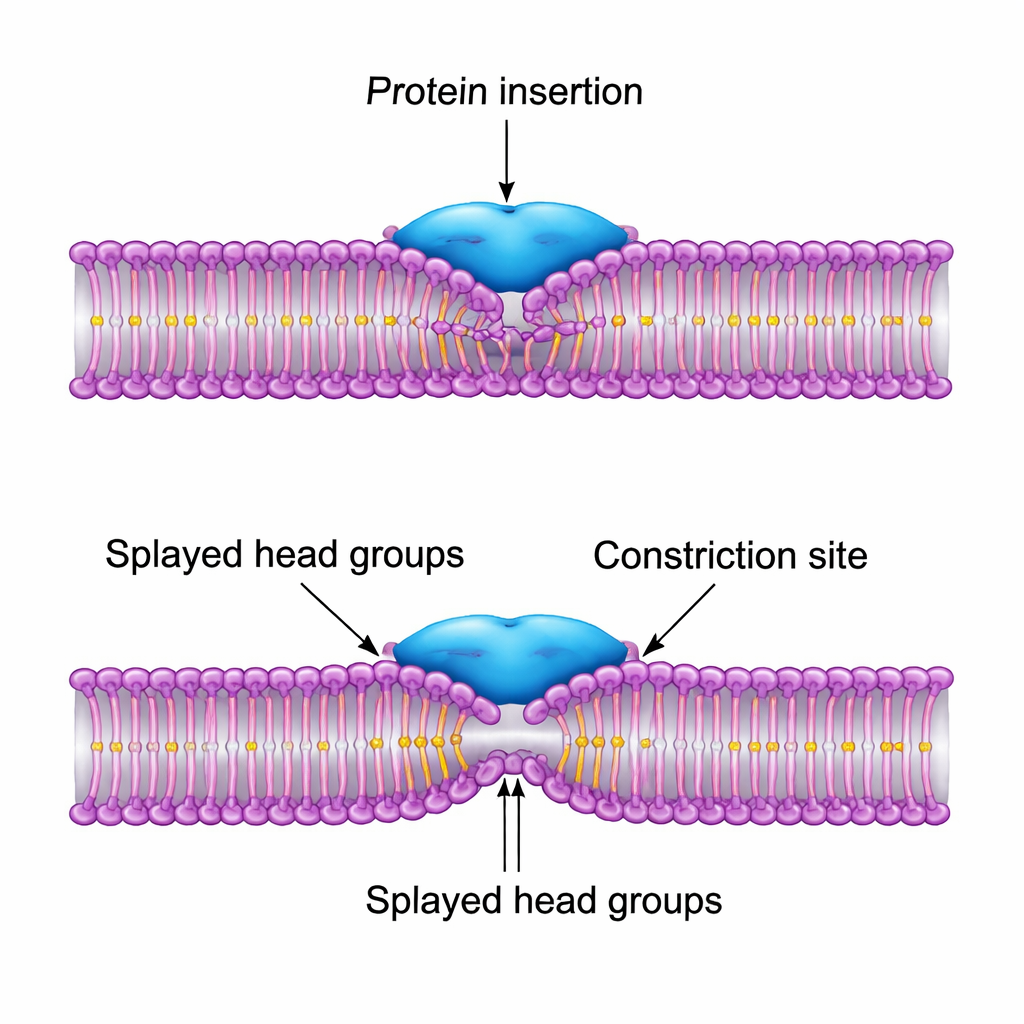
Regole di progettazione per la natura e per la nanotecnologia
Per un non specialista, il messaggio chiave è che la dinamina funziona non solo stringendo una cintura attorno alla membrana, ma regolando con cura come e dove afferra il foglietto esterno. Un cuneo superficiale che apre i lipidi esterni e concentra la curvatura appena accanto alla proteina si dimostra molto più efficace della costrizione bruta o dell’adesione forte. Questi risultati aiutano a spiegare perché l’evoluzione ha favorito l’architettura particolare della dinamina e suggeriscono principi di progettazione per proteine sintetiche o farmaci che devono tagliare o rimodellare le membrane in modo controllato in medicina e nanotecnologia.
Citazione: Spencer, R.K.W., Müller, M. Dynamin optimizes protein-membrane interactions for fission. npj Soft Matter 2, 6 (2026). https://doi.org/10.1038/s44431-026-00018-9
Parole chiave: fissione della membrana, dinamina, interazioni proteina–membrana, curvatura della membrana, teoria del campo auto-coerente