Clear Sky Science · it
La mutazione APP E590D aumenta la generazione di peptidi Aβ e Aη e aggrava la taupatia
Perché questa rara mutazione è importante
La malattia di Alzheimer è solitamente concepita come l’accumulo lento di due proteine dannose, amiloide e tau, nel cervello. La maggior parte delle persone sviluppa l’Alzheimer senza una causa unica evidente, ma alcune famiglie portano cambiamenti genetici rari che possono alterare drasticamente l’equilibrio. Questo articolo esamina uno di questi cambiamenti poco comuni nel gene della proteina precursore dell’amiloide (APP) e mostra come possa potenziare la produzione di frammenti proteici tossici e peggiorare il processo di intreccio della tau noto come taupatia. Comprendere questo caso raro fornisce indizi che potrebbero essere applicabili in modo molto più ampio a come l’Alzheimer ha origine e poi accelera.
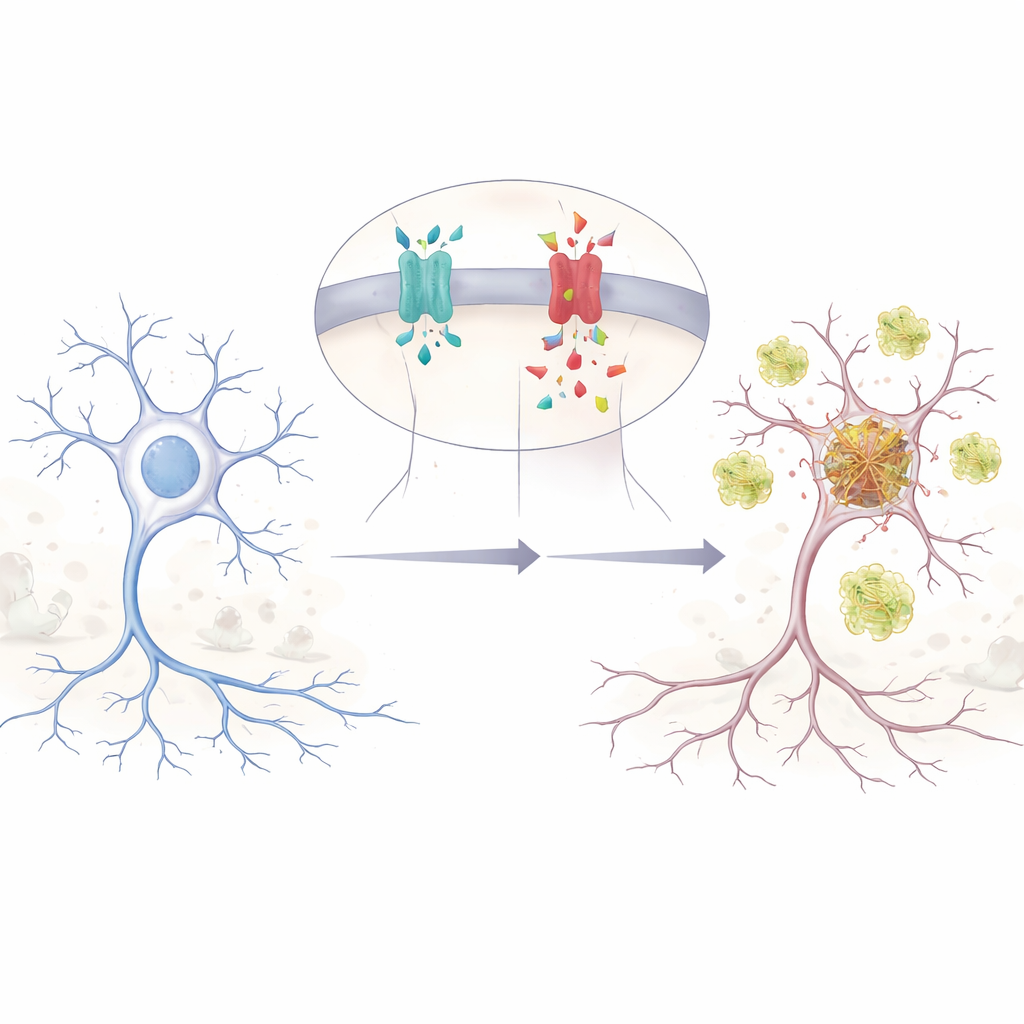
Un piccolo cambiamento genetico con grandi effetti
Gli autori si concentrano su una variazione di una singola lettera nel gene APP, denominata E590D nella principale forma cerebrale di APP. Questa mutazione è stata riportata solo in due persone, entrambe con Alzheimer confermato a età relativamente giovani e con problemi di memoria e comportamentali insoliti e molto precoci. Poiché è così rara, gli scienziati non erano sicuri se realmente causasse la malattia o fosse solo una coincidenza innocua. Per scoprirlo, il gruppo ha ricreato la mutazione in cellule umane e nei neuroni di topo, quindi ha seguito come APP venga tagliata nei suoi molti frammenti. Hanno scoperto che l’APP mutante produce molto più amiloide beta (Aβ), il peptide appiccicoso da lungo tempo associato all’Alzheimer, rispetto all’APP normale quando i livelli sono confrontati in modo corretto.
Due peptidi tossici invece di uno
APP può essere tagliata in diversi punti, come un tronco che viene affettato in posizioni differenti. Il percorso classico dell’Alzheimer genera Aβ, ma un altro taglio produce un frammento meno noto chiamato Aη. Lavori precedenti avevano mostrato che Aη può danneggiare le connessioni tra neuroni e indebolire la capacità del cervello di consolidare i ricordi. Nei loro esperimenti, i ricercatori hanno rilevato che la mutazione E590D non aumenta solo Aβ; aumenta anche in modo marcato Aη e un frammento a monte che alimenta entrambi i percorsi. Ciò significa che la mutazione sposta l’elaborazione di APP verso un doppio attacco di peptidi dannosi, potenzialmente alterando i circuiti cerebrali già prima che le placche amiloidi classiche siano rilevabili.
Come la mutazione accelera il traffico cellulare
Per capire perché si formano più frammenti tossici, il team ha studiato dove APP si trova e come si muove sulla superficie cellulare. Molti dei tagli che creano Aβ avvengono solo dopo che APP è stata internalizzata nella cellula tramite un processo chiamato endocitosi. Utilizzando tecniche di imaging e trucchi biochimici che etichettano le proteine in superficie per poi seguirne l’internalizzazione, gli scienziati hanno mostrato che l’APP mutante è meno abbondante all’esterno delle cellule ed è assorbita più rapidamente nei compartimenti interni rispetto all’APP normale. Una volta negli endosomi precoci, APP incontra gli enzimi che generano Aβ, e il traffico alterato sembra dare a quegli enzimi maggiori opportunità di agire. Allo stesso tempo, anche il taglio nel sito η sulla superficie è aumentato, spiegando l’incremento di Aη.
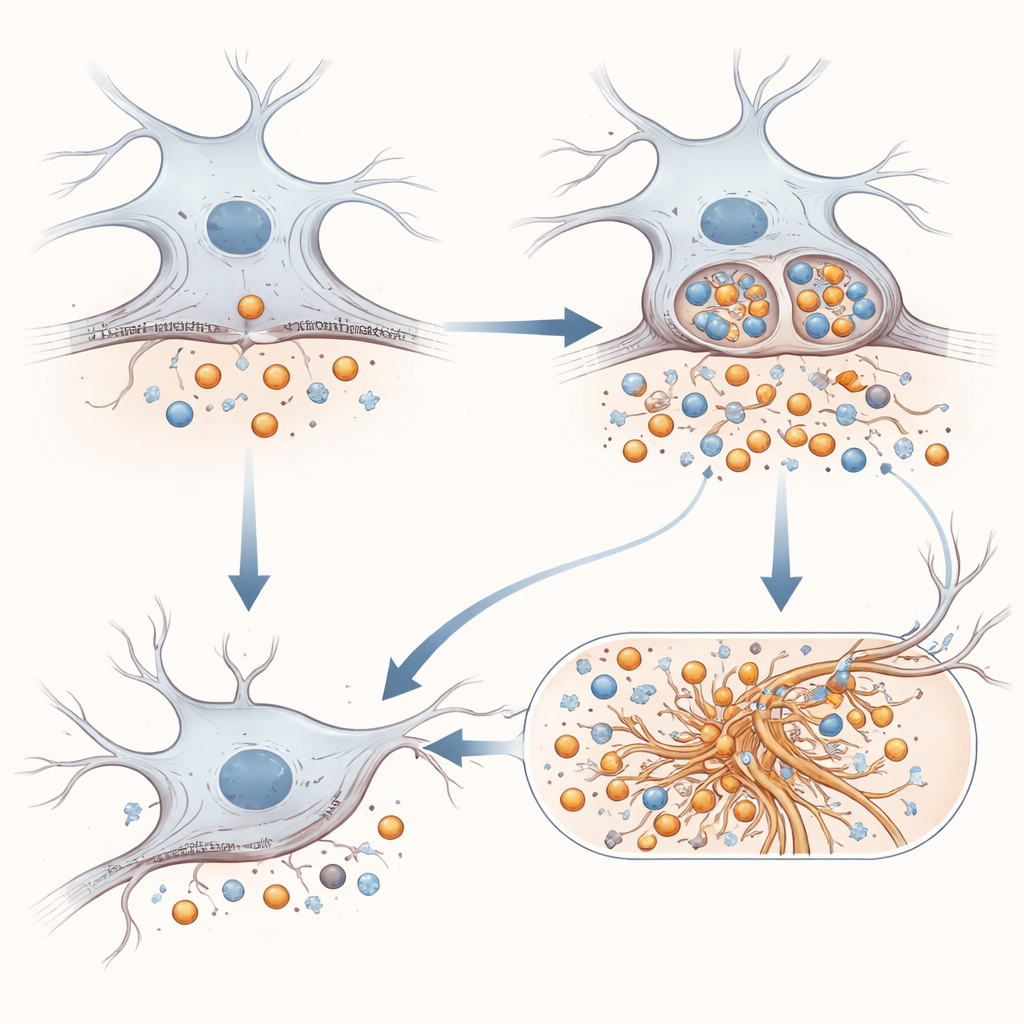
Dai frammenti proteici alla tau intrecciata e all’infiammazione cerebrale
La storia non si ferma ai frammenti legati all’amiloide. I ricercatori hanno testato se l’APP mutante influenzasse la tau, la proteina strutturale che forma fibre attorcigliate in molte demenze. In modelli cellulari che si illuminano quando i semi di tau inducono la formazione di nuovi aggregati, la presenza di APP E590D ha portato a un’aggregazione più intensa rispetto all’APP normale o all’assenza di APP. In un modello murino già incline a problemi di tau, iniettare nel’ippocampo un virus che esprimeva l’APP mutante ha aggravato gli intrecci di tau e ha scatenato una più forte attivazione di astrociti e microglia, le cellule di supporto e immunitarie del cervello. È interessante che i tipici frammenti amiloidi solubili fossero difficili da rilevare in questi cervelli di topo, ma un frammento derivato da APP distinto è apparso solo quando la mutazione era presente, suggerendo un’elaborazione alterata nel tessuto vivo.
Cosa significa questo per la comprensione dell’Alzheimer
Complessivamente, i risultati mostrano che questa rara mutazione di APP non è benigna. Spinge APP a generare più di un peptide tossico, accelera i passaggi di internalizzazione che favoriscono i tagli dannosi e amplifica l’intreccio della tau e l’infiammazione cerebrale. Per il pubblico non specialistico, il messaggio chiave è che la biologia dell’Alzheimer non è guidata da un singolo colpevole, ma da una rete di frammenti proteici e risposte cellulari interagenti. Studiare varianti genetiche potenti ma insolite fornisce una visione ingrandita di quella rete. In questo caso, suggerisce che le terapie potrebbero dover considerare sia l’amiloide sia peptidi alternativi derivati da APP come Aη, oltre al loro impatto combinato sulla tau, invece di mirare a un'unica via in isolamento.
Citazione: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Parole chiave: Malattia di Alzheimer, proteina precursore dell’amiloide, fibrille di tau, neuroinfiammazione, mutazione genetica