Clear Sky Science · it
Una piattaforma quantitativa ad alto rendimento che usa organoidi cerebrali umani dissociati 2D per modellare la neuroinfiammazione nella malattia di Alzheimer
Perché le infezioni possono avere importanza nella perdita di memoria
La malattia di Alzheimer viene solitamente descritta come un lento accumulo di proteine appiccicose nel cervello, ma prove crescenti suggeriscono che le infezioni potrebbero contribuire ad avviare questo processo. Questo studio esplora l’ipotesi usando piccoli modelli cerebrali coltivati in laboratorio per porsi una domanda semplice: un virus comune che causa le afte labiali può scatenare cambiamenti simili all’Alzheimer nelle cellule cerebrali umane, e un farmaco antivirale può attenuarli?
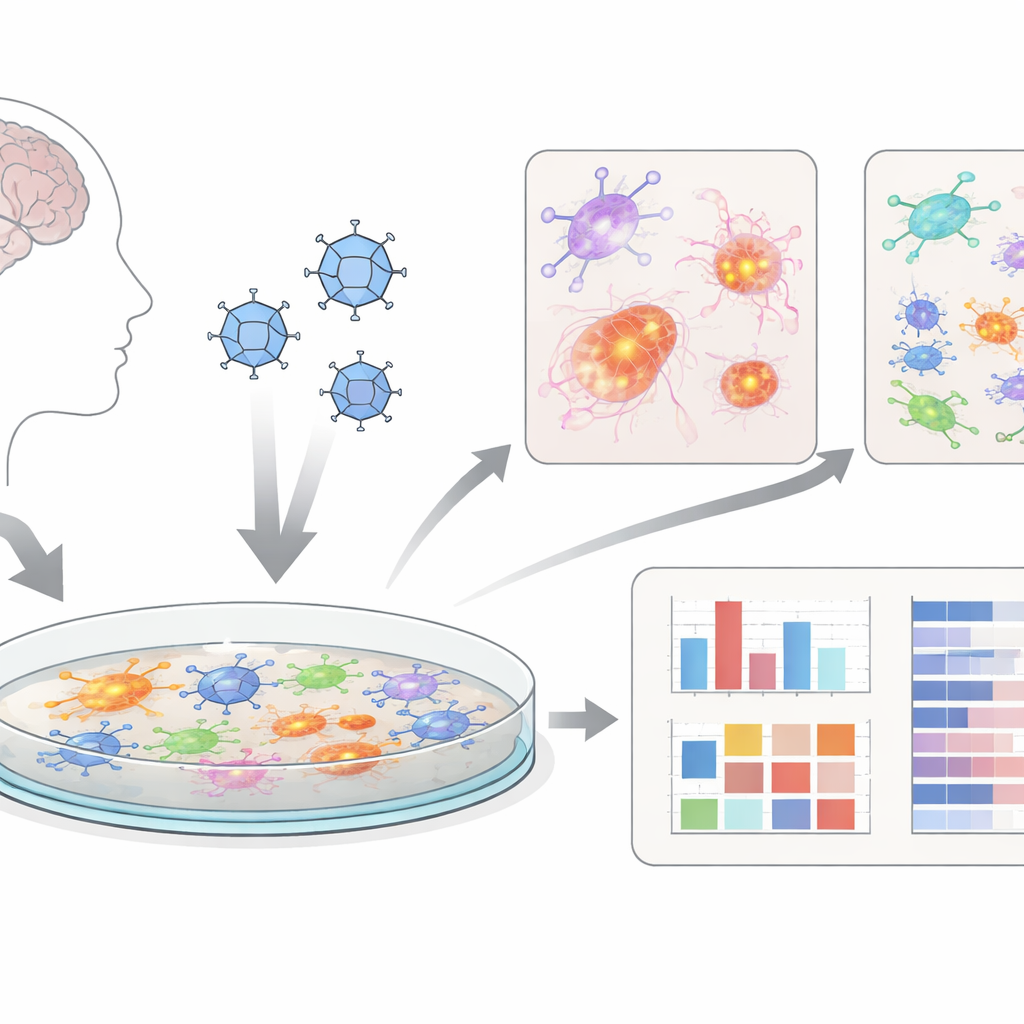
Mini-cervelli in coltura
Invece di lavorare soltanto con animali, i ricercatori hanno usato “organoidi cerebrali” – aggregati di cellule simili a quelle cerebrali cresciute da cellule staminali umane. Hanno quindi dissociato delicatamente questi organoidi 3D trasformandoli in strati piatti di cellule cerebrali miste, comprendenti neuroni, cellule di supporto chiamate astrociti e microglia con funzioni immunitarie. Queste colture bidimensionali, che chiamano dcOrgs, sono più facili da infettare in modo uniforme e adatte ai test ad alto rendimento, il che consente di esaminare in parallelo molte piastre e condizioni farmacologiche. Ciò rende il sistema interessante come strumento di screening per nuovi trattamenti.
Un virus da afta labiale come innesco
Il team ha infettato i dcOrgs con il virus herpes simplex 1 (HSV-1), il virus responsabile della maggior parte delle afte labiali e a lungo sospettato di contribuire alla demenza in alcune persone. Hanno confrontato le colture infettate con controlli trattati fittizi (mock), con colture trattate con un antivirale (aciclovir), con colture esposte a un altro virus (influenza A) e con virus inattivato con luce ultravioletta. Usando analisi automatizzate delle cellule e sequenziamento singola-cellula, hanno confermato che l’HSV-1 infettava robustamente molti tipi cellulari nel piatto, mentre il virus inattivato e l’influenza hanno prodotto pattern di cambiamento molto diversi e più blandi.
Cambiamenti simili all’Alzheimer dentro e tra le cellule
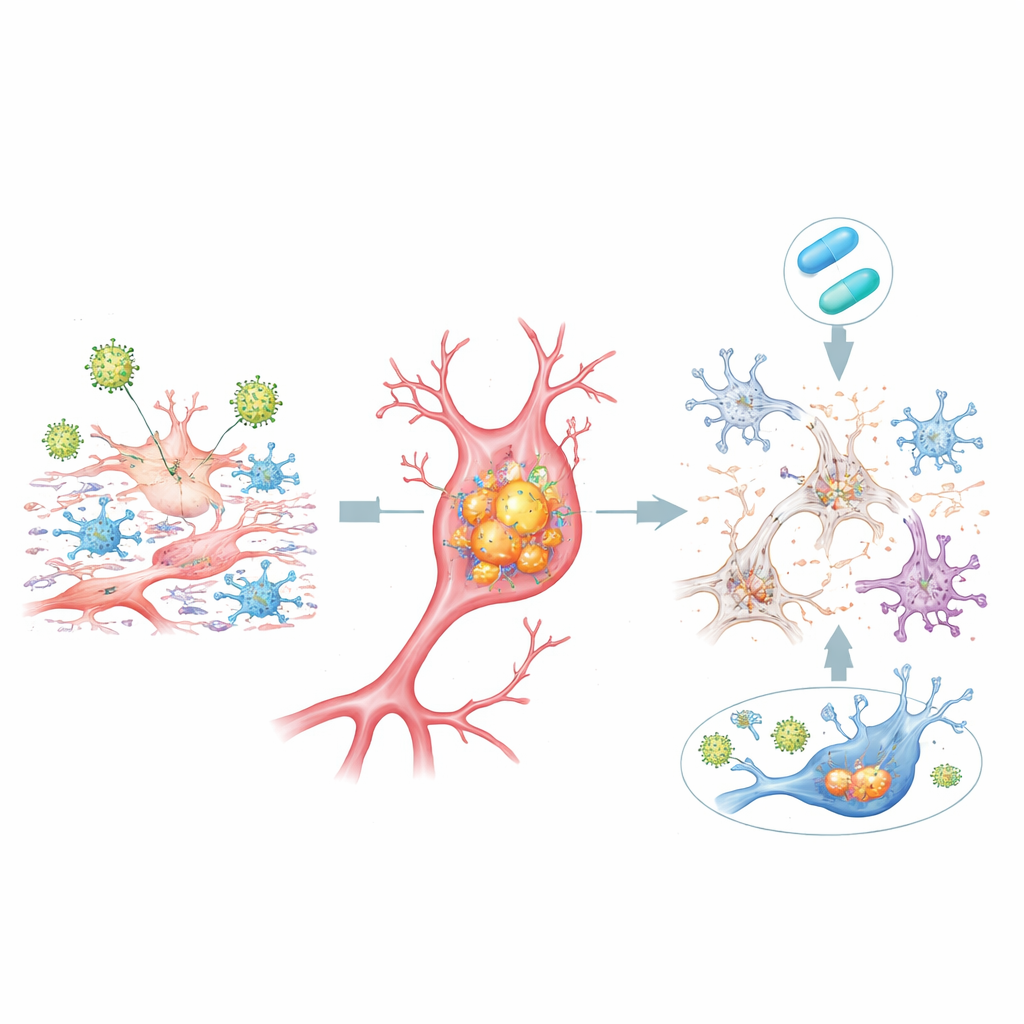
Nei dcOrgs infettati da HSV-1, molte cellule hanno accumulato alti livelli delle stesse forme proteiche osservate nei cervelli dei pazienti con Alzheimer: aggregati di beta-amiloide all’interno delle cellule e diverse versioni “fosforilate” della tau, un’altra proteina chiave della malattia. Questi accumuli erano strettamente associati alle cellule contenenti proteine virali ed erano particolarmente forti nelle cellule in via di morte. Allo stesso tempo, veniva rilasciata nel fluido circostante una minore quantità della forma più lunga del frammento beta-amiloide (Aβ42) rispetto alle forme più corte, uno spostamento che rispecchia i modelli misurati nel liquido cerebrospinale di pazienti con Alzheimer. Anche le popolazioni cellulari cambiarono: il numero di neuroni diminuì, mentre astrociti e microglia aumentarono, richiamando la perdita neuronale e l’infiammazione reattiva osservate nei tessuti cerebrali dei pazienti.
L’attività genica collega il modello all’Alzheimer umano
Quando i ricercatori hanno esaminato l’attività genica sull’intero genoma, hanno scoperto che l’infezione da HSV-1 nei dcOrgs accendeva e spegneva molti geni precedentemente collegati al rischio di Alzheimer in ampi studi genetici umani. Questi cambiamenti non sono stati osservati in colture più semplici di cellule staminali o in dcOrgs infettati dall’influenza, suggerendo un’interazione specifica tra HSV-1 e l’ambiente cerebrale misto. Il sequenziamento singola-cellula ha rivelato che alcune delle variazioni di geni legati all’Alzheimer provenivano da cellule esposte al virus ma con poco o nessun materiale genetico virale al loro interno, suggerendo che segnali provenienti da vicini infetti possono propagare programmi infiammatori dannosi.
Cosa può e non può correggere il trattamento antivirale
L’aggiunta dell’antivirale aciclovir poco dopo l’esposizione a HSV-1 ha ridotto l’espressione dei geni virali, attenuato molte risposte infiammatorie, diminuito l’accumulo intracellulare di beta-amiloide e tau tossiche e parzialmente ripristinato l’equilibrio tra i diversi tipi cellulari. Per una frazione consistente dei geni associati all’Alzheimer, i loro livelli di attività si sono riportati verso valori normali. Tuttavia, non tutti i cambiamenti erano reversibili: un gruppo significativo di geni umani è rimasto invariato o addirittura peggiorato dopo il trattamento, soprattutto quando il farmaco era meno efficace nel bloccare i geni virali tardivi. Questo sottolinea che, sebbene interrompere la replicazione virale possa aiutare, potrebbe non annullare completamente la cascata biologica una volta avviata.
Cosa significa per la comprensione dell’Alzheimer
Per un lettore non specialista, la conclusione è che un comune virus da afta labiale, agendo in un mix realistico di cellule cerebrali umane, può produrre rapidamente molte caratteristiche distintive della malattia di Alzheimer – dagli ammassi proteici e neuroni morenti fino a schemi genetici già osservati nei pazienti. Il sistema piatto basato su organoidi sviluppato qui è rapido, quantitativo e scalabile, rendendolo un potente banco di prova per antivirali e altre terapie volte a ridurre l’infiammazione cerebrale. Sebbene ciò non dimostri che le infezioni da herpes causino l’Alzheimer in ogni paziente, rafforza l’ipotesi che, in una sottopopolazione di persone, infezioni virali croniche o riattivate possano rappresentare un elemento importante del problema – e un potenziale bersaglio per la prevenzione.
Citazione: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Parole chiave: malattia di Alzheimer, herpes simplex, organoidi cerebrali, neuroinfiammazione, Terapia antivirale