Clear Sky Science · it
15 anni di misure genetiche, cliniche, cognitive, di imaging e biochimiche longitudinali in DIAN
Perché questo è importante per le famiglie e il futuro delle terapie per l’Alzheimer
La maggior parte delle persone pensa alla malattia di Alzheimer come a qualcosa che compare in tarda età, spesso senza preavviso. Ma in un piccolo numero di famiglie, specifiche variazioni genetiche ereditate quasi garantiscono che una persona svilupperà l’Alzheimer in età relativamente giovane. Lo studio osservazionale della Dominantly Inherited Alzheimer Network (DIAN) ha passato 15 anni a seguire da vicino queste famiglie in tutto il mondo. Osservando come la malattia si sviluppa molto prima che compaiano i problemi di memoria, DIAN sta rivelando una cronologia dettagliata dei cambiamenti cerebrali che potrebbe aiutare i medici a rilevare, prevenire o ritardare l’Alzheimer in molte più persone.
Un impegno globale che segue famiglie ad alto rischio
DIAN monitora adulti di famiglie portatrici di rare mutazioni in tre geni collegati a una forma ereditaria di Alzheimer. Alcuni partecipanti hanno la mutazione e altri no, ma nessuno di loro viene informato dallo studio sul proprio stato a meno che non scelga un test clinico separato. Il progetto è iniziato nel 2008 con 10 centri in tre paesi e si è ampliato fino a 23 siti operativi in 11 paesi, lavorando in sette lingue. Oltre 660 persone si sono iscritte, con più di 300 ancora attivamente coinvolte. Durante le visite periodiche, i volontari si sottopongono a esami medici e cognitivi, a scansioni cerebrali, a test sul liquido cerebrospinale e sul sangue e, per chi acconsente, alla donazione del cervello dopo la morte. I parenti non portatori fungono da gruppo di confronto insolitamente ben abbinato, aiutando i ricercatori a distinguere l’invecchiamento normale dai cambiamenti legati alla malattia.
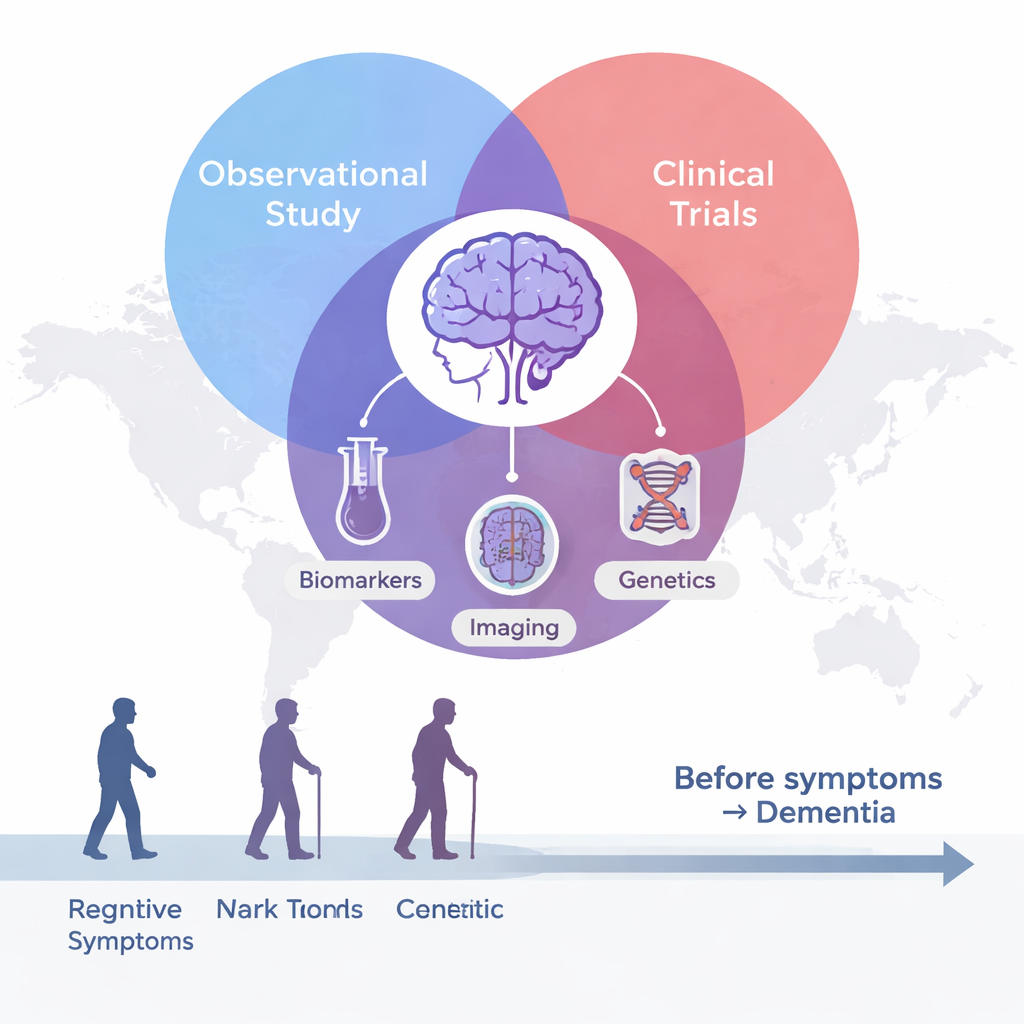
Vedere la malattia decenni prima dei sintomi
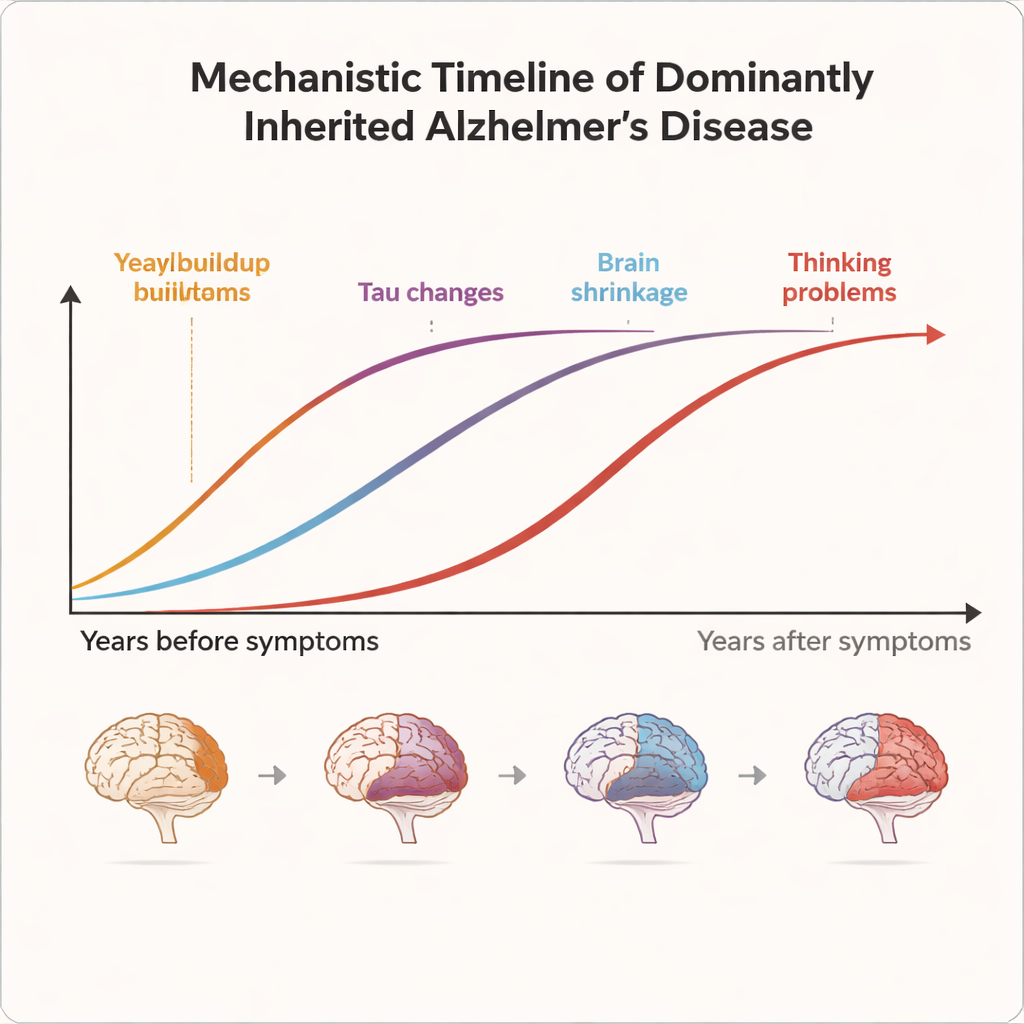
Poiché l’età in cui i sintomi di solito iniziano è abbastanza prevedibile all’interno di ogni famiglia, i ricercatori possono stimare quanti anni mancano all’esordio probabile per ciascun portatore. Questo permette di allineare le persone lungo un “orologio della malattia”, da oltre 20 anni prima dell’inizio dei problemi fino a molti anni dopo. I risultati DIAN mostrano che l’Alzheimer non è un evento improvviso ma un processo lungo. Ammassi proteici appiccicosi chiamati placche amiloidi iniziano ad accumularsi nel cervello 15–20 anni prima dei sintomi, evidenziandosi su scansioni PET specializzate e rispecchiandosi nella riduzione di una forma di amiloide nel liquido cerebrospinale. Circa 10–15 anni prima dell’esordio previsto emergono altri segnali: le proteine tau anomale aumentano nel liquido cerebrospinale, il metabolismo cerebrale rallenta e appare un sottile assottigliamento della corteccia nelle risonanze magnetiche. Solo diversi anni dopo diventano rilevabili i cambiamenti nel pensiero e nelle funzioni quotidiane nei test cognitivi dettagliati.
Una biblioteca vivente di misure e campioni
Per trasformare queste osservazioni in scienza utile a livello generale, DIAN ha costruito una delle collezioni più ricche al mondo di dati e tessuti correlati all’Alzheimer. Otto centri specializzati gestiscono informazioni cliniche, test cognitivi, imaging cerebrale, biomarcatori nei fluidi, genetica, patologia cerebrale, statistica e amministrazione generale. Campioni di sangue e liquido cerebrospinale sono trattati in una biobanca centrale, dove strumenti avanzati misurano dozzine di proteine legate ad amiloide, tau, infiammazione e danno neuronale. Analisi genetiche e “multi-omiche” esaminano DNA, RNA, proteine, lipidi e altre molecole nel sangue, nel tessuto cerebrale e nei modelli cellulari derivati dai partecipanti. Un programma di neuropatologia in crescita esamina con cura i cervelli donati per confermare le diagnosi e stadiare la malattia. Tutte queste informazioni vengono pulite, controllate per la qualità e congelate in set di dati annuali che i ricercatori esterni possono richiedere sotto rigorose garanzie di riservatezza.
Alimentare studi clinici e strumenti di nuova generazione
DIAN non è solo uno studio di ciò che accade naturalmente; è anche la spina dorsale di un programma di sperimentazioni cliniche complementare che testa farmaci volti a rallentare o prevenire l’Alzheimer ereditario. Poiché gli studi osservazionali e quelli di trattamento usano procedure armonizzate, i loro risultati possono essere combinati e confrontati. La dettagliata cronologia DIAN dei cambiamenti cerebrali ha già contribuito a definire criteri internazionali per caratterizzare l’Alzheimer biologicamente, basandosi su marcatori di amiloide, tau e neurodegenerazione piuttosto che solo sui sintomi. Guardando avanti, la rete si sta espandendo verso valutazioni a distanza tramite app per smartphone, visite domiciliari e dispositivi indossabili per rilevare i cambiamenti cognitivi molto precoci e monitorare la funzione quotidiana. Investe inoltre pesantemente in test su base ematica e in profilazioni molecolari più profonde per trovare nuovi bersagli terapeutici e capire perché la malattia progredisce in modo diverso tra individui e popolazioni.
Cosa significa questo per chi teme l’Alzheimer
Lo studio DIAN mostra che nell’Alzheimer ereditario il cervello inizia a cambiare molti anni prima che la memoria venga compromessa — e che questi mutamenti nascosti possono essere misurati nel sangue, nel liquido cerebrospinale e nelle scansioni. Sebbene le mutazioni studiate siano rare, il processo patologico sottostante sembra assomigliare molto a quello della forma molto più comune ad esordio tardivo dell’Alzheimer. Questo rende DIAN un modello potente per l’intero campo. Mappando passo dopo passo il percorso dal cervello sano alla demenza, e condividendo le sue risorse raccolte con cura in tutto il mondo, DIAN aiuta gli scienziati a progettare interventi più precoci e più precisi. Per le famiglie che affrontano un rischio ereditario e per i milioni di persone colpite dall’Alzheimer in senso più ampio, queste intuizioni offrono un percorso più chiaro verso una rilevazione precoce, un monitoraggio migliore e, in ultima analisi, una prevenzione e terapie più efficaci.
Citazione: Daniels, A.J., McDade, E., Llibre-Guerra, J.J. et al. 15 years of longitudinal genetic, clinical, cognitive, imaging, and biochemical measures in DIAN. npj Dement. 2, 13 (2026). https://doi.org/10.1038/s44400-025-00047-7
Parole chiave: Malattia di Alzheimer, demenza genetica, biomarcatori cerebrali, studio longitudinale, rilevamento precoce