Clear Sky Science · it
Codificare i bordi funzionali nei grafi per modellare le relazioni spazialmente variabili nel microambiente tumorale
Perché mappare il quartiere del cancro è importante
Il cancro non cresce in isolamento. Le cellule tumorali vivono in un quartiere affollato di cellule immunitarie, cellule di supporto, vasi sanguigni e segnali chimici, tutti stretti nello spazio. Come questi vicini sono disposti e quanto intensamente si influenzano a vicenda può determinare se un tumore si diffonde, risponde a una terapia o resta controllato. Questo articolo presenta SPIFEE, un nuovo framework di intelligenza artificiale che trasforma immagini microscopiche e mappe molecolari dei tumori in reti, aiutando i ricercatori a individuare quali interazioni tra cellule e vie molecolari sono più legate al tipo di malattia e all’esito del paziente.
Trasformare il tessuto in una mappa a rete
Gli studi moderni sul cancro possono misurare molto più di come appare un tumore al microscopio. Alcuni metodi evidenziano decine di proteine su singole cellule, altri forniscono vetrini colorati dettagliati della struttura tissutale, e strumenti più recenti registrano quali geni sono attivi in migliaia di punti su una sezione tumorale. SPIFEE tratta tutte queste misure come diverse viste dello stesso quartiere. Rappresenta ogni campione come un grafo: i nodi rappresentano entità chiave nel microambiente tumorale—come tipi cellulari, pattern visivi del tessuto o vie molecolari—mentre i bordi catturano come queste entità interagiscono nello spazio. Crucialmente, SPIFEE non riduce un’interazione a un singolo numero come la “distanza”. Invece, ogni bordo immagazzina una piccola curva che descrive quanto intensamente due entità si mescolano o si respingono su un intervallo di distanze, preservando dettagli spaziali molto più ricchi.
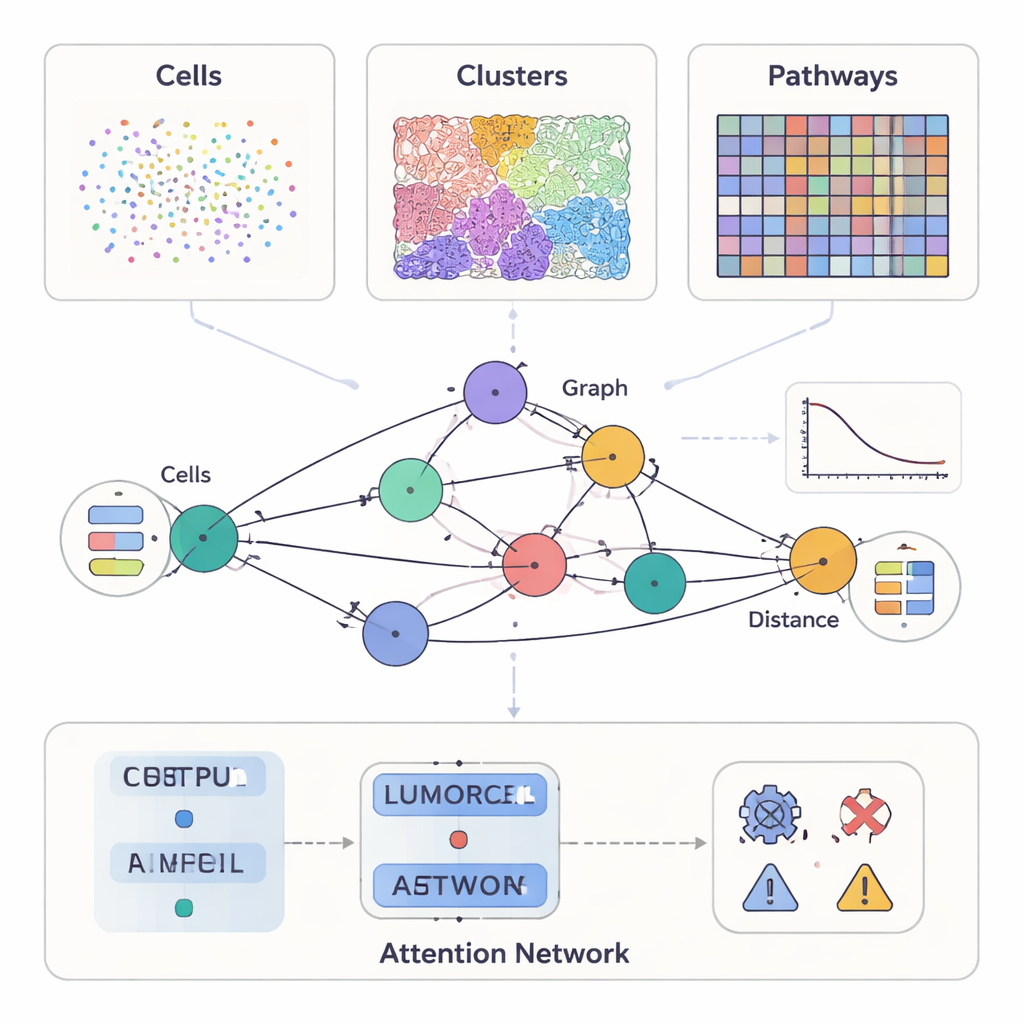
Una lente flessibile su molti tipi di dati oncologici
Gli autori hanno testato SPIFEE su diversi grandi dataset indipendenti di tumori che coprono tecnologie e scale differenti. Nei campioni di patologia pancreatica marcati con immunofluorescenza multiplex, ogni nodo del grafo rappresentava un tipo cellulare, e le caratteristiche dei nodi provenivano da RNA-seq a singola cellula che riassumeva come tali cellule tendono a comunicare. Nei vetrini polmonari colorati con il metodo di routine ematossilina-eosina, i nodi rappresentavano pattern visivi ricorrenti del tessuto, scoperti automaticamente da un sistema di apprendimento auto-supervisionato. In un terzo contesto, vetrini standard di carcinoma polmonare sono stati convertiti da uno strumento di deep learning in una trascrittomica spaziale virtuale, e i nodi SPIFEE rappresentavano vie molecolari come ipossia, estrogeni o segnalazione JAK–STAT, con caratteristiche derivate dall’attività genica. In tutti questi casi, lo stesso framework è stato in grado di ingerire diversi tipi di nodi e costruire grafi spaziali comparabili.
Trovare le interazioni che distinguono gli esiti clinici
Una volta che SPIFEE costruisce un grafo, lo passa attraverso una graph attention network, un tipo di rete neurale che impara non solo a predire un esito—come sottotipo di tumore, rischio di sopravvivenza o malattia versus infiammazione non cancerosa—ma anche a evidenziare quali bordi hanno pesato di più in quella predizione. Nel tessuto pancreatico, SPIFEE ha distinto la pancreatite cronica dall’adenocarcinoma duttale pancreatico con maggiore accuratezza rispetto a metodi grafici precedenti. Il modello si è concentrato costantemente su interazioni che coinvolgevano cellule epiteliali (simili a tumorali) e cellule T regolatorie, cellule presentanti l’antigene e cellule T helper, indicando un quartiere immunosoppressivo più pronunciato nel cancro rispetto all’infiammazione. Nei vetrini di adenocarcinoma polmonare, SPIFEE ha identificato particolari pattern stroma-tumore le cui interazioni si sono correlate con esiti di sopravvivenza migliori o peggiori, suggerendo che le “zone di confine” tra tumore e tessuto di supporto codificano indizi prognostici importanti che analisi standard possono perdere.
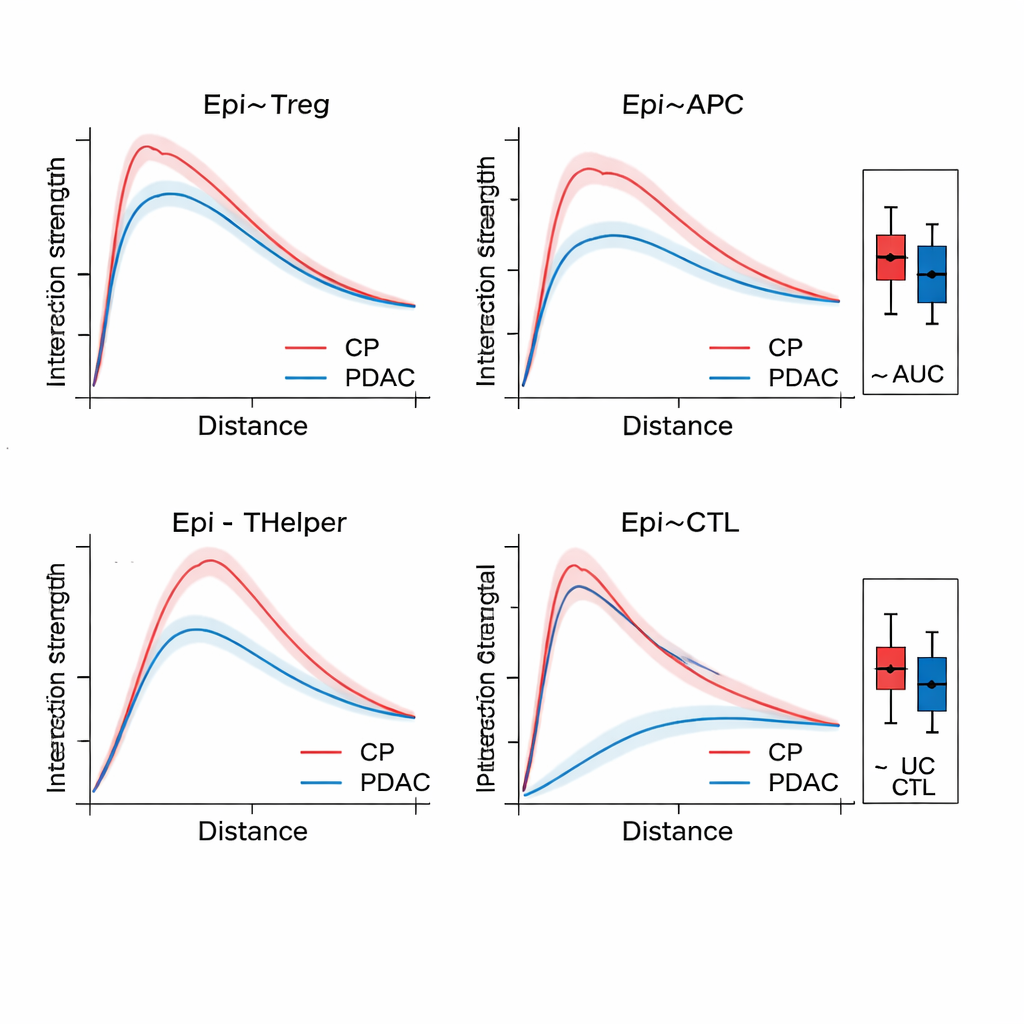
Leggere il dialogo molecolare da vetrini di routine
Forse in modo più sorprendente, SPIFEE è stato in grado di inferire interazioni significative tra vie molecolari da semplici immagini di patologia una volta che queste sono state tradotte in mappe di attività genica previste. Trattando le vie come nodi e la loro co-occorrenza spaziale come bordi funzionali, il metodo ha messo in luce coppie come ipossia con EGFR o JAK–STAT con PI3K—combinazioni già note per guidare l’evasione immunitaria e la resistenza ai farmaci nel cancro del polmone. Ha inoltre evidenziato vie correlate agli estrogeni nell’adenocarcinoma polmonare e alcune vie immunitarie e di stress nei tumori squamosi, risultati coerenti con pattern osservati in RNA-seq bulk e in un dataset indipendente di trascrittomica spaziale reale. Ciò suggerisce che, anche quando le misure molecolari sono approssimate, i pattern spaziali nei vetrini di routine conservano segnali recuperabili su come le vie chiave interagiscono nei tumori viventi.
Cosa significa per la futura cura del cancro
Per un non specialista, il messaggio chiave è che SPIFEE offre un nuovo modo di leggere la “vita sociale” delle cellule tumorali direttamente da immagini e mappe molecolari. Codificando come le relazioni cambiano con la distanza invece di appiattirle in punteggi singoli, e utilizzando reti neurali basate sull’attenzione per classificare quali interazioni sono più importanti, il framework può scoprire combinazioni di cellule, pattern tissutali e vie che distinguono i tipi di cancro e predicono la sopravvivenza. Pur richiedendo ancora validazione biologica e clinica, approcci come SPIFEE indicano un futuro in cui i campioni tumorali di routine possono fornire non solo istantanee statiche, ma mappe dinamiche di hotspot di interazione che aiutino a guidare diagnosi, stratificazione del rischio e, infine, scelte terapeutiche personalizzate.
Citazione: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Parole chiave: microambiente tumorale, trascrittomica spaziale, reti neurali grafiche, patologia oncologica, interazioni cellula-cellula