Clear Sky Science · it
Una rete neurale informata dal metabolismo identifica le vie che influenzano potenza e tossicità delle combinazioni antimicrobiche
Perché questo è importante per la salute di tutti i giorni
Man mano che sempre più infezioni smettono di rispondere ai nostri antibiotici di prima scelta, i medici ricorrono sempre più spesso a combinazioni di farmaci. Ma mescolare medicinali può essere un’arma a doppio taglio: la coppia giusta può eliminare batteri ostinati, mentre la combinazione sbagliata può danneggiare organi come reni e fegato. Questo studio presenta un nuovo approccio informatico, chiamato CALMA, pensato per aiutare scienziati e clinici a trovare combinazioni che siano potenti contro i microrganismi e al tempo stesso più sicure per i pazienti.
Combattere i germi senza tentativi a caso
Tradizionalmente, scoprire buone combinazioni di antibiotici significava testare in laboratorio e sui pazienti un numero enorme di coppie o terne di farmaci. Il numero di miscele possibili cresce esplosivamente con ogni farmaco aggiunto, rendendo irrealistico un test sperimentale completo. Inoltre, la maggior parte degli strumenti esistenti si concentra solo su quanto efficacemente le combinazioni uccidono i batteri, ignorando il potenziale danno ai tessuti umani. Gli autori sostengono che per progettare terapie migliori dobbiamo considerare entrambe le facce della medaglia: l’efficacia contro i patogeni e la sicurezza per le persone.
Un modello intelligente che comprende la chimica cellulare
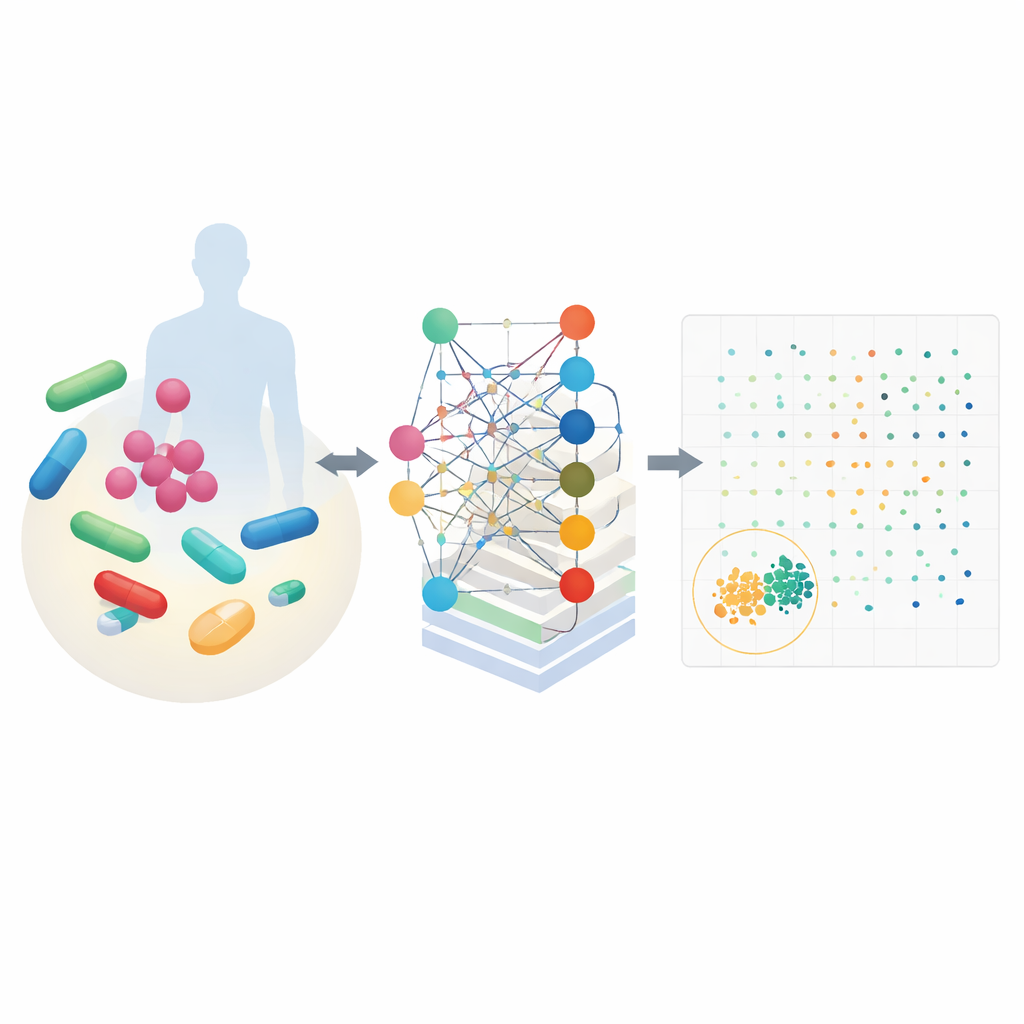
CALMA combina due idee potenti. Innanzitutto utilizza mappe dettagliate del metabolismo cellulare che descrivono come gli organismi trasformano nutrienti in energia e mattoni di costruzione. Queste mappe, costruite per batteri come Escherichia coli e il germe della tubercolosi, simulano come migliaia di reazioni chimiche cambiano in presenza di un farmaco. In secondo luogo, CALMA alimenta queste simulazioni in una rete neurale artificiale la cui struttura rispecchia le vie metaboliche. Raggruppando le informazioni secondo rotte biologiche note—come la produzione di energia o il riciclo dei nucleotidi—il modello apprende schemi che collegano specifiche vie sia all’efficacia antibatterica sia agli effetti collaterali dannosi nelle cellule umane.
Esplorare il panorama delle miscele farmacologiche
Utilizzando dati di esperimenti precedenti e grandi banche dati sulla sicurezza, i ricercatori hanno addestrato CALMA per assegnare a ogni combinazione di farmaci due punteggi: uno per quanto colpisce i batteri e un altro per la probabilità di tossicità nelle persone. Tracciando questi valori si crea un paesaggio in cui i migliori candidati si trovano in basso a sinistra—forti contro i microrganismi e poco aggressivi sulle cellule umane. Applicando CALMA a 35 farmaci di rilievo clinico, lo strumento ha ristretto quasi 600 coppie possibili a un piccolo insieme di opzioni promettenti, riducendo lo spazio di ricerca sperimentale di circa il 97 percento. Tra le principali proposte figuravano combinazioni che coinvolgevano antibiotici comuni come azitromicina, vancomicina, isoniazide e trimetoprim.
Dalle previsioni al computer ai test in laboratorio e ai pazienti reali
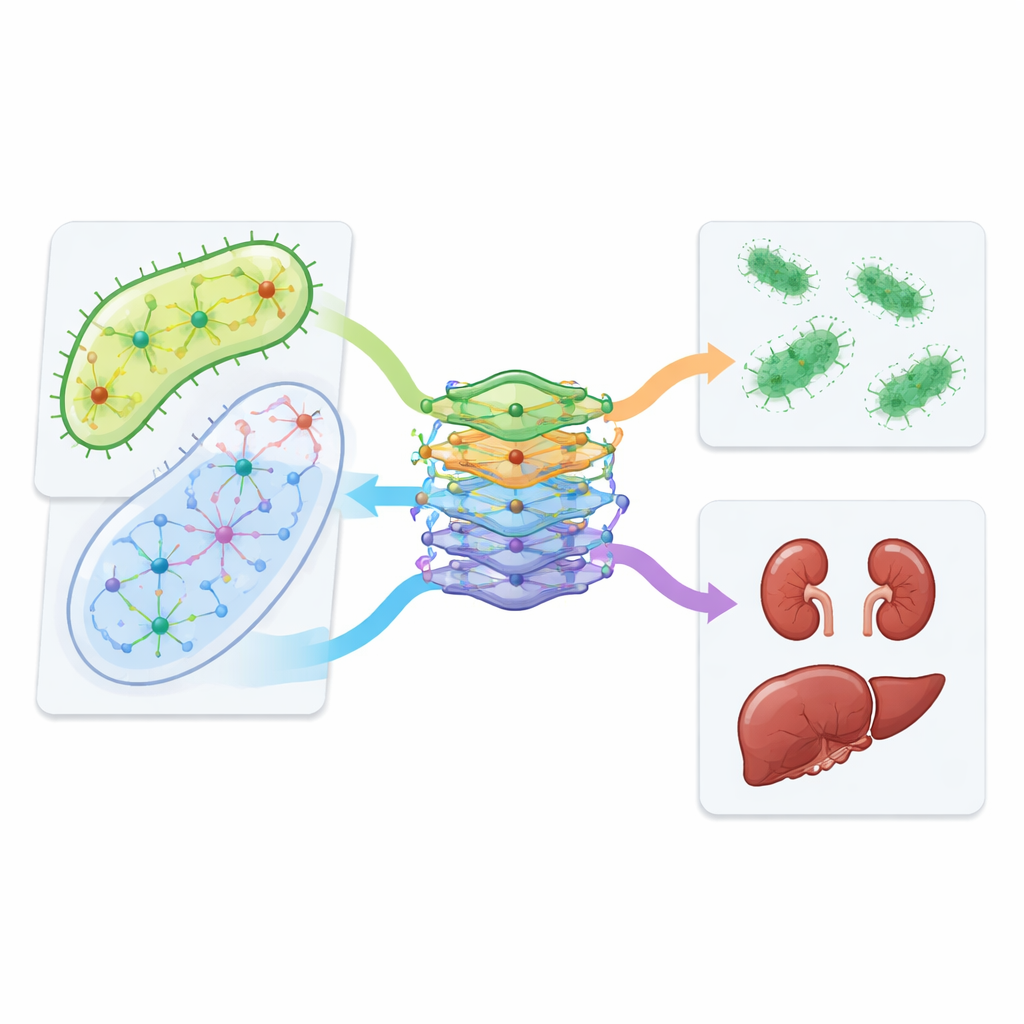
Il gruppo è andato oltre le simulazioni per testare in linee cellulari renali ed epatiche diverse combinazioni previste. Hanno scoperto che alcune coppie, inclusa l’azitromicina con vancomicina e l’isoniazide con trimetoprim, erano meno tossiche per le cellule umane rispetto ai singoli farmaci, pur mantenendo attività contro E. coli. La progettazione di CALMA ha anche permesso ai ricercatori di indagare quali rotte metaboliche guidano la tossicità. Una via che ricicla i mattoni del DNA, nota come recupero dei nucleotidi, è emersa come fattore chiave: modificarla in esperimenti cellulari cambiava la pericolosità di alcune combinazioni. Infine, gli autori hanno esaminato cartelle cliniche di centinaia di migliaia di pazienti e hanno osservato che le persone trattate con azitromicina insieme a vancomicina avevano meno problemi renali documentati rispetto a pazienti simili trattati solo con vancomicina, in linea con i risultati di laboratorio.
Cosa significa per le terapie future
Per un non specialista, CALMA può essere pensata come un filtro intelligente che comprende abbastanza biologia da suggerire quali miscele di farmaci vale la pena testare per prime. Invece di mescolare antibiotici alla cieca e sperare nel meglio, i ricercatori possono concentrarsi su combinazioni che i modelli prevedono colpiranno i punti deboli batterici risparmiando le vie umane vulnerabili. Sebbene il metodo dipenda dai dati disponibili e non sia perfetto, offre una strada più razionale per progettare terapie combinate. Col tempo, strumenti come CALMA potrebbero aiutare i medici a trattare le infezioni resistenti in modo più sicuro, ridurre il trial-and-error nello sviluppo di farmaci e persino essere adattati ad altre malattie in cui combinazioni terapeutiche ed effetti collaterali sono preoccupazioni importanti.
Citazione: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Parole chiave: combinazioni di antibiotici, tossicità dei farmaci, reti neurali artificiali, metabolismo, resistenza antimicrobica