Clear Sky Science · it
Generazione molecolare 3D vincolata dalle interazioni tramite un modello di diffusione consente la modellizzazione farmacoforica basata sulla struttura per la progettazione di farmaci
Perché è così difficile progettare farmaci migliori
La scoperta di farmaci moderna spesso si basa sul convincere una piccola molecola a inserirsi in una proteina come una chiave in una serratura. Ma la chiave deve fare più che entrare: deve formare il giusto insieme di piccole attrazioni — come deboli forze elettriche e zone che evitano l’acqua — affinché il farmaco rimanga legato in modo forte e specifico. L’universo chimico è astronomicamente vasto, molto oltre ciò che contengono gli attuali database, così i ricercatori cercano modi più intelligenti per inventare nuove chiavi da zero preservando questi cruciali schemi di contatto.
Insegnare a un computer ciò che conta davvero
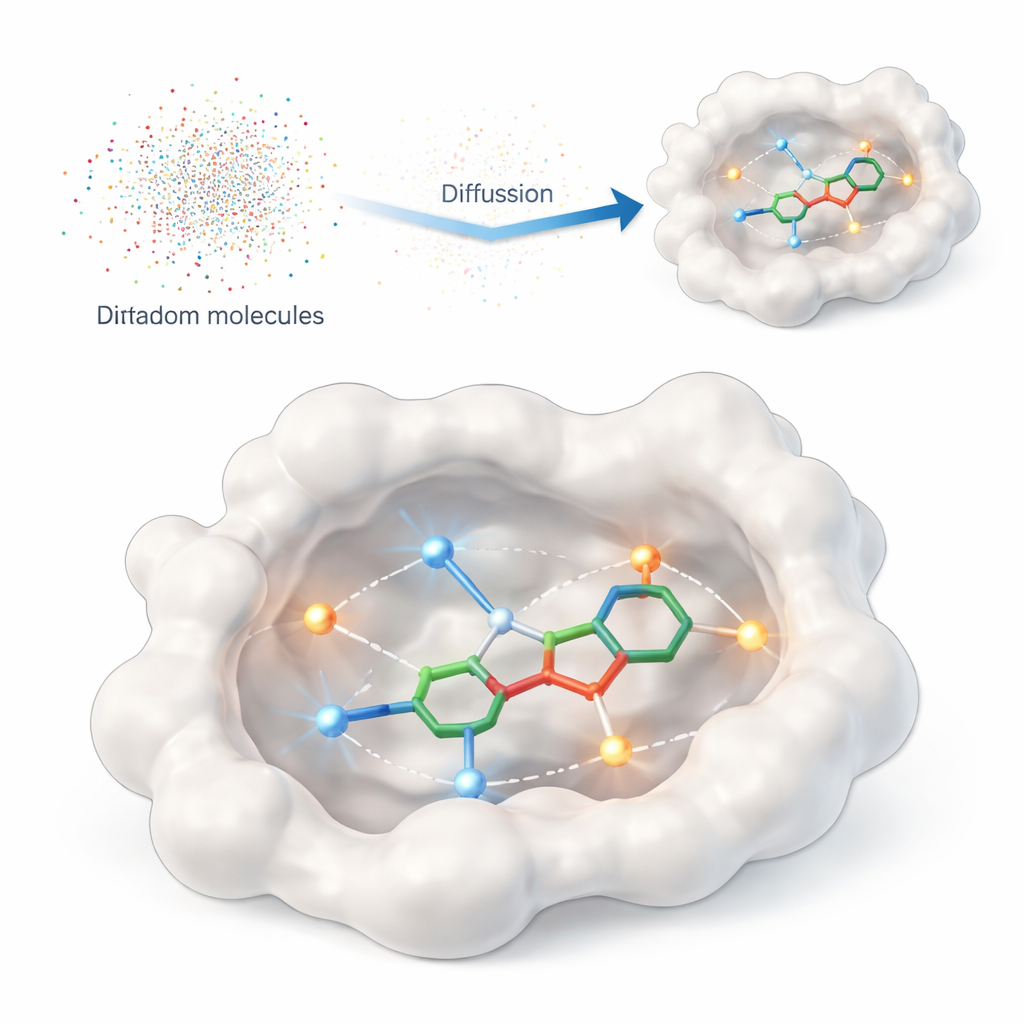
Questo studio presenta DiffPharma, un framework computazionale che genera molecole tridimensionali simili a farmaci direttamente all’interno del sito di legame di una proteina. Invece di chiedere all’algoritmo di cercare in enormi cataloghi di composti esistenti, DiffPharma crea nuove molecole atomo per atomo, guidato da come dovrebbero interagire con la proteina. Il metodo è costruito su una classe moderna di modelli generativi chiamati modelli di diffusione, che partono da rumore casuale e lo “denoisano” gradualmente in un oggetto strutturato — in questo caso, una molecola 3D adagiata nella tasca proteica.
Codificare la stretta di mano della proteina
Per dire al modello cosa conta sulla superficie della proteina, gli autori rappresentano i contatti chiave come piccole “particelle di interazione” sparse lungo i percorsi tra la proteina e una molecola di riferimento. Due tipi di interazione comuni sono messi in evidenza: legami a idrogeno, che agiscono come magneti direzionali tra atomi specifici, e contatti idrofobici, dove regioni oleose si raggruppano allontanandosi dall’acqua. Reti neurali separate apprendono la geometria e la chimica di ciascun tipo di interazione, così come la forma complessiva della tasca di legame, e poi una speciale architettura di fusione combina questi punti di vista in un’unica immagine coerente che guida la generazione delle molecole.
Quanto bene imita i reali schemi di legame?
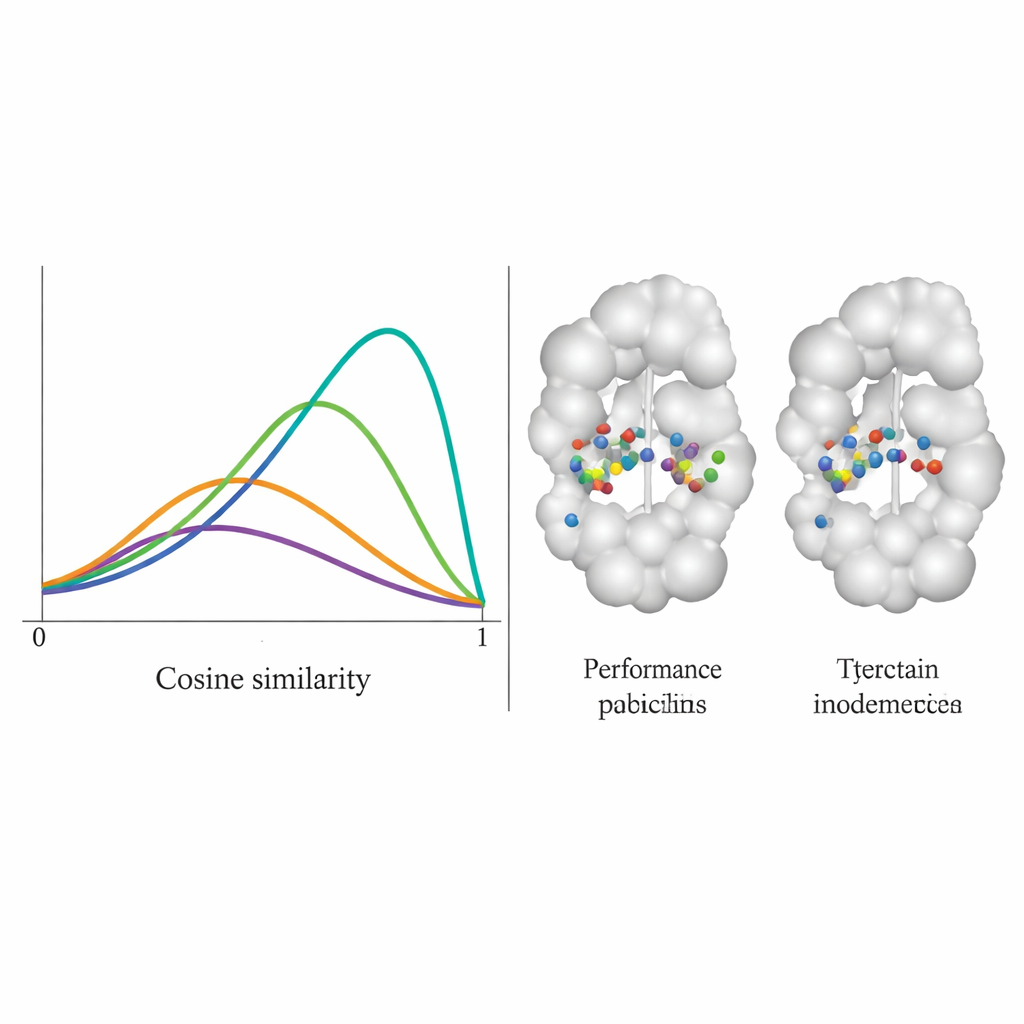
Il team ha testato DiffPharma su 100 diverse coppie proteina‑molecola e ha valutato quanto fedelmente le nuove molecole riproducessero gli schemi di contatto originali, residuo per residuo. Hanno misurato questo usando un punteggio di similarità coseno compreso tra 0 e 1, dove 1 indica accordo perfetto. La distribuzione di DiffPharma ha mostrato un picco attorno a 0,9, il che significa che, in media, gli stessi residui proteici formavano gli stessi tipi di interazioni chiave presenti nelle strutture di riferimento — sostanzialmente meglio rispetto a sei metodi concorrenti. È importante che il modello abbia fatto ciò pur producendo una varietà di forme molecolari, e i composti generati mantenevano lunghezze e angoli di legame realistici e una geometria 3D complessiva tipica di molecole reali e stabili.
Dalla teoria a potenziali candidati farmaceutici
Oltre ai benchmark, gli autori hanno chiesto se DiffPharma potesse progettare candidati farmaceutici plausibili per bersagli reali. Per due enzimi ben studiati — la chinasi AKT e una β‑lattamasi legata alla resistenza agli antibiotici — il metodo ha generato molecole che preservavano gli schemi di interazione essenziali dei ligandi noti ma spesso utilizzando scaffold chimici diversi, una forma desiderabile di “scaffold hopping” in chimica medicinale. In uno studio di caso più impegnativo sulla proteasi principale di SARS‑CoV‑2, DiffPharma è stato guidato usando scelte di interazione specifiche e poi esaminato con simulazioni di dinamica molecolare e stime dell’energia di legame. Le molecole generate sotto vincoli di interazione più stringenti hanno formato complessi più stabili e talvolta mostravano energie di legame previste più favorevoli rispetto a un inibitore di riferimento noto. Notevolmente, il sistema ha persino riscoperto quel composto di riferimento — nonostante non fosse mai apparso nell’addestramento — partendo unicamente dalla struttura proteica e dalle istruzioni di interazione.
Cosa significa per i farmaci del futuro
Per un non specialista, DiffPharma può essere visto come uno strumento intelligente e consapevole della 3D per progettare molecole farmaceutiche: fornita la forma di una tasca proteica e uno schema desiderato di “stretta di mano”, propone chiavi chimicamente ragionevoli che si adattano e interagiscono nel modo giusto. Pur non ottimizzando ancora tutte le proprietà necessarie a un medicinale, come solubilità o metabolismo, il metodo preserva in modo affidabile la mappa di contatti cruciale sulla superficie proteica ed esplora nuove regioni dello spazio chimico oltre gli attuali cataloghi. Questo approccio guidato dalle interazioni potrebbe aiutare i ricercatori a passare più rapidamente dai dati strutturali di proteine legate a malattie a punti di partenza diversi e realistici per lo sviluppo sperimentale di farmaci.
Citazione: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
Parole chiave: progettazione di farmaci basata sulla struttura, modelli generativi molecolari, modellizzazione farmacoforica, interazioni proteina‑ligando, proteasi principale di SARS‑CoV‑2