Clear Sky Science · it
Inferire anomalie delle vie di segnalazione da immagini istopatologiche tramite grafo di conoscenza eterogeneo gene-via vincolato da logica
Vedere i segnali cellulari nascosti nelle vetrini di cancro
Quando i medici esaminano il cancro al microscopio, osservano soprattutto forme e colori, non le complesse conversazioni molecolari che avvengono all’interno delle cellule. Eppure queste «conversazioni» di segnalazione invisibili tra geni e vie spesso determinano come un tumore cresce e come può rispondere al trattamento. Questo studio presenta un nuovo sistema di intelligenza artificiale che legge le immagini patologiche routinarie e inferisce quali rotte di comunicazione cellulare, o vie, stanno andando in errore—offrendo un modo per intravedere il comportamento molecolare senza test di laboratorio aggiuntivi.
Dalle tracce di singoli geni al quadro più ampio
Gli approcci tradizionali cercano di prevedere lo stato di singoli geni dalle immagini tissutali: un dato gene è mutato o no? Questo è utile, ma il cancro raramente dipende da un singolo gene guasto. Piuttosto, gruppi di geni agiscono insieme per alterare intere vie di segnalazione che controllano crescita, sopravvivenza e immunità. Gli autori sostengono che concentrarsi su singoli geni perde questo comportamento cooperativo e può fallire nel spiegare perché i tumori appaiono e si comportano in un certo modo al microscopio.
Costruire una mappa tra immagini, geni e vie
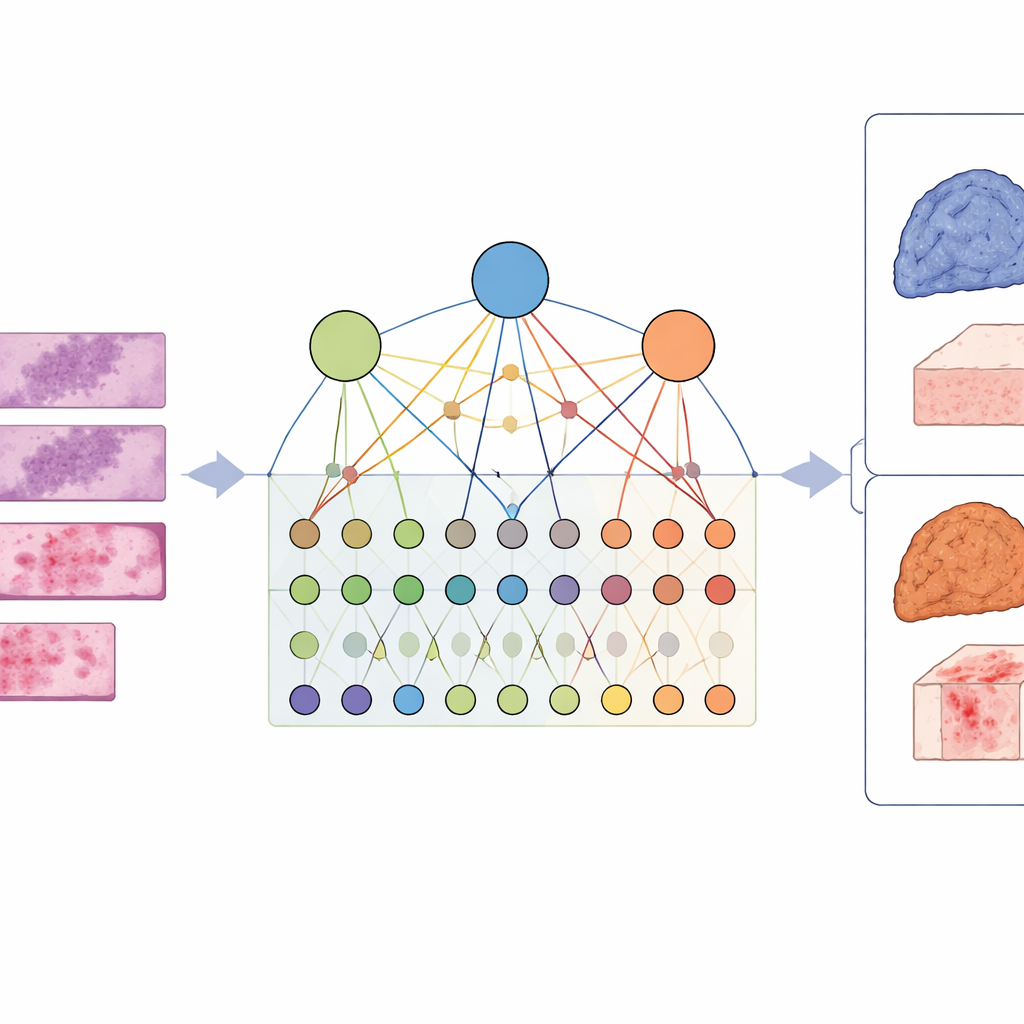
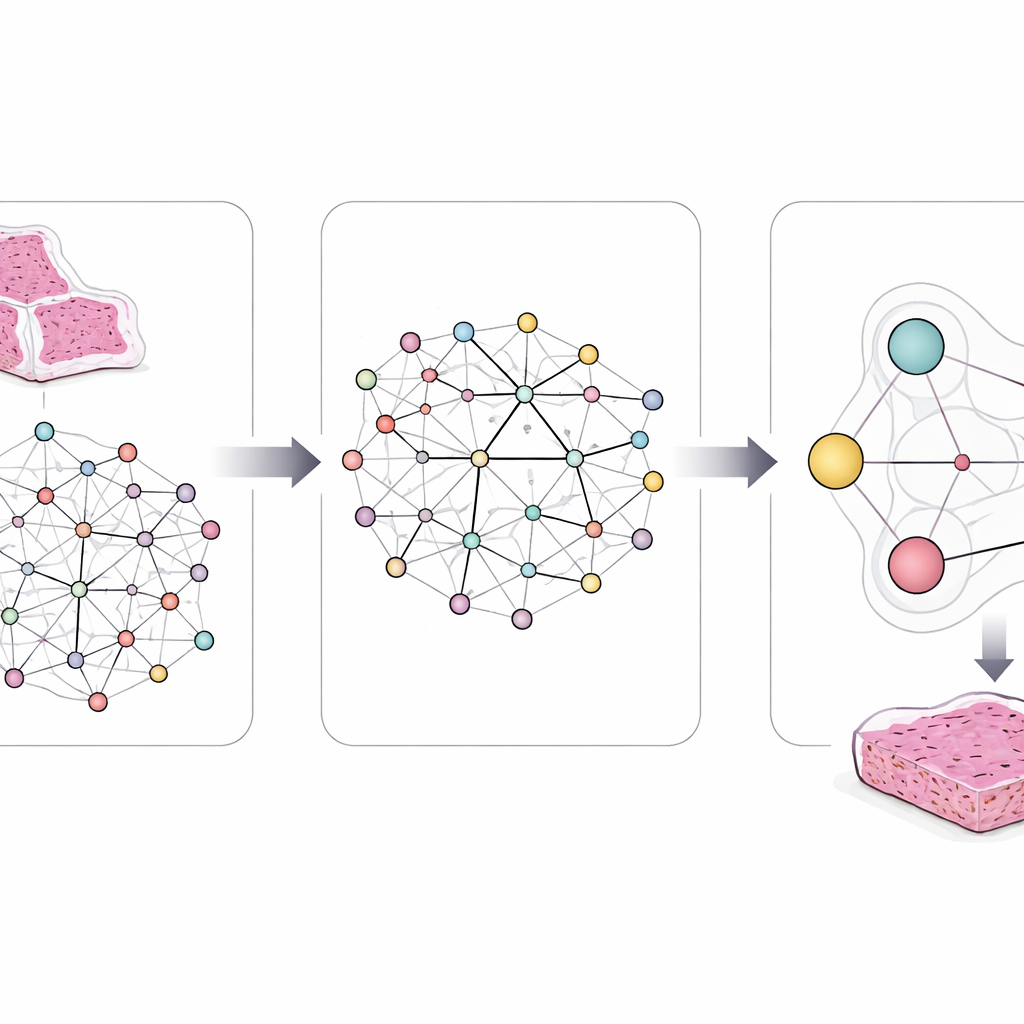
Per captare questa complessità, i ricercatori hanno progettato un framework chiamato LCG-HGNN che collega tre livelli di informazione. Innanzitutto, suddividono ogni immagine in vetrino di adenocarcinoma polmonare in molte piccole porzioni e rappresentano queste porzioni come un grafo, dove regioni vicine o dall’aspetto simile sono connesse. In secondo luogo, collegano marcatori genici alle vie di segnalazione usando banche dati biologiche consolidate, costruendo un secondo grafo che codifica quali geni appartengono a quali vie. Infine, consentono a un modello di IA di far circolare informazioni attraverso questo grafo combinato, in modo che pattern delle immagini, geni e vie si influenzino a vicenda anziché essere trattati in isolamento.
Insegnare al sistema la biologia nota
Un’innovazione chiave è che al modello non è permesso apprendere liberamente senza guida. Gli autori incorporano dichiarazioni chiare, simili a regole, derivate da decenni di ricerca sul cancro. Per esempio, alcune mutazioni appaiono quasi mai insieme nello stesso tumore, e alcune vie sono a monte o a valle di altre. Codificano tali regole come vincoli logici che indirizzano delicatamente le connessioni interne e le predizioni dell’IA. Se il modello propone una combinazione di cambiamenti genici e di vie che confligge con la biologia nota o con somiglianze tra i vetrini dei pazienti, queste regole lo spingono verso alternative più realistiche.
Mettere alla prova l’accuratezza rispetto ai metodi esistenti
Il team ha valutato il proprio sistema su oltre 1.600 vetrini di cancro polmonare collegati a dati genetici. Lo hanno confrontato con modelli di deep learning standard che si concentrano su singoli geni e con metodi più avanzati che gestiscono molti geni contemporaneamente ma ignorano la struttura delle vie. In diverse vie importanti, incluse quelle coinvolte nei segnali di crescita cellulare e nello scheletro di supporto del tessuto, il nuovo modello ha previsto con maggiore accuratezza i cambiamenti nei gruppi genici e le anomalie delle vie. Ha inoltre prodotto porzioni di immagine il cui aspetto corrispondeva strettamente a esempi clinici reali noti per essere associati a mutazioni specifiche, suggerendo che si concentrava su pattern microscopici significativi piuttosto che su stranezze casuali dell’immagine.
Perché questo è importante per i pazienti
Per un non specialista, il risultato principale è che questo approccio trasforma un vetrino di patologia di routine in una ricca fonte di informazioni molecolari. Invece di ordinare test genetici separati, spesso costosi, per ogni possibile bersaglio, i medici potrebbero in futuro usare modelli simili per esaminare vie alterate direttamente dalle immagini che già raccolgono. Sebbene il metodo necessiti ancora di una convalida più ampia nel mondo reale e non sostituisca ancora i test genomici, indica un futuro in cui la visione al microscopio raddoppia come finestra sul cablaggio interno del tumore—aiutando a guidare una cura del cancro più precisa e informata biologicamente.
Citazione: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Parole chiave: vie del cancro, IA in istopatologia, reti neurali su grafo, adenocarcinoma polmonare, patologia digitale