Clear Sky Science · it
Ingegnerizzare i macrofagi per l’immunoterapia del cancro: nuovi insight e potenziale terapeutico
Trasformare la “squadra di pulizia” del corpo in combattenti contro il cancro
I nostri corpi sono pieni di macrofagi—cellule «addette alla pulizia» che pattugliano l’organismo ingerendo germi e tessuto morto. Questa recensione esplora come gli scienziati stanno imparando a reindirizzare queste cellule contro il cancro. Poiché i macrofagi sono abbondanti all’interno dei tumori, compresi quelli che resistono alle attuali immunoterapie di punta, comprenderli e ingegnerizzarli potrebbe aprire nuove opzioni per i pazienti con tumori difficili da trattare.
Le molte facce di un unico tipo cellulare
I macrofagi non sono un tipo cellulare fisso; sono dei trasformisti. Possono arrivare dal flusso sanguigno o risiedere già nei tessuti e, una volta stabiliti, rispondono ai segnali locali. Nei tumori, questi macrofagi associati al tumore possono o uccidere le cellule tumorali o, in modo contraddittorio, favorire la crescita e la diffusione del tumore. In precedenza i ricercatori cercavano di incasellarli in due categorie—«M1» (modalità attacco) e «M2» (modalità riparazione o supporto). Nuovi strumenti di mappatura genetica e spaziale mostrano ora uno spettro molto più ricco di stati, con molte sottopopolazioni e comportamenti che variano da tumore a tumore e da zona a zona. Anche cellule un tempo considerate saldamente «pro-tumore» possono, in certi contesti, reclutare linfociti T e sostenere l’immunità anti-tumorale.
Sensare l’ambiente e inghiottire le cellule tumorali
I macrofagi non si limitano ad ascoltare segnali chimici; percepiscono anche il mondo fisico che li circonda. Mentre si muovono attraverso la fitta rete proteica di un tumore, si insinuano tra le cellule e subiscono forze dei fluidi, avvertono rigidità e tensione tramite recettori specializzati come Piezo1. Questi segnali meccanici, insieme ai classici segnali immunitari, possono inclinare i macrofagi verso ruoli più infiammatori o più calmanti. Funzionalmente, i macrofagi possono inglobare le cellule tumorali, poi digerirle e presentarne frammenti (antigeni) ai linfociti T, facendo da ponte tra immunità innata e adattativa. Le cellule tumorali si difendono inviando segnali «non mangiarmi», in particolare tramite una molecola di superficie chiamata CD47 che si lega a un freno sui macrofagi. Farmaci che bloccano questa interazione sono in molti trial clinici, aumentando l’eliminazione delle cellule tumorali ma richiedendo un attento dosaggio per evitare danni alle cellule sane.
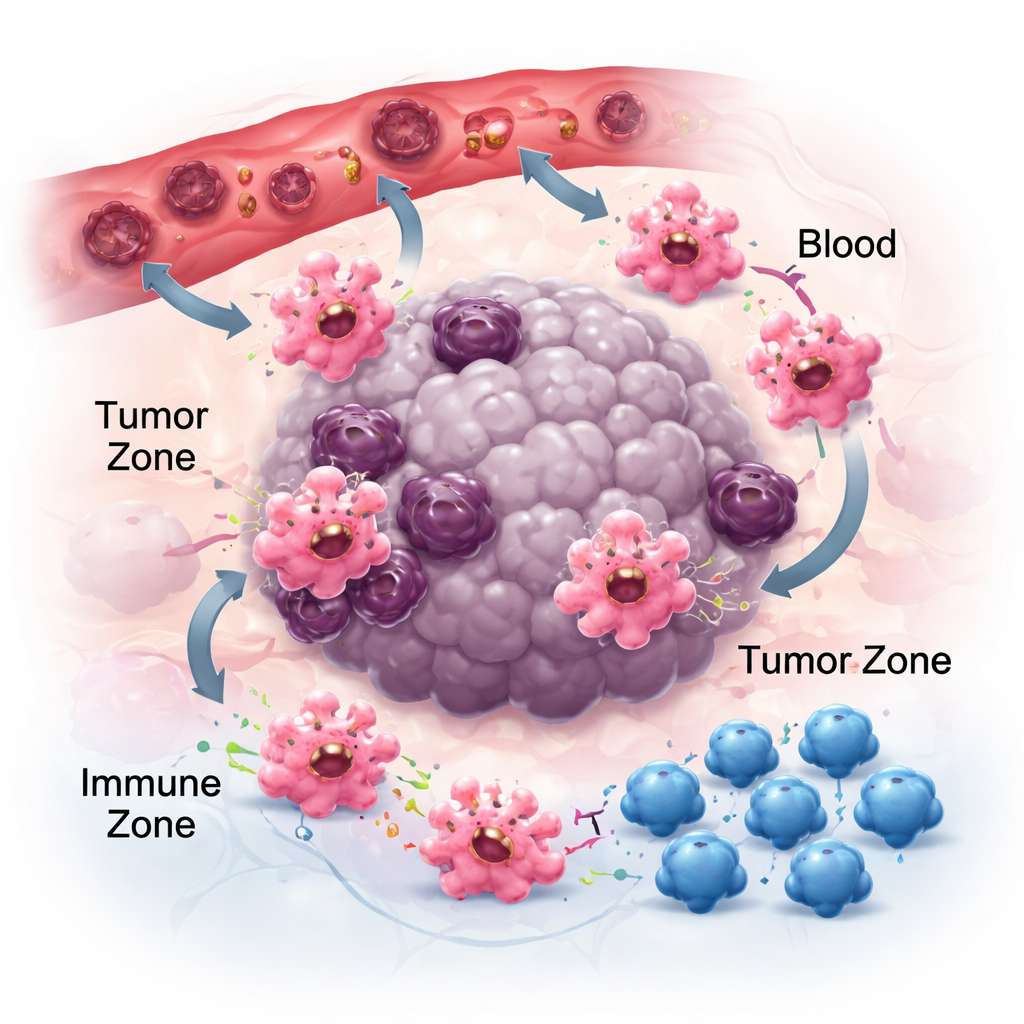
Muoversi, aderire e comunicare nel quartiere tumorale
Per avere effetto nel cancro, i macrofagi devono prima raggiungere i tumori e poi posizionarsi nelle nicchie giuste. Seguono scie chimiche—chemochine e fattori di crescita—rilasciate dalle cellule tumorali e da quelle circostanti. Coppie come CCR2–CCL2 aiutano ad attrarli nei tumori, e farmaci che bloccano questi segnali possono ridurre l’accumulo di macrofagi, seppure non completamente, indicando la presenza di altri attrattori come CSF-1 e VEGF. Una volta sul posto, il modo in cui i macrofagi si attaccano alla matrice locale influisce sul loro comportamento. I loro recettori di adesione, detti integrine, non agiscono solo come «colla»; amplificano segnali infiammatori e possono spingere le cellule verso stati più anti-tumorali. Allo stesso tempo, i macrofagi rilasciano piccole vescicole extracellulari che trasportano RNA e proteine alle cellule vicine. A seconda del tipo di tumore, queste vescicole possono indebolire l’immunità e favorire la diffusione oppure rafforzare le risposte anti-tumorali, sottolineando la natura dipendente dal contesto della comunicazione dei macrofagi.
Riprogrammare i macrofagi con geni e materiali
Poiché i macrofagi infiltrano naturalmente i tumori solidi meglio di molte cellule T, i ricercatori li stanno ora re-ingegnerizzando come medicine viventi. Una strategia genetica prende spunto dalla terapia con cellule T a recettore chimerico (CAR): aggiungere un recettore sintetico per creare macrofagi CAR (CAR-M). Queste cellule progettate riconoscono marcatori tumorali, inglobano più efficacemente le cellule maligne, degradano la matrice circostante, rilasciano segnali infiammatori e attivano i linfociti T presentando antigeni tumorali. I primi trial umani su CAR-M mirati a HER2 mostrano sicurezza e attività biologica incoraggianti, sebbene sia necessario altro lavoro per dimostrare benefici robusti e duraturi. In parallelo, approcci non genetici utilizzano particelle e «zaini» fatti di lipidi o polimeri. I macrofagi possono ingerire nanoparticelle cariche di farmaco e trasportarle in profondità nel tumore come cavalli di Troia, oppure indossare patch superficiali che rilasciano lentamente segnali immunostimolanti, aiutandoli a mantenere un’identità anti-tumorale senza sovraccaricare il loro interno. Anche le vescicole derivate dai macrofagi sono in fase di sperimentazione come veicoli naturali e senza cellule per la somministrazione.
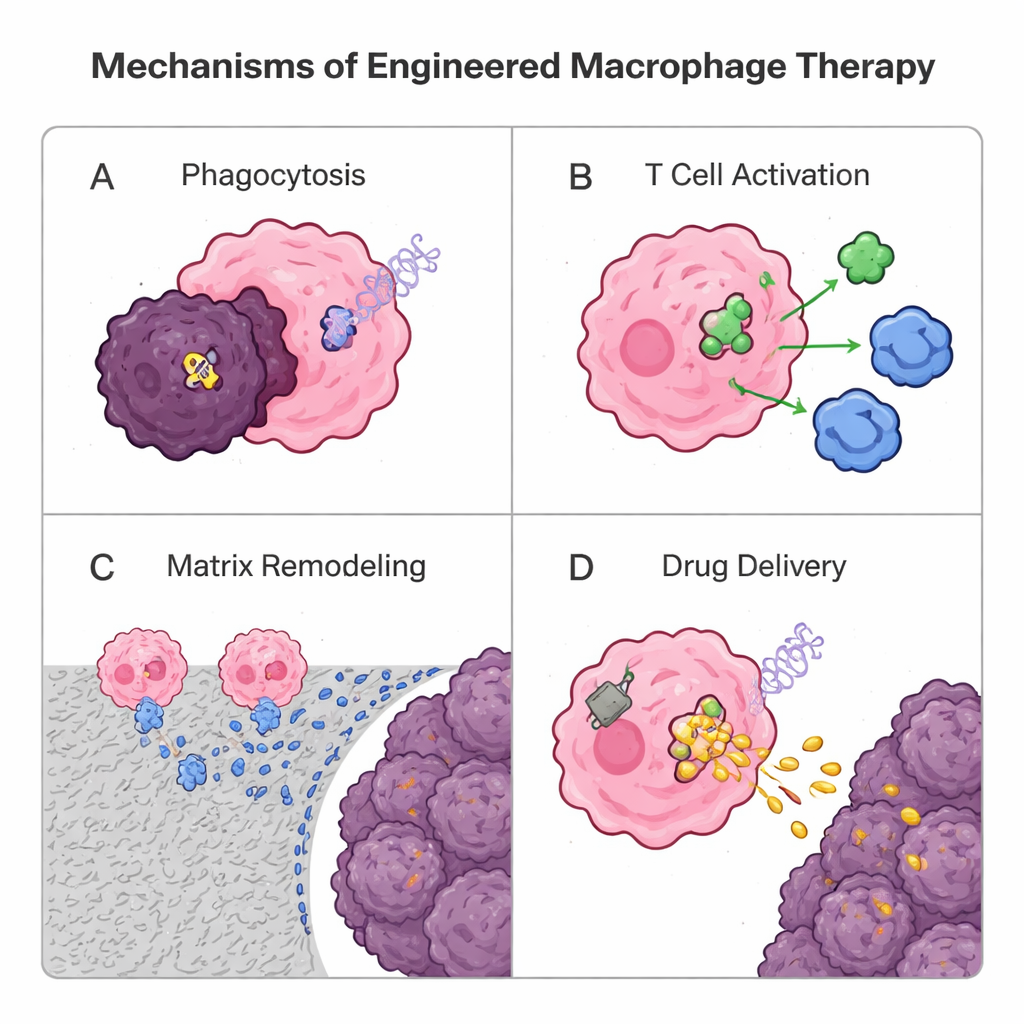
Prospettive e motivi di speranza
Nonostante le promesse, le terapie a base di macrofagi devono superare ostacoli pratici. È lungo e costoso generare un numero sufficiente di cellule consistenti dai pazienti e, una volta infuse, queste cellule non vivono né si moltiplicano indefinitamente. La loro flessibilità intrinseca, sebbene utile biologicamente, può rendere difficile mantenerle fissate in uno stato anti-tumorale all’interno di un microambiente tumorale complesso e soppressivo. Gli autori sostengono che modelli bioingegnerizzati avanzati—colture 3D, organoidi e sistemi organ-on-a-chip che imitano le meccaniche tissutali reali—saranno cruciali per comprendere e prevedere il comportamento dei macrofagi ingegnerizzati nei pazienti. Eppure, la loro capacità naturale di entrare nei tumori solidi, divorare cellule cancerose e risvegliare i linfociti T, unita a un primo quadro di sicurezza, suggerisce che le terapie basate sui macrofagi potrebbero diventare una nuova arma importante, soprattutto contro i tumori «freddi» che oggi resistono alla maggior parte dei trattamenti immunitari.
Citazione: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Parole chiave: immunoterapia con macrofagi, microambiente tumorale, CAR macrofagi, fagocitosi, somministrazione di farmaci con nanoparticelle